微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 同温同压下,等质量的下列气体所占有的体积最大的是( )
A.O3
B.NH3
C.CO2
D.NO2
参考答案:A.O3的摩尔质量为48g/mol;
B.NH3的摩尔质量为17g/mol;
C.CO2的摩尔质量为44g/mol;
D.NO2的摩尔质量为26g/mol,
由n=mM=VVm可知,V=m×VmM,同温同压下,Vm相等,则等质量的气体的体积与摩尔质量成反比,及摩尔质量越大,体积越小,摩尔质量最小的为NH3,则NH3的体积最大,
故选B.
本题解析:
本题难度:简单
2、选择题 将CH4、CO、H2三种气体分别装在三个容器中,当三者的温度和密度都相同时,三个容器中气体产生的压强大小的关系正确的是( )
A.CO>CH4>H2
B.CO>H2>CH4
C.H2>CH4>CO
D.H2>CO>CH4
参考答案:设容器的体积相同,则气体的质量相同,设质量为m,则有
n(CH4)=m16mol,
n(CO)=m28mol,
n(H2)=m2mol,
当体积、温度相同时,气体的压强与物质的量成正比,
则三个容器中气体产生的压强大小的关系为H2>CH4>CO,
故选C.
本题解析:
本题难度:一般
3、选择题 相同状况下,下列气体所占体积最大的是( )
A.3gH2
B.16gO2
C.32gH2S
D.64gSO2
参考答案:相同状况下,气体摩尔体积相等,根据V=nVm=mMVm知,气体的物质的量越大则气体体积越大,
氢气的物质的量=3g2g/mol=1.5mol,
氧气的物质的量=16g32g/mol=0.5mol,
硫化氢的物质的量=32g34g/mol<1mol,
二氧化硫的物质的量=64g64g/mol=1mol,
所以氢气的物质的量最大,则相同条件下,氢气的体积最大,
故选:A.
本题解析:
本题难度:简单
4、选择题 设NA 代表阿伏加德罗常数的数值,下列说法正确的是
A.1 mol磷酸钾中阴离子所带电荷数为NA
B.在18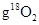 中含有
中含有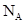 个18O原子
个18O原子
C.0.10mol Fe粉与足量水蒸气反应转移的电子数为0.30 NA
D.将0.1mol硅酸钠溶于1L水中,所得溶液中含有0.2NA个Na+
参考答案:BD
本题解析:
正确答案:BD
A.不正确,1 mol磷酸钾中阴离子所带电荷数为3NA
C.不正确,0.10mol Fe粉与足量水蒸气反应转移的电子数为0.27NA
本题难度:一般
5、选择题 依照阿伏加德罗定律,下列叙述正确的是( )
A.同温同压下两种气体的体积之比等于摩尔质量之比
B.同温同压下两种气体的物质的量之比等于密度之比
C.同温同压下两种气体的摩尔质量之比等于密度之比
D.同温同体积下两种气体的物质的量之比等于压强的反比
参考答案:A.由n=mM=NNA=VVm可知,相同质量时,同温同压下两种气体的体积与摩尔质量呈反比,故A错误;
B.同温同压下,由ρ=mV=MVm可知,相同质量的两种气体,摩尔质量越大密度越大,而摩尔质量越大物质的量越小,二者呈反比,故B错误;
C.由ρ=mV=MVm可知,同温同压下两种气体的摩尔质量之比等于密度之比,故C正确;
D.由PV=nRT可知,同温同体积下两种气体的物质的量之比等于压强的正比,故D错误.
故选C.
本题解析:
本题难度:一般