微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 区别NaCl、FeCl3和NH4Cl三种溶液,可选用下列试剂中的( )
A.KSCN溶液
B.BaCl2溶液
C.NaOH溶液
D.AgNO3溶液
参考答案:A.KSCN溶液只能鉴别出FeCl3,不能区分,故A错误;
B.BaCl2溶液与三者溶液均不反应,不能区分,故B错误;
C.NaCl、NH4Cl和FeCl3三种溶液分别与NaOH溶液反应的现象为:无现象、有刺激性气味的气体、红褐色沉淀,现象不同,能区分,故C正确;
D.AgNO3溶液与三者溶液反应均生成白色沉淀,现象相同,不能区分,故D错误;
故选C.
本题解析:
本题难度:一般
2、实验题 请用下列装置设计一个实验,证明Cl2的氧化性比I2的氧化性强。
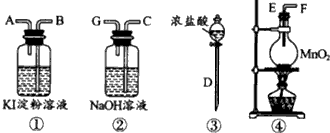
请回答下列问题:
(1)若气流从左到右,则上述仪器的连接顺序为D 接E,_____接____,____接____。
(2)圆底烧瓶中发生反应的化学方程式为____。
(3)证明Cl2比I2的氧化性强的实验现象是 ___,反应的离子方程式是____。
(4)装置②的作用是___。
(5)若要证明Cl2的氧化性比Br2强,则需做的改动是____。
参考答案:(1)F ;B ;A ;C
(2) MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(3)①中溶液变蓝;Cl2+2I-=2Cl-+I2
(4)吸收多余的氯气
(5)将①中KI淀粉溶液换成NaBr溶液
本题解析:
本题难度:一般
3、实验题 已知稀溴水和氯化铁溶液都呈黄色,某化学活动小组进行了如下实验探究:同学甲与乙分别在足量的氯化亚铁溶液中加入1~2滴液溴,振荡后溶液呈黄色。
(1)同学甲认为这不是发生化学反应所致,则使溶液呈黄色的微粒是:________(填粒子的化学式);同学乙则认为这是发生化学反应所致,试写出对应的离子方程式:________________________。
(2)查阅资料可知同学乙的判断正确。请根据下面提供的可用试剂,用两种方法加以验证,证明乙同学的判断正确,并将选用的试剂代号及实验中观察到的现象填入下表。
(实验可供选用的试剂:A.碘化钾淀粉溶液 B.氢氧化钠溶液 C.硝酸银溶液D.硫氰化钾溶液 E.四氯化碳 F.酸性高锰酸钾溶液)
参考答案:(1)Br2;Br2+2Fe2+==2Fe3++2Br-(2)
本题解析:
本题难度:一般
4、实验题 (14分)有一化学样品Na2SO3,可能含有NaCl、Na2SO4、KNO3、K2CO2、K2SO4中的一种或几种杂质,某实验小组利用图12提供的装置确定该样品的成分及Na2SO3的质量分数。称此样品6.30g,加入6.0mol・L-1的硫酸至过量,产生无色气体560mL(标准状况),向逸出气体后的溶液中加入稍过量的BaCl2溶液,得到白色沉淀9.32g,透过蓝色钻玻璃观察,滤液的焰色反应无紫色。请回答下列问题:
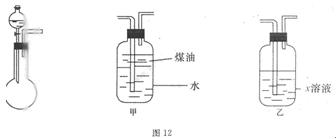
(1)溶液X是?,煤油的作用是?。
(2)若实验中加入硫酸溶液的体积为5.00mL,则样品中Na2SO3的质量分数是?,
写出有关离子方程式?。
(3)结合已提供的实验仪器,设计实验(实验仪器自选)如何正确测出气体的体积,简述操作步骤:??
?。
(4)说明一定含有硫酸钠的依据:??
? ?。
?。
参考答案:(1)X溶液是浓H2SO4(1分),作用是防止SO2与水接触(1分, 其它合理答案参照给分)
其它合理答案参照给分)
(2)50%(2分)SO32-+2H+=SO2↑+H2O(3分)? Ba2++SO42-=BaSO4↓ (2分)
(3)反应装置冷至室温后,再上下移动量筒,使量筒与甲瓶内液面保持水平,然后读取体积。(其它合理答案参照给分,3分)
(4)产生沉淀的物质的量为0.04mol,而加入的硫酸物质的量为0.03mol ,所以必有硫酸钠(其它合理答案参照给分,2分)
本题解析:略
本题难度:一般
5、选择题 下列实验方案不可行或结论不正确的是
① 用酸性高锰酸钾溶液除去乙烷气体中的少量乙烯
② 将溴乙烷和NaOH溶液混合加热后,再加入硝酸银溶液,检验溴元素
③ 分液时,分液漏斗里下层液体从下口放出,上层液体从上口倒出
④ 向同pH、同体积的醋酸和盐酸溶液中加入足量镁粉至完全反应,通过比较产生H2的体积判断两种酸的电离程度:醋酸<盐酸
⑤ 向新制的AgCl乳白色悬浊液中滴加0.1 mol/L的KI溶液,产生黄色沉淀,证明:Ksp[AgCl]>Ksp[AgI]
A.①②
B.①③⑤
C.②④
D.③④⑤
参考答案:A
本题解析:①、酸性高锰酸钾溶液能把乙烯氧化生成CO2,因此不能用酸性高锰酸钾溶液除去乙烷气体中的少量乙烯,应该用溴水,①不正确;
②、将溴乙烷和NaOH溶液混合加热后,应该先加入硝酸酸化后,再加入硝酸银溶液,检验溴元素,②不正确;
③、分液时,分液漏斗里下层液体从下口放出,上层液体从上口倒出,③正确;
④、醋酸是弱酸,存在电离平衡,因此在pH相同的条件下,醋酸的浓度大于盐酸的浓度。则向同pH、同体积的醋酸和盐酸溶液中加入足量镁粉至完全反应,醋酸产生的气体体积多,所以通过比较产生H2的体积判断可以两种酸的电离程度是醋酸<盐酸,④正确;
⑤、由于沉淀容易向生成更难溶的方向进行,所以向新制的AgCl乳白色悬浊液中滴加0.1 mol/L的KI溶液,如果产生黄色沉淀,则可以证明:Ksp[AgCl]>Ksp[AgI],⑤正确,答案选A。
本题难度:简单