微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图为一原电池的结构示意图,下列说法中,不正确的是
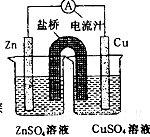
A.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu
B.原电池工作时,Zn电极流出电子,发生氧化反应
C.原电池工作时,铜电极上发生氧化反应,CuSO4溶液蓝色变深
D.盐桥中阳离子流向CuSO4溶液中
参考答案:C
本题解析:A、锌的金属性强于铜,根据装置图可知,锌是负极,电极反应式为Zn-2e-=Zn2+。铜是正极,溶液中的铜离子得到电子,电极反应式为Cu2++2e-=Cu,所以总的反应式为Zn+Cu2+=Zn2++Cu,A正确;B、锌是负极,铜是正极,所以原电池工作时,Zn电极流出电子,发生氧化反应,B正确;C、铜是正极,溶液中的铜离子得到电子,发生还原反应,溶液颜色变浅,C不正确;D、原电池电子从负极沿导线传递到正极,所以原电池中阳离子向正极移动,则盐桥中阳离子流向CuSO4溶液中,D正确,答案选C。
本题难度:一般
2、填空题 如图在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地向烧杯中央滴入硫酸铜溶液。
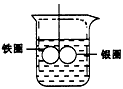
(1)片刻后可观察到的现象是(指悬吊的金属 圈)_______________。
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变 C.铁圈向下倾斜 D.银圈向下倾斜
(2)产生上述现象的原因是__________________________________。
参考答案:(1)D
(2)加入硫酸铜溶液后,构成Fe-Ag原电池,Fe溶解,减轻,Cu2+在银圈上得到电子,并沉积在其上,使其增重,所以银圈向下倾斜
本题解析:
本题难度:一般
3、选择题 下图是一种航天器能量储存系统原理示意图。下列说法正确的是

[? ]
A.该系统中只存在3种形式的能量转化
B.装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH-
C.装置X能实现燃料电池的燃料和氧化剂再生
D.装置X、Y形成的子系统能实现物质的零排放, 并能实现化学能与电能间的完全转化
参考答案:C
本题解析:
本题难度:一般
4、选择题 下列几种铁板,在镀层被破坏后,铁被腐蚀最慢的是
A 镀锌铁板? B. 镀铜铁板? C. 镀锡铁板? D. 镀铅铁板
参考答案:A
本题解析:铁主要是电化学腐蚀,当铁在原电池中做正极即可牺牲阳极保护铁不受腐蚀
本题难度:一般
5、填空题 根据所学知识回答下列问题,在如图所示装置中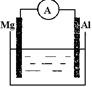 ,
,
(1)若烧杯中溶液为稀硫酸,则观察到的现象为??,正极反应式为??,负极反应式为?,
该装置中的能量变化形式为?。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为?,装置中总反应方程式为?。
参考答案:(1)电流表指针偏转,铝片表面冒气泡(2分);2H++2e-=H2↑(1分),Mg-2e-=Mg2+(1分),化学能转化为电能(1分)。(2)Al(1分),2Al+2NaOH+2H2O=2NaAlO2+2H2↑(2分)。
本题解析:原电池反应属于自发的氧化还原反应,镁比铝活泼,但在氢氧化钠溶液中,铝能反应而镁不能。
本题难度:简单