|
���л�ѧ֪ʶ�㽲�⡶����ԭ����������ѵ��2017���̰棩(ʮ)
2017-07-18 00:27:14
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ⷨ��ȡ�Ȼ�ͭ��Һ�е�ͭ��������ȷ���ǣ�?��
A����ͭƬ���ӵ�Դ����������һ�缫�ò�Ƭ
B����̼�����ӵ�Դ����������һ�缫��ͭƬ
C��������������Һ������������
D���ô����ǵ�ľ��������������
�ο��𰸣�B
���������
A������ȷ����ͭƬ���ӵ�Դ�ĸ�������һ�缫�ò�Ƭ �� B����ȷ�� C������ȷ��������������Һ������������ �� D������ȷ����ʪ��ĵ��۵⻯����ֽ������������Cl2��ѡB��
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ����
A���ȼҵ�У��ռ�������������
B����������Ȼ���ұ��������
C�����ʱ���öƲ����������
D������բ�������Դ�����������ɷ�ֹ�丯ʴ
|
�ο��𰸣�C
����������ȼҵ�ǵ�ⱥ�͵��Ȼ��ƣ�����������������������������������ˮ�е������ӣ��ٽ�ˮ�ĵ��룬����Һ�Լ��ԣ������������������ɣ�A�����Ȼ����ǹ��ۻ������Ӧ������ڵ�����������ȡ��������B�����ʱ���Ʋ�������������Ƽ���������C��ȷ������բ������ӵ�Դ�ĸ����������ɷ�ֹ��ʴ��������ӵ�Դ��������������D����ѡC.
���㣺���ԭ��
�����Ѷȣ�һ��
3������� ��10�֣���ͼΪ������ļ����������أ���ش�

�׳���Ϊ�õ�⾫��ͭ��װ�ã�
��1��A���缫��ӦΪ?��
B���缫��ӦΪ_?_��
�ҳ��е��ܷ�Ӧ���ӷ���ʽΪ?��
��2�����ײ���������12.8g�����Ҳ������ų������ڱ�״���µ����Ϊ?��
��3�����Ҳ�ʣ��Һ��Ϊ400mL�������õ���Һ�����ʵ���Ũ��Ϊ?��
�ο��𰸣���10�֣� ��1�� Cu2+ + 2e�C==?Cu?��? Cu ��2e�C="=" ?Cu2+
2Cl- + 2H2O 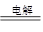 ?Cl2�� + 2OH- + H2 ��?��2�� 4.48L?��3��? 1? mol��L-1 ?Cl2�� + 2OH- + H2 ��?��2�� 4.48L?��3��? 1? mol��L-1
�����������1��A�����Դ�ĸ���ѵ�������������������ӵ��Ǵ�ͭ����缫��ӦʽΪCu2+ + 2e�C==?Cu����B�缫�������������ӵ��Ǵ�ͭ���缫��Ӧʽ��Cu ��2e�C="=" ?Cu2+���ҳ���C�缫��������������������ⱥ��ʳ��ˮ�����ܵ����ӷ���ʽ��2Cl- + 2H2O 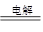 ?Cl2�� + 2OH- + H2 ���� ?Cl2�� + 2OH- + H2 ����
��2���ײ���������12.8g��������ͭ��12.8g�����ʵ�����0.2mol��ת�Ƶ�����0.4mol������ݵ��ӵĵ�ʧ�غ��֪���Ҳ������ų����������0.2mol��22.4L/mol��4.48L��
��3�����ݣ�2����֪��������0.2mol������������������0.4mol�����ʵ���Ũ����0.4mol��0.4L��1.0mol/L��
�����������ǻ���������Ŀ��飬���������ǿ�����ؿ���������û���֪ʶ���ʵ������������������ѶȲ��ؼ���Ҫ�������յ绯ѧԭ����ѧ�����ѵ÷֡�
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����

[? ]
A��Cu(s)+2H2O(l)===2Cu(OH)2 (s)+H2(g)���÷�Ӧ��ͨ����ͼװ����ʵ��
B��������ɱ���ܱ������н��з�Ӧ��CaCO3(s)  CaO(s)+CO2(g)�ﵽƽ���ѹ���������v��������v���棩������ƽ�����淴Ӧ�����ƶ� CaO(s)+CO2(g)�ﵽƽ���ѹ���������v��������v���棩������ƽ�����淴Ӧ�����ƶ�
C��Zn(s)+CuSO4(aq)===ZnSO4(aq)+Cu(s) ��H<0���ɸ÷�Ӧ��֪����������ϵһ�����ϣ�E [ZnSO4(aq)] < E [CuSO4(aq)]
D�����ܱ������н��з�Ӧ��HI(g) H2(g)+I2(s)��H��-26.5 kJ��mol-1,�������1 mol HI���ﵽƽ���ų�26.5 kJ������ H2(g)+I2(s)��H��-26.5 kJ��mol-1,�������1 mol HI���ﵽƽ���ų�26.5 kJ������
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5��ѡ���� ���ε���Ҫ�ɷ���KIO3��NaCl��KIO3�ڹ�ҵ�Ͽ��õ�ⷨ��ȡ����ʯī����Ϊ�缫�����KI��Һ����Ӧ����ʽΪKI+3H2O��KIO3 +3H2���������й�˵������ȷ����?
A�����ʱ��ʯī����������������
B�����ʱ���������ϲ���KIO3
C������������ҺpH���
D�������ÿת��0.6mol e���������Ͽɵõ�0.1mol��ˮKIO3����
�ο��𰸣�D
���������A�����������������ŵ�Fe-2e-=Fe2-��I-��ת��ΪIO3-������ B��I-ת��ΪIO3-��I��-1�����ߵ�+5�ۣ�ʧȥe����������Ӧ���������Ϸ���������C����Ӧ����ʽΪKI+3H2O��KIO3 +3H2��,���������ĺ����ɣ���ҺpH���䣬���� D���������з�Ӧ��ÿת��6mol e���������Ͽɵõ�1mol KIO3����ת��0.6mol e���������Ͽɵõ�0.1mol��ˮKIO3����ȷ��
�����Ѷȣ���
|