微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 下面图表示制备无水盐E的主要步骤:
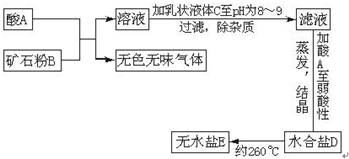
已知B是石灰石,D盐含有约49%的结晶水,无水盐E可用作干燥剂.取少量E溶于水,向其中滴加硝酸后,再滴加硝酸银溶液,有白色沉淀F生成.
填写以下空白(写出化学式或名称):
A______,C______,D______,E______,F______.
参考答案:这是一例典型的定性分析和定量分析相结合的推断题.
(一)定性分析:因为B是石灰石,和酸A反应,放出的无色无味气体应是CO2,生成可溶性钙盐,由此判定最终形成的无水盐E也是钙盐溶液,因为E溶于水后向其中滴加硝酸后,再滴加硝酸银溶液,有白色沉淀F生成,知F是AgCl,E是CaCl2,吻合了E可作干燥剂这条件,D是CaCl2的结晶水合物.
(二)定量分析:设无水盐为CaCl2?xH2O
? CaCl2?xH2O~xH2O
101+18x?18x ?
100?49
解之:x=6
则D盐化学式 CaCl2?6H2O酸A是盐酸,乳状液体C应是石灰乳,
故答案为:HCl(盐酸);Ca(OH)2(石灰乳);CaCl2?6H2O;CaCl2;AgCl.
本题解析:
本题难度:一般
2、填空题 A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示.
请回答下列问题:
(1)若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分,A和D反应生成B的化学方程式为______.B的结构式为______.
(2)若D为用量最大、用途最广的金属单质,加热蒸干B的溶液没有得到B的盐,继续灼烧后得到的固体物质成分是______.
(3)若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式为______.
(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一,也可作为医疗上治疗胃酸过多症的药剂.
①C溶液呈碱性的原因是______.(用离子方程式表示)
②将等物质的量的B和C溶于水形成混合溶液,溶液中各种离子浓度由大到小的顺序为______.
参考答案:(1)B和D为空气的主要成分,则为N2和O2,根据A→B→C的反应中都有D参加反应,则D应为O2,B为N2,转化关系为:NH3O2
本题解析:
本题难度:一般
3、推断题 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,右图是它们之间的相互转化关系。请回答:
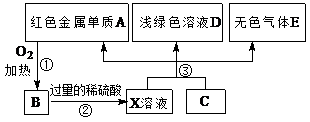
(1)反应①的基本反应类型是 ;
(2)C的化学式为 ;
(3)写出反应②的离子方程式 ? 。
(4)A和稀硫酸、双氧水生成X的化学方程式?。
参考答案:(6分)(1)化合反应(1分)? (2)Fe (1分)? (3) CuO+2H+ Cu2++H2O(2分)
Cu2++H2O(2分)
(4) Cu+H2O2+H2SO4="===" CuSO4+2H2O(2分)
本题解析:A为红色金属,可知A为铜,那么B为氧化铜;B与硫酸反应后的X溶液为硫酸和硫酸铜的混合溶液,X溶液和C 反应生成了浅绿色溶液,铜和无色气体E,可知C为铁单质,我们知道浅绿色溶液应该为硫酸亚铁溶液,即D为硫酸亚铁,无色气体E为氢气。
(1 )反应①是金属铜(A)和氧气在加热条件下生成氧化铜(B),反应为2Cu+O2点燃2CuO,反应物为两种,生成物为一种,为化合反应。
(2)由于生成的溶液D为浅绿色的,所以C含有和能硫酸铜和剩余硫酸反应的物质应该是金属铁,其化学式为Fe。
(3)反应②是氧化铜和过量的硫酸反应生成硫酸铜和水,其反应方程式为:CuO+H2SO4=CuSO4+H2O,离子方程式为CuO+2H+ Cu2++H2O。
Cu2++H2O。
(4)由于在B中加入了过量的硫酸,导致氧化铜与硫酸反应生成硫酸铜后,硫酸依然会有剩余,所以X为硫酸铜(生成的)和硫酸(剩余的)的混合溶液.
(5)根据分析,A是铜,X是CuSO4,故A和稀硫酸、双氧水生成X的化学方程式为Cu+H2O2+H2SO4="===" CuSO4+2H2O。考点:
点评:此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论。
本题难度:一般
4、推断题 A、B、C、D是中学化学的常见物质,其中 A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。

请填空:
(1)若D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不 能得到B,则B的化学式可能是____(只写一种)。
(2)若A是一种碱性气体,常用作制冷剂,B和D为空气的主要成分,则反应② 的化学方程式为___。
(3)若D为氯碱工业的主要产品,B有两性,则反应②的离子方程式是_____。
(4)若D为酸或酸性气体,则A、C可以是___(请按顺序写出任意一组符合要求的物质的化学式)。
(5)若C是一种温室气体,D是空气的主要成分之一,1 mol黑色固体A完全燃烧放出393.5 kJ热量,1 mol B气体完全燃烧放出283.0 kJ热量,则A→B反应的热化学方程式为________。
参考答案:(1)FeCl3
(2)N2 +O2 2NO
2NO
(3)Al(OH)3+OH-=[Al(OH)4]-
(4)NaOH、NaHCO3或Fe、Fe(NO3)3或 Na[Al(OH)4]、AlCl3或CaO、Ca(HCO3)2或 Na2CO3、CO2或Na2O2、NaHCO3等(其他合理答案均可)
(5)2C(石墨,s)+O2(g)=2CO(g) △H=221 kJ・mol-1
本题解析:
本题难度:一般
5、推断题 下图是一些常见的单质和化合物之间的转化关系图,有些反应中的部分物质被略去。常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为生活中最常用的金属单质,J为红褐色固体,L为两性氢氧化物。反应①、②均为工业上的重要反应。
请回答下列问题:?
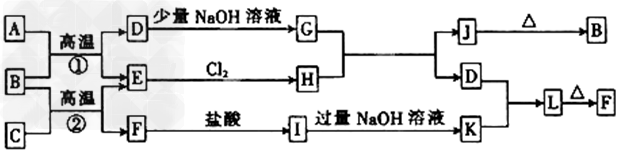
(1)写出B的化学式为_________;D的电子式为______________。?
(2)组成单质C的元素在元素周期表中的位置为_________________;
(3)写出向I溶液中加入过量NaOH溶液时发生反应的离子方程式____________________。
(4)写出向Na2SiO3溶液中通入少量D时发生反应的离子方程式___________________。
参考答案:(1)Fe2O3;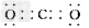
(2)第三周期IIIA族
(3)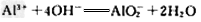
(4)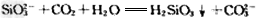
本题解析:
本题难度:一般