微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
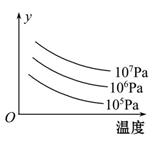
1、选择题 某密闭容器中,可逆反应 L(s)+G(g) 3R(g) ΔH>0,如图表示外界条件温度、压强的变化对上述反应的影响。下列表述正确的是(? )
3R(g) ΔH>0,如图表示外界条件温度、压强的变化对上述反应的影响。下列表述正确的是(? )
A.该反应达平衡后加入适当的催化剂可提高G的转化率
B.达到平衡后向容器中加入L,平衡向右移动,G的转化率增大
C.图中的y可能是平衡混合气中G的质量分数
D.图中的y可能是达到平衡时G的转化率
参考答案:C
本题解析:催化剂对化学平衡没有影响,对G的转化率没有影响,A错;平衡后向容器中加入L固体,对平衡没有影响,平衡不发生移动,G的转化率不变,B错;对于反应L(s)+G(g) 3R(g)?ΔH>0,升高温度平衡向正反应方向移动,混合气体中G的质量分数减小。增大压强平衡向逆反应方向移动,混合气体的质量减小,G的质量增大,混合气体中G的质量分数增大,C对;升高温度反应向正反应方向移动,G的转化率增大,增大压强G的转化率减小,D错。
3R(g)?ΔH>0,升高温度平衡向正反应方向移动,混合气体中G的质量分数减小。增大压强平衡向逆反应方向移动,混合气体的质量减小,G的质量增大,混合气体中G的质量分数增大,C对;升高温度反应向正反应方向移动,G的转化率增大,增大压强G的转化率减小,D错。
本题难度:一般
2、选择题 相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g)  2XY3(g) ΔH=-92.6 kJ・mol-1
2XY3(g) ΔH=-92.6 kJ・mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器
编号
| 起始时各物质的物质的量/mol
| 达到平衡时体系能量的变化
|
X2
| Y2
| XY3
|
①
| 1
| 3
| 0
| 放热:23.15 kJ
|
②
| 0.6
| 1.8
| 0.8
| Q(Q>0)
|
?
下列叙述不正确的是(?)
A.容器①、②中反应的平衡常数相等
B.容器②中反应达到平衡时放出的热量为Q
C.达到平衡时,两个容器中XY3的物质的量浓度均为2 mol・L-1
D.若容器①的体积为0.20 L,则达平衡时放出的热量大于23.15 kJ
参考答案:B
本题解析:平衡常数只与温度有关,温度不变,平衡常数不变,A项正确;由达平衡时①放出的热量为23.15 kJ,可知X2和Y2的转化率均为25%,即平衡时X2、Y2和XY3的物质的量分别为0.75 mol、2.25 mol和0.5 mol,此时XY3的物质的量浓度均为2 mol・L-1,可知②的反应应逆向进行,反应过程需要吸收热量,B项错误;两容器中反应达平衡时为等效平衡,故C项正确;增大压强平衡向正反应方向移动,放出热量多,D项正确。
本题难度:一般
3、填空题 (1)工业合成氨技术的反应原理是:N2(g)+3H2(g)
2NH3(g)△H=-92.4kJ/mol.在500℃、20MPa时,将N2、H2置于一个固定容积的密闭容器中发生反应,反应过程中各种物质的量变化如图1所示,回答下列问题:
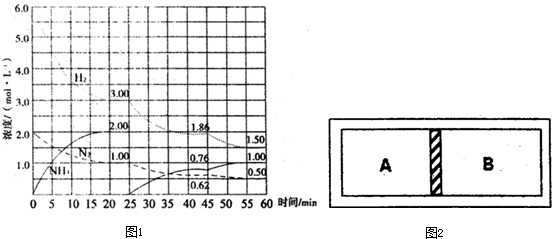
①计算反应在第一次平衡时平衡常数K=______(保留二位小数)
②产物NH3在5~10min、20~25min和45~50min时平均反应速率[平均反应速率分别以v1、v2、v3表示]从大到小排列次序为______.
③在45min时,采取的措施是______;
(2)如图2是一个体积固定的恒温密闭容器,正中间有一个可以滑动的隔板将容器隔成A、B两室.A室放入H2和O2共5mol,B室放入H2和N2共5mol,使隔板恰好处于正中间.
①控制一定条件,只使A室气体充分反应,此时隔板左移,待反应完成且密闭容器温度恒定(大于120℃)后,A室气体体积是B室体积的.计算原H2和O2的体积比为______.
②再控制一定条件,使H2和N2发生反应(正反应放热).当密闭容器温度恒定(大于120℃)且达到平衡时,隔板右移恰好回到正中间,若加入的N2为1mol,则N2的转化率为______,若加入的N2为xmol,则x的取值范围是______.
参考答案:(1)①第一次达到平衡常数时,氨气的浓度为:2.00mol/L,氢气浓度为:3.00mol/L,氮气的浓度为:1.00mol/L,
第一次平衡时平衡常数K=2.0021.00×3.003≈0.15,
故答案为:0.15;
②5~10min氨气的浓度变化大于0.5mol/L,20~25min氨气浓度变化为0,45~50min氨气的浓度变化小于0.50.5mol/L,时间变化为5min,由v=△c△t可知,反应速率关系为:v1>v3>v2,
故答案为:v1>v3>v2;
③45min时,氨气的浓度增大,氮气、氢气的浓度减小,化学平衡平衡向着正向移动,该反应是放热反应,说明降低了温度,
故答案为:降低温度;
(2)①A室气体体积是B室体积的45,A、B的压强相同,B的物质的量为5mol且不变,所以A反应后的物质的量为4mol,反应后气体减小了1mol,
2H2 +O2 点燃.2H2O△n
2 1 2 1
2mol1mol 1mol
反应消耗的氢气的物质的量为2mol、氧气的物质的量为1mol,所以氢气和氧气的物质的量有两种情况,
本题解析:
本题难度:一般
4、填空题 (8分) 已知3A(g)+B(g)  xC(g)+2D(g),将等物质的量的A、B混合于2 L的密闭容器中,经5 min后达到化学平衡,此时测得D的浓度为0.5 mol/L,且c(A)∶c(B)=3∶5。又知5 min 内用C表示的平均反应速率为0.1 mol/(L・min)。求:
xC(g)+2D(g),将等物质的量的A、B混合于2 L的密闭容器中,经5 min后达到化学平衡,此时测得D的浓度为0.5 mol/L,且c(A)∶c(B)=3∶5。又知5 min 内用C表示的平均反应速率为0.1 mol/(L・min)。求:
(1)反应开始前容器中的A、B的物质的量:n(A)=n(B)=________mol;
(2)5min内用B表示的平均反应速率v(B)= ________mol/(L・min);?
________mol/(L・min);?
(3)此时A的转化率为_______,x的值为________。
参考答案:(1) ___3__ ___mol;?(2) v(B)=______0.05__mol/(L・min);?
___mol;?(2) v(B)=______0.05__mol/(L・min);?
(3)____50%__,x的值为__2______。
本题解析:略
本题难度:一般
5、填空题 (5分)汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、100 kPa下,ΔH=-113 kJ・mol-1,ΔS=-145 J・(mol・K)-1.
(1)为了提高该反应的速率和NO的转化率,采取的正确措施为?
A.加催化剂同时升高温度
B.加催化剂同时增大压强
C.升高温度同时充入N2
D.降低温度同时增大压强