微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是()
A.复分解反应中有的是氧化还原反应,有的不是氧化还原反应
B.置换反应有可能是非氧化还原反应
C.化合反应一定是氧化还原反应
D.分解反应不一定是氧化还原反应
参考答案:D
本题解析:复分解反应都不是氧化还原反应;置换反应都是氧化还原反应;有单质生成的分解反应和有单质参加的化合反应是氧化还原反应,因此正确的答案选D。
本题难度:一般
2、填空题 (4分)用双线桥法表示下列反应方程式中电子转移的方向和数目,并指出氧化剂和氧化产物。
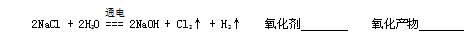
参考答案:

本题解析:略
本题难度:简单
3、填空题 (12分)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。
(1)CoxNi(1-x)Fe2O4(其中Co、Ni均为+2)可用作H2O2分解的催化剂,具有较高的活性。
①该催化剂中铁元素的化合价为 。
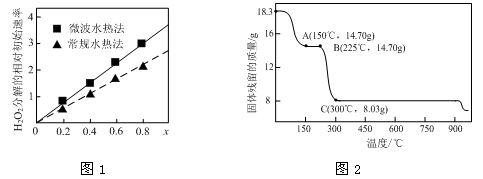
②图1表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线。由图中信息可知: 法制取得到的催化剂活性更高;Co2+、Ni2+两种离子中催化效果更好的是 。
(2)草酸钴是制备钴的氧化物的重要原料。下图2为二水合草酸钴(CoC2O4・2H2O)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物。
①通过计算确定C点剩余固体的化学成分为 (填化学式)。试写出B点对应的物质与O2在225℃~300℃发生反应的化学方程式: 。
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL 5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比。
参考答案:(1)①+3 ②微波水热 Co2+
(2)① Co3O4(写成CoO・Co2O3亦给分) 3CoC2O4 + 2O2 = Co3O4 +6CO2
②由电子守恒:n(Co3+) =" 2" n(Cl2) =" 0.4" mol(1分)
由电荷守恒:n(Co)总=n(Co2+)溶液=" 0.5" n(Cl-) =" 0.5×(" 2.4mol-0.2mol×2)=" 1" mol
所以固体中的n(Co2+)= 1mol-0.4mol=" 0.6" mol(1分)
n(O)=(0.4mol×3+0.6mol×2)÷2=1.2mol(1分)
故n(Co):n(O)=1mol:1.2mol=5:6(1分)
(除第(1)②小题每空1分,第(2)②小题4分外,其余每空2分,共12分)
本题解析:(1)①该催化剂中Co、Ni均为+2价,O为-2价,所以Fe元素的化合价是[8-(2x+2-2x)]/2=+3;
②反应速率越快,则催化剂的催化活性越高,根据图像可知,x相同时微波水热法初始反应速率大于常规水热法,所以微波水热法制取得到的催化剂活性更高;随x增大,初始速率增大,而x增大,Co2+的比例增大,所以Co2+的催化效果更好;
(2)①由题意知,二水合草酸钴(CoC2O4・2H2O)的起始质量是18.3g,物质的量是0.1mol,其中Co元素的质量是5.9g,300℃时该固体分解为Co的氧化物,C点固体质量是8.03g,则O元素的质量是8.03g-5.9g=2.13g,物质的量是2.13g/16g/mol=0.133125mol,则该固体中Co与O原子的物质的量之比是0.1:0.133125=3:4,所以C点对应固体的化学式是Co3O4;B点对应的物质的质量是14.70g,与 起始的固体质量相比减少18.3-14.7=3.6g,恰好为结晶水的质量,所以B点对应的物质是草酸钴,与O2在225℃~300℃发生反应生成Co3O4和二氧化碳,所以反应的化学方程式是3CoC2O4 + 2O2 = Co3O4 +6CO2;
②设该钴的氧化物中+3价Co的原子个数是x,与盐酸反应得到的黄绿色气体为氯气,物质的量是4.48L/22.4L/mol=0.2mol,则反应中失去电子的物质的量是0.4mol,Co最终都变为+2价,则+3价Co得到电子的物质的量是x=0.4,480 mL 5 mol/L盐酸中氯离子的物质的量是0.48L×5mol/L=2.4mol,被氧化的氯离子的物质的量是0.4mol,所以溶液中还余氯离子的物质的量是2.4-0.4=2.0mol,根据Cl元素守恒,所以CoCl2的物质的量是1.0mol,则钴的氧化物中+2价钴的物质的量是1.0-0.4=0.6mol,根据正负化合价的代数和为0,则钴的氧化物中O元素的物质的量是(0.4mol×3+0.6mol×2)/2=1.2mol,所以该钴氧化物中Co、O的物质的量之比为1.0:1.2=5:6.
考点:考查元素化合价的判断,物质化学式的计算,得失电子守恒规律的应用
本题难度:困难
4、填空题 (每空2分,共10分)
(1) 除去NaHCO3溶液中混有的Na2CO3,相应的化学方程式_____________。
(2) 除去Na2CO3固体中混有的NaHCO3,相应的化学方程式_____________。
(3) 除去CO2气体中混有的HCl,相应的离子方程式___________________。
(4) 除去Fe2O3中混有的Al2O3,相应的离子方程式_____________________。
(5) 除去FeCl3溶液中混有的FeCl2,相应的离子方程式_________________。
参考答案:(10分)
(1) Na2CO3 + H2O + CO2= 2NaHCO3 (2分)
(2分)
(2) 2NaHCO3==Na2CO3 + H2O + CO2↑(2分)
(3) HCO3-+ H+ = H2O + CO2↑(2分)
(4) Al2O3+2OH-===2AlO2-+H2O(2分)
(5) 2Fe2++Cl2=2Fe3+ + 2Cl-(2分)
本题解析:略
本题难度:简单
5、选择题 我国所生产的碘盐中含有少量的碘酸钾(KIO3),以补充人体所需的碘元素而预防甲状腺疾病,而核应急专用碘片中含有的主要成分是碘化钾(KI),食用一定的碘片可以阻止放射性碘被人体甲状腺所吸收,那碘化钾中碘元素的化合价为(?)
A.+5
B.+1
C.―5
D.―1
参考答案:D
本题解析:钾+1按照化合物化合价代数和为零可得,碘元素的化合价是-1价。故选D。
点评:此类题目是较为简单的题目,所以,只要熟悉基本的原理及氧化还原反应的概念,此类问题便不难解决。
本题难度:简单