��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����йػ�ѧ�����ʾ����ȷ����
A������ԭ�ӽṹʾ��ͼ��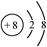
B��Na2O2�ĵ���ʽ��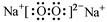
C��HClO�Ľṹʽ��H��O��Cl
D��������Ϊ16�������ӣ�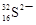
�ο��𰸣�A
���������A������ȷ����ԭ�������ֻ��6�����ӣ���������ԭ�ӽṹʾ��ͼ�� ��B��Na2O2�����ӻ����O22�D��������ԭ�Ӽ��γ�һ�Թ��õ��Ӷԣ���ȷ��C��HClO��������Ϊ+2�ۣ��γ�2�����õ��Ӷԣ�C��ȷ��D��ԭ�ӷ��ŵ����ϽDZ�ʾ������������������������֮�ͣ���ȷ��
��B��Na2O2�����ӻ����O22�D��������ԭ�Ӽ��γ�һ�Թ��õ��Ӷԣ���ȷ��C��HClO��������Ϊ+2�ۣ��γ�2�����õ��Ӷԣ�C��ȷ��D��ԭ�ӷ��ŵ����ϽDZ�ʾ������������������������֮�ͣ���ȷ��
�����Ѷȣ���
2��ѡ���� 2.3g���ڸ���Ŀ����б������ɵ�3.5g���壬��˿��ж�����������Ϊ(����)
A��Na2O2
B��Na2O
C��Na2O��Na2O2
D����ȷ��
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
3������� ��ѧ��ѧ����������A��B��C��D֮���������ת����ϵ��A+B��C+D+H2O��û����ƽ�����밴Ҫ����գ�
��1����AΪ������Ԫ����ɵĺ�ɫ���嵥�ʣ���B��Ũ��Һ����ʱ������C��D�������壮C��D�����������ʹ����ʯ��ˮ����ǣ���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�______���������������岻��ѡ�õ��Լ���______
a��BaCl2��Һ?b��KMnO4��Һ?c��Ʒ����Һ? d���ữ��Ba��NO3��2��Һ
��500mL2mol/L��NaOH��Һ��ͨ��0.8mol��ɫ��ζ��C���壬ǡ����ȫ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽ��______����ʱ��Һ�е����Ӱ���Ũ���ɴ�С���е�˳����______��
��2����AΪ��ɫ�������ʣ�������B����Һ�ڳ�����ǡ����ȫ��Ӧ�����ɵ���ɫ����C������Ѹ�ٱ�ɾ���ɫ��������ԭ��B���ʵ���Ϊ2molʱ������C����������______?L��������������ɵĺ���ɫ����ͨ��һ����ƿ�����ƿ������ƿ�����ˮ�У���ƿ���������ɫ��dz�����û�ѧ����ʽ�ͱ�Ҫ�����ֽ�����ɫ�仯��ԭ��______��
��3����A��ˮ�е��ܽ�����¶ȵ����߶����ͣ�BΪ�����ڷǽ������ʣ�D��Ư�۵ijɷ�֮һ��C����ˮ�ⷴӦ�����ӷ���ʽ��______
��4����AΪ���10���ӵ��������뵥��18���ӵ������ӹ��ɵ���ɫ���壬�����ֽ⣬�ֽ���������ּ�������ˮ�����壮����A�������ӵķ�����______�������������̼����ۣ���
�ο��𰸣���1��C��D�����������ʹ����ʯ��ˮ����ǣ���ʹ����ʯ��ˮ����ǵ������Ƕ�����̼�Ͷ�����������C��D�Ͷ�����̼�Ͷ�������A��̼�����������£�̼��Ũ���ᷴӦ���ɶ�����̼�����������ˮ����Ӧ����ʽΪ��C+2H2SO4��Ũ��?��?.??CO2��+2SO2��+2H2O��
������̼�Ͷ���������ͬ�������Ƕ���ʹ����ʯ��ˮ����ǣ���ͬ���Ƕ����������Ư���Ժͻ�ԭ�ԣ�
a����������Ͷ�����̼�������Ȼ�����Ӧ������������ͬ�������𣬹�ѡ��
b������������ʹ���Ը��������ɫ��������̼����ʹ���Ը��������Һ��ɫ�������ܼ��𣬹ʲ�ѡ��
c������������ʹƷ����Һ��ɫ��������̼����ʹƷ����Һ��ɫ�������ܼ��𣬹ʲ�ѡ��
d�����������ܺ������ữ�����ᱵ��Ӧ���ɰ�ɫ������������̼���ܺ������ữ�����ᱵ��Ӧ�������ܼ��𣬹ʲ�ѡ��
��ѡa��
�������Ƶ����ʵ���=2mol/L��0.5L=1mol��������̼�����ʵ�����0.8mol��1��n(NaOH)n(CO2)=54��2�������������ƺͶ�����̼��Ӧ����̼���ƺ�̼�����ƣ��������ƺͶ�����̼ǡ�÷�Ӧ����̼���ƺ�̼�����ƣ���Ӧ����ʽΪ5NaOH+4CO2�TNa2CO3+3NaHCO3+H2O��
5NaOH+4CO2�TNa2CO3+3NaHCO3+H2O��
5mol 4mol? 1mol? 3mol
1mol 0.8mol 0.2mol 0.6mol
ͨ������ʽ֪������0.2mol̼���ơ�0.6mol̼�����ƣ������Ӳ�ˮ��Ũ�������Ȼ̼���ƺ�̼��������ˮ�⣬��������Һ���Ե���Ϊ����ˮ��Ϊ�Σ�����̼���������Ũ�ȴ���̼�������Ũ�ȣ�̼������Ӻ�̼���������ˮ�������������Ũ�ȴ���������Ũ�ȶ�ʹ��Һ�ʼ��ԣ���������Ũ�ȴ�С˳��Ϊ��c��Na+����c��HCO3-����c��CO3 2- ����c��OH-����c��H+����
�ʴ�Ϊ��C+2H2SO4��Ũ��?��?.??CO2��+2SO2��+2H2O��a��5NaOH+4CO2�TNa2CO3+3NaHCO3+H2O��c��Na+����c��HCO3-����c��CO3 2- ����c��OH-����c��H+����
��2����ɫ����C������Ѹ�ٱ�ɾ���ɫ������C��NO��AΪ��ɫ��������ͭ��ͭ��ϡ���ᷴӦ��������ͭ��һ��������ˮ������B��ϡ���ᣬ���ݵ�ԭ���غ����һ�����������������NO���ΪX��
HNO3----NO��
1mol? 22.4L
2mol? x
x=44.8L
��������������ת��Ϊ�������������Ҷ�������������������֮����ڻ�ѧƽ�⣬�÷�Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ���������ɫ��dz��
�ʴ�Ϊ��44.8��2NO2������ɫ��?N2O4����ɫ������H��0�����£�ƽ��������Ӧ�����ƶ�������ɫNO2Ũ�ȼ�С������������ɫ��dz��
��3����A��ˮ�е��ܽ�����¶ȵ����߶��������������ƣ�BΪ�����ڷǽ������ʣ�D��Ư�۵ijɷ�֮һ���������ƺ�������Ӧ�����Ȼ��ơ�������ƺ�ˮ������B��������C�ܷ���ˮ�ⷴӦ������C�Ǵ�����ƣ�D���Ȼ��ƣ������������ˮ�ⷽ��ʽΪ��ClO-+H2O?HClO+OH-��
�ʴ�Ϊ��ClO-+H2O?HClO+OH-��
��4����AΪ���10���ӵ��������뵥��18���ӵ������ӹ��ɵ���ɫ���壬���10���ӵ���������笠����ӣ������ֽ⣬�ֽ���������ּ�������ˮ�����壬��A���Ȼ�泥�����18���ӵ��������������ӣ������ӵļ��鷽���ǣ�ȡ����A��һ�ྻ�Թ��У�������ˮ�ܽ�μ���������Һ��������ɫû�����ٵμ�ϡ���ᣬ���������ܽ⣬��A��������ΪCl-��
�ʴ�Ϊ��ȡ����A��һ�ྻ�Թ��У�������ˮ�ܽ�μ���������Һ��������ɫû�����ٵμ�ϡ���ᣬ���������ܽ⣬��A��������ΪCl-��
���������
�����Ѷȣ�һ��
4������� ��5.6g������������ϡ�����г�ַ�Ӧ���õ�80mL�ܶ�Ϊ1.25g/mL����Һ���Լ��㣺
��1�����ɱ�״���µ�H2��������
��2��������Һ���������������ʵ���Ũ�ȣ�
�ο��𰸣���1������������5.6g����ȫ��Ӧ�����������ɱ�״���µ�H2�����ΪV����
Fe+H2SO4=FeSO4+H2
56g?22.4L
5.6g? V
����V=5.6g56g��22.4L=2.24L��
��5.6g����ȫ��Ӧ���ɱ�״����H2�����Ϊ2.24L��
��2��5.6g����ȫ��Ӧ��������Ԫ���غ��֪����Һ��n��FeSO4��=n��Fe��=5.6g56g/mol=0.1mol����Һ��c��FeSO4��=0.1mol0.08L=1.25mol/L��
����Һ���������������ʵ���Ũ��Ϊ1.25mol/L��
���������
�����Ѷȣ�һ��
5��ѡ���� ���е���ʽ�У���ȷ����

�ο��𰸣�C
���������A�������ӵ���ʽ����ȷ��Ӧ����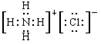 ��B��NH4������ʽ����ȷ��Ӧ����
��B��NH4������ʽ����ȷ��Ӧ����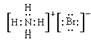 ��D��Ҳ�������ӵ���ʽ����ȷ��Ӧ����
��D��Ҳ�������ӵ���ʽ����ȷ��Ӧ����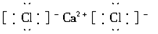 ��������ȷ�Ĵ�ѡC��
��������ȷ�Ĵ�ѡC��
�����Ѷȣ���