微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式书写正确的是
A.用醋酸溶液除去水垢中的CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑
B.碘水中通入足量的SO2气体:I2+SO2+2H2O═2I-+SO+4H+
C.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO+3Cl-+H2O+4H+
参考答案:B
本题解析:分析:A.醋酸为弱酸,在离子反应中应保留化学式;
B.发生氧化还原反应生成HI和硫酸;
C.至中性,二者以2:1反应,反应生成硫酸钡、硫酸钠、水;
D.强碱溶液不会存在大量的H+.
解答:A.用醋酸溶液除去水垢中的CaCO3的离子反应为CaCO3+2HAc═Ca2++H2O+CO2↑+2Ac-,故A错误;
B.碘水中通入足量的SO2气体的离子反应为I2+SO2+2H2O═2I-+SO42-+4H+,故B正确;
C.NaHSO4溶液与Ba(OH)2溶液反应至中性的离子反应为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子反应为4OH-+3ClO-+2Fe(OH)3═2FeO42-+3Cl-+5H2O,故D错误;
故选B.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答的关键,注意选项D中碱性溶液中及发生的氧化还原为解答的难点,题目难度中等.
本题难度:简单
2、选择题 能用“ Ba2+ + SO42-= BaSO4↓ ”表示的反应是
A.H2SO4与Ba(OH)2反应
B.K2SO4与Ba(OH)2反应
C.CuSO4与Ba(OH)2反应
D.H2SO4与BaCO3反应
参考答案:B
本题解析:试题分析:A、H2SO4与Ba(OH)2反应的离子方程式为Ba2++2OH-+2H++SO42-═2H20+BaSO4↓,错误;B、K2SO4与Ba(OH)2反应的离子方程式为Ba2++SO42-═BaSO4↓,正确;C、CuSO4与Ba(OH)2反应的离子方程式为Ba2++2OH-+Cu2++SO42-═Cu(OH)2↓+BaSO4↓,错误;D、H2SO4与BaCO3反应,碳酸钡是难溶于水的盐,该反应不能用Ba2++SO42-═BaSO4↓表示,错误。
考点:考查离子方程式的意义和书写。
本题难度:困难
3、选择题 KCl、KBr的混合物3.87g溶于水中,加入过量的AgNO3溶液,充分反应后,得到沉淀6.63g,则原混合物中钾元素的质量分数为
A.0.241
B.0.259
C.0.403
D.0.487
参考答案:C
本题解析:分析:发生反应KCl、KBr转化为AgCl、AgBr,由于银离子代替钾离子导致质量增大,由电荷守恒可知n(K+)=n(Ag+),结合质量差计算n(K+),再根据m=nM计算m(K+),再根据质量分数的定义计算.
解答:发生反应KCl、KBr转化为AgCl、AgBr,由于银离子代替钾离子导致质量增大,由电荷守恒可知n(K+)=n(Ag+),则108g/mol×n(K+)-39g/mol×n(K+)=6.63g-3.87g,解得n(K+)=0.04mol,
故原混合物中钾元素的质量分数=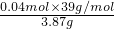 ×100%=40.3%,
×100%=40.3%,
故选C.
点评:本题考查混合物的有关计算,难度中等,注意根据反应分析质量变化的原因,注意电荷守恒利用判断n(K+)=n(Ag+)是解题的关键,比较过程法更简单.
本题难度:简单
4、选择题 过氧化钠与CO2作用,反应的化学方程式为2Na2O2+2CO2═2Na2CO3+O2.当0.2mol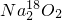 与足量CO2完全反应后,如表所示对生成物Na2CO3和O2的描述中正确的是
与足量CO2完全反应后,如表所示对生成物Na2CO3和O2的描述中正确的是
A.A
B.B
C.C
D.D
参考答案:B
本题解析:分析:Na218O2与CO2的反应实质是-1价的氧发生歧化反应,发生2Na218O2+2CO2═2Na2CO3+18O2,以此解答该题.
解答:Na218O2与CO2的反应实质是-1价的氧发生歧化反应,发生2Na218O2+2CO2═2Na2CO3+18O2,其中生成物Na2CO3中有1个18O为,摩尔质量为108g/mol,氧气为18O2,摩尔质量是36g?mol-1,则当0.2molNa218O2与足量CO2完全反应后,生成Na2CO3的质量为21.6g,生成标准状况下O2的体积为2.24L,
故选B.
点评:本题考查钠的重要化合物,题目难度不大,注意把握反应的原理,为解答该题的关键.
本题难度:简单
5、选择题 已知?Cl2+H2O=HCl+HClO,新制的氯水具有漂白性,其中起漂白作用的物质是
A.Cl2
B.H2O
C.HCl
D.HClO
参考答案:D
本题解析:分析:新制的氯水中含有次氯酸,具有漂白作用.
解答:新制的氯水中含有次氯酸,具有漂白作用,
故选D.
点评:本题主要考查了次氯酸的性质,需要注意的是Cl2无漂白性.
本题难度:简单