��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��12�֣�ij�ֳ����İ�ɫ����A�������ᷴӦ�����̼�����ζ������B����Bͨ�����ʯ��ˮ��ʯ��ˮ����ǡ�����A��ˮ��Һ�м�����������Һ�ȣ���������ɫ����C����ɫ����D��D����ʹʪ��ĺ�ɫʯ����ֽ���������ȹ���A��������ˮ��B��D������B��D�����ʵ���֮��Ϊ1:1������������ʵ�������жϳ�A��?��B��?��C��?��
���ȹ���A����ˮ��B��D�Ļ�ѧ����ʽ��_____________?��
A�����ᷴӦ�����ӷ���ʽ___________________________________��
A������������Һ��Ӧ�����ӷ���ʽ_______________________________________________��
�ο��𰸣�NH4HCO3? CO2? BaCO3? NH4HCO3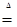 H2O + CO2�� + NH3��? HCO3- + H+ = CO2 +H2O?
H2O + CO2�� + NH3��? HCO3- + H+ = CO2 +H2O?
NH4+ + HCO3- + Ba2+ ?+ 2OH- = BaCO3��+ NH3��+ 2H2O
�����������
�����Ѷȣ�һ��
2������� ��8�֣�
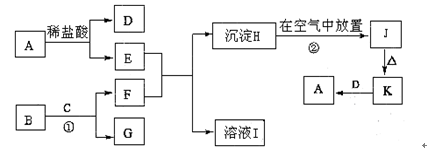
����ΪһЩ�������ʵ��ת����ϵͼ����֪��A�����������г��õ�һ�ֽ������ʣ�BΪ����ɫ��ĩ��C�ڳ�����Ϊ��ɫҺ�壬HΪ��ɫ������JΪ���ɫ����
�����
(1) A��B�Ļ�ѧʽΪ��A?��B?��
(2)���̢��еķ�Ӧ����?��
(3)��Ӧ�ٵĻ�ѧ����ʽ?��
�ο��𰸣�(1)Fe? Na2O2?(2)���ɵİ�ɫ����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ
(3)2Na2O2��2H2O��4NaOH��O2
�����������
�����Ѷȣ�һ��
3������� A��H�Լ�X��Y��ת����ϵ��ͼ��
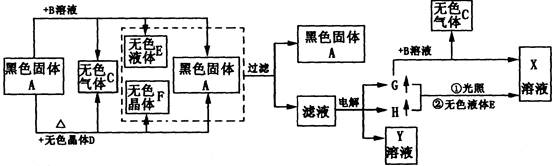
��1�����������Һʱ����G�ĵ缫��?����缫��ӦʽΪ?��
��2��ȡ��ͼ����Һ����ɫ��Ӧ����ɫ����ͼ����ɫ��Ӧ����ɫ�Ļ���?��
��3��д����ɫ������XŨ��Һ���ȷ�Ӧ�����ӷ���ʽ?��
��4��д��G��B��Һ��Ӧ�Ļ�����ʽ?��
�ο��𰸣�
��1����? 2C1--2e- = Cl2����2�� D��Y��F����KC1O3��KOH��KCl��ע������F��KCl���۷֣���3��MnO2+4H++2C1- Mn2++C12��+2H2O?
Mn2++C12��+2H2O?
��4��C12+H2O2��2HC1+O2
���������
����Ϊ���ƶ��⡣����ؼ��Ǻ�ɫ����A���Ƶ����ӿ�ͼ��֪����ɫ����A��B��Һ����ɫ����D�ķ�Ӧ�У����յIJ�������Ȼ��A���ʣ���֪����������Ӧ��AΪ�������²�ΪMnO2����ɫ����DΪKClO3��������Ӧ2KClO3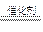 2KCl��3O2��������CΪ������B��Һ�ڴ��������¿���������������BΪH2O2����ӦΪ2H2O2
2KCl��3O2��������CΪ������B��Һ�ڴ��������¿���������������BΪH2O2����ӦΪ2H2O2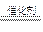 2H2O��O2����������ɫҺ��EΪˮ����ɫ����FΪKCl�����˺���ҺΪKCl��Һ���������Ϊ��KOH��H2��Cl2��Y��KOH��Һ��G�ܹ���H2O2��Ӧ����G��Cl2����ӦΪC12+H2O2��2HC1+O2��H��H2��G��H���պ�IJ���ΪHCl������ˮ�õ����ᣬX�����ᡣ
2H2O��O2����������ɫҺ��EΪˮ����ɫ����FΪKCl�����˺���ҺΪKCl��Һ���������Ϊ��KOH��H2��Cl2��Y��KOH��Һ��G�ܹ���H2O2��Ӧ����G��Cl2����ӦΪC12+H2O2��2HC1+O2��H��H2��G��H���պ�IJ���ΪHCl������ˮ�õ����ᣬX�����ᡣ
�����Ѷȣ�һ��
4������� ��14�֣���ͼ��ʾ���ʣ����ֲ���ͷ�Ӧ����δ������У�ֻ��A�ǵ��ʣ�������B�� C����̬����B�ǵ�������Ĵ�����Ⱦ�W�ǵ���ɫ���塣
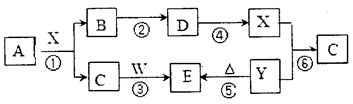
�ݴ˻ش��������⣺
��1������W�������еĻ�ѧ������Ϊ_________�������������Ӹ�����Ϊ_________��
��2������C�ĽṹʽΪ____________��
��3����ͼ��Ӧ�в�����������ԭ��Ӧ����______________����д��ţ���
��4��д��A��X��Ӧ�Ļ�ѧ����ʽ_____________�������ɵ�B�ڱ�״���µ����Ϊ? 22��4L����Ӧ��ת�Ƶ�����ĿΪ_____________��
��5����д��C��W��Ӧ�Ļ�ѧ����ʽ��_______________��
��6����д��X��Y��Ӧ�����ӷ���ʽ��_________________��
�ο��𰸣���1�����Ӽ����ۼ���1�֣�? 1�U2?��1�֣�
��2��? O=C=O?��2�֣�
��3���ܢݢޣ�2�֣�
��4��C+2H2SO4��Ũ�� CO2��+2SO2��+2H2O��2�֣���? 1.204��1024��2�֣�
CO2��+2SO2��+2H2O��2�֣���? 1.204��1024��2�֣�
��5��2Na2O2+2CO2=2Na2CO3+O2��2�֣�
��6��H++HCO3-��CO2��+H2O��2�֣�
���������B�ǵ�������Ĵ�����Ⱦ�W�ǵ���ɫ���壬����B�Ƕ�������W�ǹ������ơ�C����̬������������Ʒ�Ӧ�����C�Ƕ�����̼��E��̼���ơ�Y�ֽ�����̼���ƣ�����Y��̼�����ơ�X��̼�����Ʒ�Ӧ���ɶ�����̼������X���ᣬ��������ᣬ��D��������������ˮ���õ����ᡣ�ڼ���ʱ̼��Ũ���ᷴӦ�����ɶ�����̼�Ͷ�������
�����Ѷȣ�һ��
5������� ��֪A��B��C����ѧ��ѧ�ij������ʣ�������һ��������������ת����ϵ��
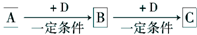
��1����A��ʹʪ��ĺ�ɫʯ����ֽ������CΪ����ɫ���壮��Aת��ΪB��Ӧ�Ļ�ѧ����ʽΪ______��
��2����D�Ǿ��������Եĵ��ʣ�AԪ��Ϊ�������ڵĽ���Ԫ�أ���C�ĵ���ʽΪ______��
��3����D�������г����Ĺ��ɽ�����A�ǻ���ɫ���壬��B��C�����ӷ���ʽΪ______��
��4����D��һ�ֳ������������壻A��һ��ǿ���������ˮ��Һ�е���������������Ӿ�����10�����ӣ���Bת��ΪC�����ӷ���ʽΪ______��
��5����AΪ����л��D�Ǿ��������Եĵ��ʣ�25�桢101kPaʱ��3.2g?A��ȫȼ�������ȶ���������ʱ�ų�178kJ����������д����ʾ����A��ȼ���ȵ��Ȼ�ѧ����ʽ______��
��6����A���������Ϊ75%����Һ������ҽ����������B������������ͭ���ȣ��к�ɫ�������ɣ���A����B�Ļ�ѧ����Ϊ______��
�ο��𰸣�A��D��Ӧ����B��B��D��Ӧ����C����B��C�к��е�ij�ֹ�ͬԪ���DZ��Ԫ�أ�
��1����A��ʹʪ��ĺ�ɫʯ����ֽ��������A�ǰ�����CΪ����ɫ�������������������D�ܷ�Ӧ����B����B��һ��������D��������Aת��ΪB�ķ�Ӧ����ʽΪ4NH3+5O2����.��4NO+6H2O��
�ʴ�Ϊ��4NH3+5O2����.��4NO+6H2O��
��2����D�Ǿ��������Եĵ��ʣ�AԪ��Ϊ�������ڵĽ���Ԫ�أ����ݷ�Ӧ·��֪��B��C�ж�����AԪ�أ��������ڽ���Ԫ��û�б�ۣ����ƺ�������Ӧ���������б�ۣ�����A���ƣ�D��������B�������ƣ�C�ǹ������ƣ��������������ӻ���������ʽΪ
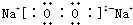
���ʴ�Ϊ��
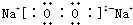
��
��3����D�������г����Ĺ��ɽ�����������A�ǻ���ɫ���壬������������������Ӧ�����Ȼ���B���Ȼ���������Ӧ�����Ȼ�����C�������Ӻ�����Ӧ�����������ӣ����ӷ�Ӧ����ʽΪ2Fe3++Fe=3Fe2+��
�ʴ�Ϊ��2Fe3++Fe=3Fe2+��
��4����D��һ�ֳ������������壬��D�Ƕ�����̼��A��һ��ǿ���������ˮ��Һ�е���������������Ӿ�����10�����ӣ���A���������ƣ�����������̼���������Ʒ�Ӧ����̼���ƺ�ˮ��������̼��̼���ơ�ˮ��Ӧ����̼�����ƣ���B��̼���ƣ�C��̼�����ƣ�̼������ӺͶ�����̼��ˮ��Ӧ����̼��������ӣ����ӷ�Ӧ����ʽΪ��CO32-+CO2+H2O=HCO3-��
�ʴ�ΪCO32-+CO2+H2O=HCO3-��
��5����AΪ����л����A�Ǽ��飬D�Ǿ��������Եĵ��ʣ�D�����������������������Ӧ����һ����̼��ˮ��һ����̼��������Ӧ���ɶ�������25�桢101kPaʱ��3.2g?A�����ʵ�����0.2mol��3.2g?A��ȫȼ�������ȶ���������ʱ�ų�178kJ����������1molA��ȫȼ�������ȶ�������ʱ�ų�890kJ�������������Ȼ�ѧ��Ӧ����ʽΪ��CH4��g��+2O2��g��=CO2��g��+2H2O��l ����H=-890kJ/mol��
�ʴ�Ϊ��CH4��g��+2O2��g��=CO2��g��+2H2O��l ����H=-890kJ/mol��
��6����A���������Ϊ75%����Һ������ҽ������������A���Ҵ���B������������ͭ���ȣ��к�ɫ�������ɣ���B��ȩ����ΪA��D��Ӧ����B������A��B����̼ԭ������ͬ����B����ȩ����ȩ������������������C��ͭ�����������������£��Ҵ�����������������ȩ����Ӧ����ʽΪ��2CH3CH2OH+O2Cu
���������
�����Ѷȣ�һ��