微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 图中的每一个方格表示有关的一种反应物或生成物,其中A、C为无色气体.
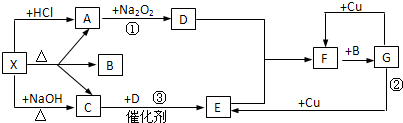
请回答:
(1)物质X可以是______,C是______,F是______.
(2)反应①的化学方程式是______.
(3)反应③的化学方程式是______.
(4)反应②的离子方程式是______.
参考答案:X和NaOH反应生成无色气体C,推知C为NH3,X是铵盐;X和盐酸反应生成无色气体A,A和Na2O2反应生成D,推知A为CO2,D为O2,进而推出E为NO,F为NO2,G为HNO3,浓度不同时,能和铜反应生成不同的气体,则X可能是
NH4HCO3或(NH4)2CO3,则
(1)由以上分析可知,X可能是NH4HCO3或(NH4)2CO3,C为NH3,F为NO2,
故答案为:(NH4)2CO3或NH4HCO3;NH3;N02;
(2)反应①为CO2和Na2O2的反应,二者反应生成碳酸钠和氧气,反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2,
故答案为:2CO2+2Na2O2=2Na2CO3+O2;
(3)反应③为氨气的催化氧化,为工业制硝酸的反应,化学方程式为4NH3+5O2催化剂.高温高压4NO↑+6H2O,
故答案为:4NH3+5O2催化剂.高温高压4NO↑+6H2O;
(4)反应②为稀硝酸与铜的反应,生成NO,反应的离子的方程式为3Cu+8H++2N03-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2N03-=3Cu2++2NO↑+4H2O.
本题解析:
本题难度:一般
2、填空题 已知常温下B、D、E、L为密度比空气大的气体,D、E为单质,其他为化合物。A是一种淡黄色固体,C微溶于水,F、G均能与L的水溶液反应放出B。据下边反应框图填空。
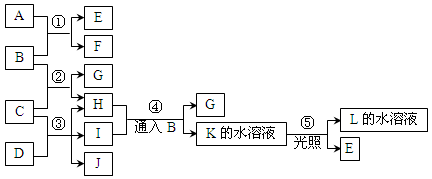
(1)F的俗名是?,B分子的结构式为________工业上利用反应③生产?。
(2)反应④的离子方程式为?。
(3)有一种单质能与H反应生成E,该反应的化学方程式为?。
(4)某气体M具有漂白作用,既有氧化性,又有还原性,M通入D的溶液中反应的离子方程式为?。
参考答案:(1)纯碱或苏打(1分),O=C=O?(1分)漂白粉(1分)
(2)Ca2++2ClO-+CO2+H2O=CaCO3+2HClO(2分)
(3)2F2+2H2O=4HF+O2(2分)
(4)SO2+Cl2+2H2O=SO42-+2Cl-+4H+(2分)
本题解析:A是一种淡黄色固体,且A是化合物,所以A是过氧化钠。A和B反应生成E和F,其中B、D、E、L为密度比空气大的气体,D、E为单质,所以B是CO2,E是氧气,F是碳酸钠。C微溶于水,F、G均能与L的水溶液反应放出B,这说明L应该是酸,因此L是氯化氢。C是氢氧化钙,氢氧化钙和CO2反应生成碳酸钙和水,即H是水。将CO2通入到I的水溶液中生成碳酸钙和K,K光照生成氯化氢和氧气,这说明K是次氯酸,所以I是次氯酸钙,J是氯化钙,D是氯气。
(1)碳酸钠的俗名是纯碱或苏大,CO2分子中含有碳氧双键,其结构式为O=C=O ,氯气与氢氧化钙反应可以制备漂白粉,所以工业上利用反应③生产漂白粉。
(2)碳酸的酸性强于次氯酸,因此CO2通入到次氯酸钙溶液中生成次氯酸,所以反应④的离子方程式为Ca2++2ClO-+CO2+H2O=CaCO3+2HClO。
(3)能和水反应生成氧气的单质可以是单质氟,反应的化学方程式为2F2+2H2O=4HF+O2。
(4)M具有漂白作用,既有氧化性,又有还原性,所以M是SO2,与氯气在水溶液中反应的离子方程式为SO2+Cl2+2H2O=SO42-+2Cl-+4H+。
本题难度:一般
3、简答题 有A、B、C、D、E和F六瓶无色溶液,他们是中学化学中常用的无机试剂.纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同.现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶.
根据上述实验信息,请回答下列问题:
(1)能确定溶液是(写出溶液标号与相应溶质的化学式):______
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:______.
参考答案:(1)①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾,说明A为NH3?H2O或NH3;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,可能为Al(OH)3或Mg(OH)2,F中沉淀完全溶解,则F为AgNO3;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出,该气体为CO2,说明E为酸溶液,且纯E为无色油状液体,说明E为H2SO4,B可能为Na2CO3或K2CO3;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶,则该沉淀可能为BaSO4或AgCl,则C应为BaCl2,.
根据B、C、D和F是盐溶液,且他们的阴离子均不同,D可能为Al2(SO4)3或MgSO4,
所以,能确定的是A:NH3?H2O或NH3;E:H2SO4;?F:AgNO3;?C:BaCl2,
故答案为:A:NH3?H2O或NH3;E:H2SO4;?F:AgNO3;?C:BaCl2;
(2)不能确定的是D可能为Al2(SO4)3或MgSO4,B可能为Na2CO3或K2CO3,
检验方法是:用洁净的铂丝蘸取少量B,在酒精灯火焰中灼烧,若焰色呈黄色则B为Na2CO3溶液;若透过蓝色钴玻璃观察焰色呈紫色,则B为K2CO3溶液;取少量D,向其中滴加NaOH溶液有沉淀生成,继续滴加过量的NaOH溶液,若沉淀溶解,则D为Al2(SO4)3溶液,若沉淀不溶解,则D为MgSO4溶液.
故答案为:B:Na2CO3或K2CO3,用洁净的铂丝蘸取少量B,在酒精灯火焰中灼烧,若焰色呈黄色则B为Na2CO3溶液;若透过蓝色钴玻璃观察焰色呈紫色,则B为K2CO3溶液;
D:Al2(SO4)3或MgSO4取少量D,向其中滴加NaOH溶液有沉淀生成,继续滴加过量的NaOH溶液,若沉淀溶解,则D为Al2(SO4)3溶液,若沉淀不溶解,则D为MgSO4溶液.
本题解析:
本题难度:一般
4、推断题 某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。

填写下面空白:
(1)图中标号处需加入的相应物质分别是①_______、②_______、③_______、④_______、⑤_______。
(2)写出①处发生反应的离子方程式__________________;_________________;__________________;
___________________;写出③处发生反应的化学方程式________________________。
(3)铁红的化学式为________;分别写出铁红和氧化铜在工业上的一种主要用途:
铁红____________________;氧化铜______________________。
参考答案:(1)①铁屑;②稀硫酸;③稀硝酸;④氢氧化钠;⑤氢氧化钠
(2)Fe+2H+==Fe2++H2↑;2Fe3++Fe==3Fe2+;Cu2++Fe===Cu+Fe2+;2Au3++3Fe==2Au+3Fe2+;
3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
(3)Fe2O3;用作红色颜料;用作制造铜盐的原料
本题解析:
本题难度:一般
5、选择题 代号为X、Y、Z的三种化合物,在某条件下均能分解,各产生两种产物,而其中有一物质是相同的,如式中的W,反应式如下(反应条件未注明):
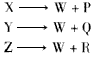
已知:(1)P为一种盐,其水溶液与AgNO3( aq)反应,产生白色沉淀。
(2)Q为只由一种元素构成的可燃气体。
(3)元素R在常温常压为液体,能从AgNO3( aq)中,置换出Ag(s)。试依据上列反应式,推论下列哪些叙述正确
?[? ]
A.P是AgCl(s)
B.Q是O2(g)
C.R是Hg (1)
D.Y是H2O (1)
E.Z是KBr(s)
参考答案:CD
本题解析:
本题难度:一般
|