微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10)[物质结构].甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学程式是?___________________________________
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:___________________________________
(3)在一定条件下,甲与O2反应的化学方程式是?_______________________
(4)丁的元素符号是_________,它的核外电子排布式为?_______________________
(5)丁的氧化物的晶体结构与_________________?的晶体结构相似。
参考答案:(10分)(1)CaC2+2H2O―→C2H2↑+Ca(OH)2(2分)
(2)例如:3CO+Fe2O3 2Fe+3CO2,(2分)工业上利用该反应进行炼铁。(1分)(其他合理答案也可以)
2Fe+3CO2,(2分)工业上利用该反应进行炼铁。(1分)(其他合理答案也可以)
(3)N2+O2 2NO (2分) (4)Si? 1s22s22p63s23p2?(2分)(5)金刚石(1分)
2NO (2分) (4)Si? 1s22s22p63s23p2?(2分)(5)金刚石(1分)
本题解析:略
本题难度:一般
2、填空题 浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种。
(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为:?。
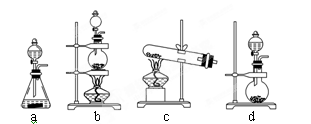
(2)实验室用二氧化锰制取氯气的化学方程式为:?;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气?(填写装置的序号)。
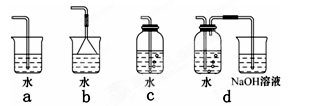
(3)实验室中模拟Br―→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现。写出Br―→Br2的转化离子方程式为:?;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是?(选填下列选项的编号字母)。
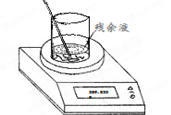
(4)实验室制备氯气的反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100 mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如右图),再把已称好50.0 g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应。观察读数变化如下表所示:
CaCO3用量
| 未加CaCO3时
| 加约四分之一时
| 加一半时
| 全部加完时
|
读数/g
| 318.3
| 325.3
| 334.5
| 359.5
|
请你据此分析计算:
①实验中产生的CO2气体质量为?;
②残余液中盐酸的物质的量浓度为 (结果精确到小数点后一位)?。
参考答案:(1)2NaCl+2H2O 2NaOH+H2↑+Cl2↑(2分)
2NaOH+H2↑+Cl2↑(2分)
(2)MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑(2分);b(1分)
MnCl2+2H2O+Cl2↑(2分);b(1分)
(3)2Br-+Cl2=2Cl-+Br2(2分);d(1分) (4)①8.8g(2分);②4.0mol/L(3分)
本题解析:(1)“氯碱工业”是以食盐水为原料,通过电解法制取Cl2等物质,有关的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(2)实验室用二氧化锰制取氯气的化学方程式为MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑。根据方程式可知该反应是固体与液体加热制备气体,因此需要的主要仪器是酒精灯、分液漏斗、烧瓶,则实验装置应该是装置b,即答案选b。
MnCl2+2H2O+Cl2↑。根据方程式可知该反应是固体与液体加热制备气体,因此需要的主要仪器是酒精灯、分液漏斗、烧瓶,则实验装置应该是装置b,即答案选b。
(3)氯气的氧化性强于单质溴的,能把溴离子氧化生成单质溴,所以Br―→Br2的转化离子方程式为2Br-+Cl2=2Cl-+Br2。氯气能溶于水,但溶解度很小。另外氯气有毒,需要尾气处理,可以用氢氧化钠溶液吸收,因此正确的答案选d。
(4)①根据质量守恒定律可知,反应中产生CO2的质量=318.3g+50.0g-359.5g=8.8g。
②CO2的物质的量=8.8g÷44g/mol=0.2mol,则根据方程式可知
CaCO3+2HCl=CaCl2+H2O+CO2↑
2mol? 1mol
0.4mol? 0.2mol
所以盐酸的浓度=0.4mol÷0.1L=4.0mol/L
本题难度:一般
3、选择题 氯气溶于水发生反应:Cl2 + H2O  ?HCl + HClO 。氯水中起杀菌消毒作用的是
?HCl + HClO 。氯水中起杀菌消毒作用的是
A.Cl2
B.HCl
C.HClO
D.H2O
参考答案:C
本题解析:HClO起杀菌消毒的作用,是利用了HClO的强氧化性;
本题难度:简单
4、选择题 将20 mL 10 mol・L-1的浓盐酸滴入盛有足量MnO2粉末的烧瓶中并加热,若不考虑HCl的挥发,则被氧化的氯化氢的物质的量是(? )
A.小于0.1 mol
B.等于0.1 mol
C.大于0.1 mol,小于0.2 mol
D.等于0.2 mol
参考答案:A
本题解析:随反应进行,盐酸变稀,稀到一定浓度时,反应停止,即0.2 mol HCl不可能完全反应。
本题难度:简单
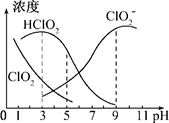
5、选择题 印染工业常用亚氯酸钠(NaClO2)漂白织物.亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2―,其中HClO2是漂白剂的有效成分,ClO2是有毒气体.各组分含量随pH变化情况如图所示,由图可知,使用该漂白剂的最佳pH为( )。
A.3.0
B.4.0~4.5
C.6.5~7.0
D.9.0
参考答案:B
本题解析:HClO2是漂白剂的有效成分,ClO2是有毒气体,所以根据图像可知,使用该漂白剂的最佳pH为4.0~4.5,答案选B。
本题难度:一般