微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)①下图1是N2(g)和O2(g)反应生成NO(g)过程中的能量变化示意图,则该反应的热化学方程式为__________________。
②根据下图2分析,若0.5 mol CO被氧化,则该过程放出_________kJ的热量。
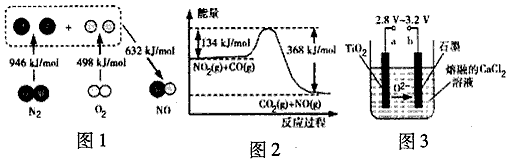
(2)TiO2可由钛铁矿经过下列流程处理得到,溶液2中含有Fe2+、TiO2+和少量Mg2+等阳离子。

①溶液2加水稀释,可使TiO2+水解生成白色沉淀TiO(OH)2,原因是_______________。
②工业上在800℃~1 000℃下,电解TiO2可制得海绵钛,其装置示意图如上图3。写出其阴极的电极反应式:_____________________。
2、填空题 纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,常用的制备方法有电化学法、湿化学法等。电化学法可用铜棒和石墨作电极,电解Cu(NO3)2稀溶液制备。湿化学法的制备过程为:在KOH溶液中加入一定量的CuSO4溶液,再加入一定量的还原剂--肼(N2H4),加热并保持温度在90℃。检验反应完全后,分离、洗涤、真空干燥得到固体样品。反应方程式为:
4CuSO4?+?N2H4?+?8KOH?=?2Cu2O?+?N2↑+?4K2SO4?+?6H2O
⑴电化学法制备Cu2O时,铜棒做________极,阴极生成Cu2O的电极反应式为______________________。
⑵湿化学法中,检验纳米Cu2O已经生成的实验方法是_____________________。
⑶湿化学法得到的产品中常含有Cu。称取某产品1.76?g(设仅含Cu2O和Cu),加入足量的稀硝酸,充分反应后得到标准状况下的NO气体224mL,计算产品中Cu2O的质量分数。(写出计算过程)
3、填空题 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。已知:
CH4(g)+ H2O(g)==== CO(g)+3H2(g) △H =206.2kJ・mol-1
CH4(g)+ CO2(g)==== 2CO(g)+2H2(g)△H =247.4kJ・mol-1
2H2S(g)====2H2(g)+S2(g) △H =169.8kJ・mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_____________________。
(2)H2S热分解制氢时,常向反应器中通入一定比例空气,使部分H2S燃烧,其目的是__________________________;燃烧生成的SO2与H2S进一步反应,生成物在常温下均非气体,写出该反应的化学方程式:
_____________________。
(3)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是______________。
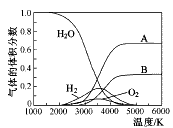
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见下图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为__________________。
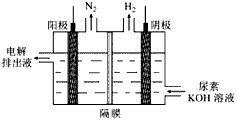
(5)Mg2Cu是一种储氢合金。350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077)。Mg2Cu与H2反应的化学方程式为______________________。
4、填空题 钛(Ti)被称为继铁、铝之后的第三金属,钝钛和以钛为主的合金是新型的结构材料,主要用于航天工业和航海工业,下列是有关钛的冶炼及应用的问题。
(1)金属钛冶炼过程中其中一步反应是将原料金红石转化:
TiO2(金红石)+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
已知:C(S)+O2(g)=CO2(g)? ?H=-393.5?kJ・mol-1
?H=-393.5?kJ・mol-1
2CO(g)+O2(g)=2CO2(g)? H=-566?kJ・mol-1
H=-566?kJ・mol-1
TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)? H=+141?kJ・mol-1
H=+141?kJ・mol-1
则TiO2(g)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的 ?H=______________,
?H=______________,
(2)钠热还原法是冶炼金属钛的方法之一,主要反应原理为:4Na+TiCl4 4NaCl+Ti,该反应不能在水溶液中进行,一是因为TiCl4会强烈水解生成TiO2,另一原因_______________(用适当化学方程式辅以必要的文字说明)。
4NaCl+Ti,该反应不能在水溶液中进行,一是因为TiCl4会强烈水解生成TiO2,另一原因_______________(用适当化学方程式辅以必要的文字说明)。
(3)镁还原法也是冶炼金属钛的常用方法,其主要反应原理如下: ?
MgCl2 Mg+Cl2?TiCl4+2Mg
Mg+Cl2?TiCl4+2Mg 2MgCl2+Ti
2MgCl2+Ti
从海水中提取MgCl2时,先在海水中加入熟石灰,沉淀出Mg(OH)2,写出Mg(OH)2溶度积表达式:_______________可加入适当过量的熟石灰,从Mg(OH)2溶解平衡角度解释其原因_________________
(4)TiCl4与LiOH在水溶液中一定条件下可反应生成Li4Ti5O12(钛酸锂),Li4Ti5O12可与LiMn2O4(锰酸锂)等正极材料组成理离子二次电池,工作时Li+?在电池内定向移动,其电池反应为: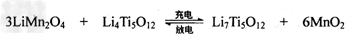 使用时先充电,写出其充电式的阳极反应_______________,放电时Li+的移动方向?_______________。
使用时先充电,写出其充电式的阳极反应_______________,放电时Li+的移动方向?_______________。
5、填空题 开发具有广谱、高效、低毒的杀菌、消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 molO3转化为1 molO2和1mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是 ____。(填序号)
A.Cl2
B.H2O2
C.ClO2
D.O3
(2)氯氨(NH2Cl)可作为杀菌剂,请用化学方程式表示氯氨在水中的杀菌机理:___
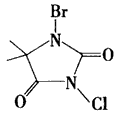
(3)氯溴海因(C5H6 BrClN2O2)是一种比较安全的氯气和氯制剂的替代产品,其结构式如下图所示: 氯溴海因在水中的水解过程比较复杂,主要是水解生成次卤酸和海因,请画出海因的结构式:___。?
(4)以铂(Pt)和铁为电极,以KOH溶液为电解液,用电解法可制备高铁酸钾 (K2FeO4)。写出阳极的电极反应式:____。