��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1���ƶ��� ��ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯�����ת����ϵͼ���йط�Ӧ�����������ɵ�H2O����ȥ����
��֪����a��A��B��C��D�Ƿǽ������ʣ�����B��C��D�ڳ��³�ѹ�������塣
��b����Ӧ�١����ǻ��������е���Ҫ��Ӧ��
��c��������E���γ��������Ⱦ��֮һ��������K�dz��õĵ��ʡ�
��d��������L����Ư���ԣ�����Cl2��NaOH��Һ��Ӧ���Ƶá�
��e��������J������Ԫ����ɣ�����Է�������Ϊ32��
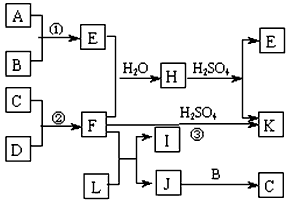
�밴Ҫ����գ�
��1����Ӧ�۵Ļ�ѧ����ʽ_________________��
��2��C�Ľṹʽ___________��H�Ļ�ѧʽ___________��
��3��L����Һ�뻯����E��Ӧ�����ӷ���ʽ_________________��
��4��������J�Ļ�ѧʽ_________________��
�ο��𰸣���1��2NH3+H2SO4==(NH4)2SO4
��2��N��N��(NH4)2SO3��NH4HSO3
��3��ClO-+SO2+2OH-==Cl-+SO42-+H2O
��4��N2H4
���������
�����Ѷȣ�һ��
2������� ��12�֣����ݷ�Ӧ��ͼ��գ���֪��Ӧ�١��ݾ�Ϊ��ҵ������Ӧ���г�����Ӧ�����У¡��ǡ��ɡ��ʡ��̾�Ϊ�������ʣ��¡�D���ʡ���Ϊ���塣���ǹ�ҵ����F����Ҫ��ʯԭ�ϵ���Ҫ�ɷݣ�����Է�������Ϊ120��
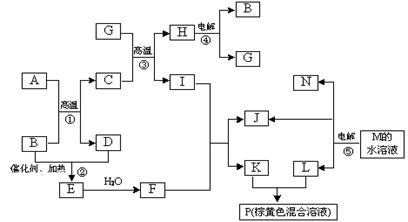
��1��IԪ����Ԫ�����ڱ��е�λ��_?______��M�������ӵĽṹʾ��ͼ��?��
��2������A���������Ļ�ѧ�������Na2O2���ƣ���A�ĵ���ʽΪ?��
��3��д����Ӧ����ʹ���豸������___________________��
��4��д�����л�ѧ��Ӧ�����ӷ���ʽ��
�� ��Ӧ�ݣ�______________________________________________?___��
�� G��N�ķ�Ӧ��________________________________________________��
�� K��L�ķ�Ӧ��________________________________________________��
��5����֪ÿ����16 gD���ų�106��5 kJ��������Ӧ�� ���Ȼ�ѧ����ʽΪ��
���Ȼ�ѧ����ʽΪ��
?��
�ο��𰸣���1���������ڵڢ���?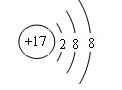 ?
?
��2��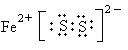
��3������¯
��4��2Cl��+ 2H2O �� Cl2�� + H2�� + 2OH��
2Al +2OH��+2H2O =  2AlO2��+3H2��?
2AlO2��+3H2��?
2Fe2+ +Cl2=2Fe3+ + 2Cl��
��5��4FeS2��s����11O2��g���� 2Fe2O3��s����8SO2��g������H=��3408kJ/mol
�����������
�����Ѷȣ���
3���ƶ��� A-I�ֱ��ʾ��ѧ��ѧ�г�����һ�����ʣ�����֮�����ϵ����ͼ��ʾ�����ַ�Ӧ�������û���г�������֪HΪ����Ԫ�صĹ�̬�����F�Ǻ��ɫ������ˮ�ij�������A��B��C��D��E��F���������о���ͬһ��Ԫ�ء�?

����д���пհף�
��1��A��B��C��D��E��F����������������ͬһ��Ԫ����Ԫ�����ڱ���λ��___________
��2��д��C��H���ʵĻ�ѧʽ��C__________��?H?_____________
��3��д����Ӧ�١��Ļ�ѧ����ʽ�ۡ͢��ߵ����ӷ���ʽ��
��Ӧ�٣�________________________________
��Ӧ�ޣ�________________________________
��Ӧ�ۣ�________________________________
��Ӧ�ߣ�________________________________
��4����Ӧ�����е�������_____________��
�ο��𰸣���1���������ڵڢ���
��2��?C��?FeCl2��H��?Al2O3?
��3����?8Al+3Fe3O4 4Al2O3+9Fe��
4Al2O3+9Fe��
��4Fe(OH)2+O2+2H2O=4Fe(OH)3
��Fe3O4+8H+=Fe2+ +2Fe3+ +4H2O��
��2Al+2OH-+2H2O=2AlO2-+3H2��
��4��?�а�ɫ����Ѹ�ٱ�ɻ���ɫ�����ձ�Ϊ���ɫ��
���������
�����Ѷȣ�һ��
4���ƶ��� ��A���ܱ������м��ȵ����ʵ�����ȵ�B��C��D��E�������壬����ȴ������һ���¶�ʱ�������о�������X���ɣ���ʱԭ4��������ֻ��Bû�вμӷ�Ӧ��������ͬ������B������������ܶ�Ϊ14�����ж����塣�й����ʵ�ת����ϵ����ͼ������E�ڳ�����Ϊ��ɫҺ�壬GΪ����ɫ���壬X��F��һ�ֳ����ĵ��ʡ���Ӧ����n(C):n(D)=2 :1����Ӧ�٢ڢۢ��ڹ�ҵ�����о�����ҪӦ�ã�ͼ�в��ַ�Ӧ����������δע�����Իش���������
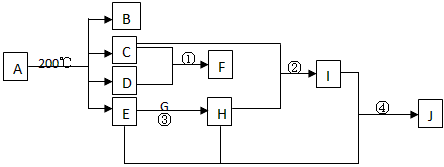
(1)A�Ļ�ѧʽ__________�� C�ĵ���ʽ__________��D�Ľṹʽ__________��
(2)д����ѧ��Ӧ����ʽ��____________________��
(3)д��J��ϡ��Һ�����ͭ�����ӷ�Ӧ����ʽ____________________��
�ο��𰸣�(1)NH4HC2O4��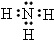 ��
��
(2)4NH3+5O2 4NO+6H2O
4NO+6H2O
(3)3Cu+8H++2NO3-�T�T3Cu2++2NO��+4H2O
���������
�����Ѷȣ�һ��
5������� �й�Ԫ��X��Y��Z��D��E����Ϣ����
| Ԫ�� | �й���Ϣ
X
Ԫ����Ҫ���ϼ�Ϊ-2��ԭ�Ӱ뾶Ϊ0.074nm
Y
��������������������������֮��Ϊ4
Z
ԭ�Ӱ뾶Ϊ0.102nm���䵥����X�ĵ�����ȼ�գ���������������ɫ����
D
����������������ǿ����������ǿ��
E
�����������г�������������Ʒ�ڳ�ʪ�������ױ���ʴ����
|
�û�ѧ������������⣺
��1��E��Ԫ�����ڱ��е�λ��Ϊ______��Z���⻯�����ʽΪ______
��2���е㣺������______X���⻯��������������
X��Y��D�γɵļ����ӵİ뾶�ɴ�СΪ______��
��3��X��һ���⻯�������ʵ������ȡX�ĵ��ʣ��䷴Ӧ�Ļ�ѧ����ʽΪ______��D���������������ǿ������ӷ���ʽΪ______��
��4��EԪ����YԪ�ؿ��γ�EY2��?EY3���ֻ��������˵����ȷ���ǣ�����ţ�______��
�ٱ���EY2��Һʱ��������Һ��������E����
��EY2��E2Y3����ͨ�����Ϸ�Ӧ����
��ͭƬ��̼����EY3��Һ���ԭ��أ�������ͭƬ�ص�������̼��
������е�NaoH��Һ�еμӼ��α���EY3��Һ�������Ƶý���
��5����ͼ��ʾ���ʾ�Ϊ������������м�Ϊ��������Ԫ���е�������ɣ����ڳ�����ΪҺ̬����ҵ�ϳ��õ����ұ��������������ҷ�����Ӧ�Ļ�ѧ����ʽ______��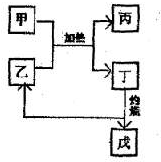
�ο��𰸣�XԪ����Ҫ���ϼ�Ϊ-2��ԭ�Ӱ뾶Ϊ0.074nm����X���ڵڢ�A�壻Zԭ�Ӱ뾶Ϊ0.102nm���䵥����X�ĵ�����ȼ�գ���������������ɫ���棬��ZΪSԪ�أ�XΪOԪ�أ�D����������������ǿ����������ǿ���DΪAlԪ�أ�
E�����������г�������������Ʒ�ڳ�ʪ�������ױ���ʴ������EΪFeԪ�أ�Y��������������������������֮��Ϊ4�����������Ԫ��ΪO��Cl������XΪOԪ�أ���YΪClԪ�أ�
��XΪOԪ�أ�YΪClԪ�أ�ZΪSԪ�أ�DΪAlԪ�أ�EΪFeԪ�أ�
��1��EΪFeԪ�أ�����Ԫ�����ڱ��������ڵڢ��壻ZΪSԪ�أ��⻯��ΪH2S�����ڹ��ۻ������ԭ������ԭ��֮���γ�1�Թ��õ��Ӷԣ�����ʽΪ
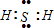
��
�ʴ�Ϊ���������ڵڢ��壻
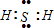
��
��2��XΪOԪ�أ����⻯��ΪH2O������ΪҺ̬����Ԫ�ص縺�Ժ�ǿ��ˮ����֮�������������Էе������⣼H2O��
�ʴ�Ϊ������
X��Y��D�γɵļ����ӷֱ�ΪO2-��Cl-��Al3+��O2-��Al3+���ӵĺ�������Ų���ͬ���˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶O2-��Al3+��Cl-��O2-��������������ͬ�����Ӳ�Խ�࣬���Ӱ뾶Խ���������Ӱ뾶Cl-��O2-���������Ӱ뾶Cl-��O2-��Al3+��
�ʴ�Ϊ������Cl-��O2-��Al3+��
��3��XΪOԪ�أ�X��һ���⻯�������ʵ������ȡX�ĵ��ʣ���Ϊ��������ֽ���ȡ��������Ӧ����ʽΪ
2H2O2?MnO2?.?2H2O+O2����D�����������ΪAl2O3������ǿ������ƫ��������Ӻ�ˮ��
���ӷ���ʽΪAl2O3+2OH-=2AlO2-+H2O��
�ʴ�Ϊ��2H2O2?MnO2?.?2H2O+O2����Al2O3+2OH-=2AlO2-+H2O��
��4��EԪ����YԪ�ؿ��γ�EY2��?EY3���ֻ�����ΪFeCl2��FeCl3��
��FeCl2�ױ���������������FeCl2��Һʱ��������Һ��������Fe���ʣ��ʢ���ȷ��
��FeCl2��ͨ��FeCl3��Fe���ϵõ���FeCl3���������������ϵõ����ʢ���ȷ��
��ͭƬ��̼����FeCl3��Һ���ԭ��أ�ͭ����������Ӧ��Ϊ������������ͭƬ�ص�������̼�����ʢ���ȷ��
������е�NaoH��Һ�еμӼ��α���FeCl3��Һ���õ������������������ܵõ������������壬�ʢܴ���
��ѡ���٢ڢۣ�
��5����Ϊ��������Ԫ���е�������ɣ����ڳ�����ΪҺ̬������Ϊˮ����ҵ�ϳ��õ����ұ����������Ϊ�����������Զ�Ϊ�����������ʼ�Ϊ���Σ���Ϊ�Ȼ�����������ҷ�����Ӧ�Ļ�ѧ����ʽ AlCl3+3H2O?��?.?Al��OH��3+3HCl����
�ʴ�Ϊ��AlCl3+3H2O?��?.?Al��OH��3+3HCl����
���������
�����Ѷȣ�һ��