��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (8��)2molCO2������Ϊ??g����������ԼΪ??�����ڱ�״������ռ�е����ԼΪ??L������ԭ�ӵ����ʵ���Ϊ??mol��
�ο��𰸣�(8��) 88? 2NA? 44.8? 4? ( ÿ��2��)
�����������
�����Ѷȣ�һ��
2��ѡ���� ��NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A��14g����ͨʽΪCnH2n�������к��е�C��C����ĿΪNA/n
B����״���£�NO�� O2��11.2 L��ϣ����û������ķ�������Ϊ 0.75 NA
C��25��ʱ��pH��7��NH4Cl��NH3?H2O�����Һ�У�OH��������Ϊ10��7 NA
D������2.7g���ֱ���100mLŨ��Ϊ2 mol��L�D1�����������������Һ��ַ�Ӧ��ת�Ƶĵ�������Ϊ0.3NA
�ο��𰸣�A
���������
��ȷ�𰸣�A
B������ȷ��2NO��O2=2NO2? 2NO2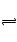 N2O4
N2O4
C?ֻ��Ũ�ȣ�û���������������������
D������㣬����ʣ�࣬�������ᷴӦ����������㣬ת�Ƶĵ�����Ϊ0.2NA
�����Ѷȣ�һ��
3������� CO��CH4��Ϊ�����Ŀ�ȼ�����塣
120�桢101 kPa�£�a mL��CO��CH4��ɵĻ��������bmL O2����ȫȼ�պָ���ԭ�¶Ⱥ�ѹǿ��
��1�����������������ǡ����ȫ��Ӧ������bmL������̼�����������һ����̼�ͼ�������ʵ���֮��Ϊ�� ��������м������������Ϊ�� ��
��2����ȼ�պ����������С��a/4 mL����a��b��ϵ����ѧ��ʾʽ�� 91EXAM.org��
�ο��𰸣���9�֣���1��2:1 22.2%��2��b��5a/4
�����������1�����ݷ���ʽ2CO+O2 2CO2��CH4+2O2
2CO2��CH4+2O2 CO2+2H2O����֪�������Ķ�����̼�����ĵ������������ͬʱCO��CH4�����ʵ���֮����2:1�����������м��������������16/(2��28+16) ��100%=22.2%;
CO2+2H2O����֪�������Ķ�����̼�����ĵ������������ͬʱCO��CH4�����ʵ���֮����2:1�����������м��������������16/(2��28+16) ��100%=22.2%;
��2��120�桢101 kPa��ˮ�����壬����ȼ�պ�������������䣬��COΪxml��CH4Ϊyml����
2CO+O2 2CO2 ��V
2CO2 ��V
x x/2 x x/2
CH4+2O2 CO2+2H2O��
CO2+2H2O��
y 2y y
��x+y=a��x/2+2y��b��x/2=a/4����ʽ�������b��5a/4
���㣺���黯ѧ����ʽ�ļ���
�����Ѷȣ�����
4��ѡ���� �����������У�������һ������50mol?NH4Cl��16mol?KCl��24mol?K2SO4��Ӫ��Һ������KCl��NH4Cl�ͣ�NH4��2SO4���ֹ���Ϊԭ�������ƣ����ߵ����ʵ��������ǣ���λΪmol��
A.2��64��24
B.64��2��24
C.32��50��12
D.16��50��24
�ο��𰸣�B
���������������������Ը��������غ��˼���������������ֻ�У�NH4��2SO4�����ṩ�������24mol?K2SO4�������Ϊ24mol��Ϊ��������ֵ㣮
�����KCl��NH4Cl�ͣ�NH4��2SO4���ֹ������Ƶ�Ӫ��Һ�и��������ʵ����뺬50molNH4Cl��16molKCl��24molK2SO4��Ӫ��Һ�е����ӵ����ʵ�����ͬ��Ӫ��Һ�����ӵ����ʵ����ֱ�Ϊ��
n��NH4+ ��=50mol��n��Cl-��=66mol��n��K+��=64mol��n��SO42- ��=24mol��
��������������غ��֪����Ҫn[��NH4��2SO4]=24mol��
����笠������غ��n��NH4Cl��=50mol-24mol��2=2mol��
���������غ㣬��n��KCl��=66mol-2mol=64mol��
��ѡB��
���������⿼��ѧ���غ�˼���ڽ����е�Ӧ�ã�Ҫ��ѧ������һ���ķ����ͽ�������������
�����Ѷȣ�����
5������� �ڱ�״���£�
��1��0.5mol?HClռ�е������______
��2��33.6L?H2�����ʵ�����______
��3��16gO2���ܶ���______
��4��44.8LN2�к��е�N2��������______��
�ο��𰸣���1����״����Vm=22.4L/mol��HCl�����Ϊ0.5mol��22.4L/mol=11.2L���ʴ�Ϊ��11.2L��
��2����״����Vm=22.4L/mol��H2�����ʵ���Ϊ33.6L22.4L/mol=1.5mol���ʴ�Ϊ��1.5mol��
��3����״����Vm=22.4L/mol��������M=32g/mol�����=MVm=32g/mol22.4L/mol=1.4g/L���ʴ�Ϊ��1.4g/L��
��4����״����Vm=22.4L/mol��N2��n=VVm=44.8L22.4L/mol=2mol��
���е�N2������Ϊ2��NA=2NA=1.204��1024���ʴ�Ϊ��2NA��1.204��1024��
���������
�����Ѷȣ�һ��