微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在恒温、恒容的密闭容器中进行反应A(g) B(g)+C(g)。若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需反应时间为?
B(g)+C(g)。若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需反应时间为?
[ ]
A.10s
B.大于10s
C.小于10s
D.无法判断
参考答案:B
本题解析:
本题难度:一般
2、选择题 在一密闭容器中,CO和H2O混合加热到800℃达到下列平衡:CO(g)+H2O(g)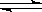 CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为
CO2(g)+H2(g) ,K=1.0,若反应开始时CO和H2O的浓度分别为0.20mol/L和1.00mol/L,则CO转化为CO2的转化率为
A.80%
B.83%
C.75%
D.91%
参考答案:B
本题解析:设CO转化为CO2的转化率为x,则
由反应方程式:?CO(g)+? H2O(g)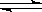 CO2(g)+H2(g) ,K=1.0
CO2(g)+H2(g) ,K=1.0
起始浓度(mol/L)0.20? 1.00? 0? 0
变化浓度(mol/L)x? x? x? x
平衡浓度(mol/L)0.20―x? 1.00―x? x? x
即:
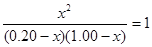 ,得
,得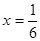 ,即得CO转化为CO2的转化率为83%
,即得CO转化为CO2的转化率为83%
本题难度:一般
3、填空题 (每空2分共8分)
向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
①.若a=0,b=0,则c=?
②.若a=0.7,b=2.1,则:
Ⅰ.c=??.
Ⅱ.这时反应向?进行.
Ⅲ.若要维持反应开始向该反应方向进行,c的范围是?
参考答案:4? 2.6?逆反应方向? 1<c≤4
本题解析:略
本题难度:简单
4、选择题 只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是
A.K不变,平衡可能移动
B.K值变化,平衡一定移动
C.平衡移动,K值可能不变
D.平衡移动,K值一定变化
参考答案:D
本题解析:化学平衡移动的一般影响因素是浓度、温度与压强等,但化学平衡常数只与温度有关,温度变,平衡常数才会变。故选D.
本题难度:一般
5、选择题 从植物花汁中提取的一种有机物HIn,可做酸、碱指示剂,在水溶液中存在电离平衡:HIn(红色)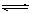 H+ + In-(黄色)△H>0对上述平衡解释不正确的是
H+ + In-(黄色)△H>0对上述平衡解释不正确的是
A.升高温度平衡向正方向移动
B.加入盐酸后平衡向逆方向移动,溶液显红色
C.加入NaOH溶液后平衡向正方向移动,溶液显黄色
D.加入NaHSO4溶液后平衡向正方向移动,溶液显黄色
参考答案:D
本题解析:正反应是吸热反应,所以升高温度平衡向正方向移动,A正确;加入盐酸后增大氢离子浓度,平衡向逆方向移动,溶液显红色,B正确;加入NaOH溶液后消耗氢离子,降低氢离子浓度,平衡向正方向移动,溶液显黄色,C正确;加入NaHSO4溶液后增大氢离子浓度,平衡向逆方向移动,溶液显红色,D不正确,答案选D。
点评:电离平衡也是动态平衡,适用于勒夏特列原理。
本题难度:一般