��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij�¶��£���2mo1A��3mo1B����һ�ܱ������У�������Ӧ��aA(g)��B(g)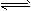 C(g)��D(g)��5min ��ﵽƽ�⡣��֪���¶�����ƽ�ⳣ��K=1 �����¶Ȳ���ʱ���������������Ϊԭ����10����A��ת���ʲ������仯����
C(g)��D(g)��5min ��ﵽƽ�⡣��֪���¶�����ƽ�ⳣ��K=1 �����¶Ȳ���ʱ���������������Ϊԭ����10����A��ת���ʲ������仯����
[? ]
A��a=1
B��a=2
C��B��ת����Ϊ40%
D��B��ת����Ϊ20%
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
2��ѡ���� 3molA��2.5molB���ʢ���ݻ�Ϊ2L�������ڣ�ʹ���Ƿ�����Ӧ2A(s)+3B(g)? 2C(g)+D(g)������5min����0.5molD������˵����ȷ����?��?��

A��B��ƽ����������Ϊ0.3mol(L��min)
B��C��ƽ��Ũ��Ϊ2mol/L
C��ƽ�������ѹǿ��ƽ�⽫���������ƶ�
D������λʱ�������ɵ�B��C�����ʵ���֮��Ϊ3��2������ϵ����ƽ��״̬
�ο��𰸣�D
���������
��ȷ�𰸣�D
A������ȷ��B��ƽ����������Ϊ1.5mol��2L��5MIn=0.15mol(L��min)�D1
B������ȷ��C��ƽ��Ũ��Ϊ1mol/2L=0.5mol/L
C������ȷ��ƽ�������ѹǿ��ƽ�ⲻ�ƶ���AΪ���塣
D����ȷ������λʱ�������ɵ�B��C�����ʵ���֮��Ϊ3��2������B��ʾ������������C��ʾ����������������ɱ���������ϵ����ƽ��״̬
�����Ѷȣ�һ��
3������� ��500�桢101KPa�����£���a?mol?SO2��b?mol?O2����һ�ݻ��ɱ���ܱ������У��ﵽƽ��ʱSO3�������Ϊ40%�����¶Ⱥ�ѹǿ���ֲ��䣬ƽ��ʱ�ܱ��������ݻ�Ϊ��ʼ��______����
�ο��𰸣���Ӧ�ķ���ʽΪ��2SO2+O2

2SO3����ƽ��ʱת����xmolO2����
? 2SO2+O2

2SO3
��ʼ��amol bmol? 0
ת����2xmol? xmol? 2xmol
ƽ�⣺��a-2x��mol? ��b-x��mol 2xmol
����2xa-2x+b-x+2x��100%=40%��
x=a+b6
���ݰ����ӵ������жϣ�ѹǿһ��������������ʵ���֮�ȵ������֮�ȣ�
��ƽ��ʱ�ܱ��������ݻ�Ϊ��ʼ��a+b-xa+b=56��
�ʴ�Ϊ��56��
���������
�����Ѷȣ���
4��ѡ���� t��ʱ����һ�ܱ������г���2molA��3molB���������»�ѧ��Ӧ��aA(g)+B(g) C(g)+D(g) ��֪��ƽ��ʱ��Ca(A)��C(B)= C(C)��C(D),Ȼ�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬��B��ת������?��?��
C(g)+D(g) ��֪��ƽ��ʱ��Ca(A)��C(B)= C(C)��C(D),Ȼ�����¶Ȳ��������£����������ݻ���ԭ��10�������A�İٷֺ���ʼ��δ�иı䣬��B��ת������?��?��
A. 60%? B. 40%? C. 4%? D. ��ȷ��
�ο��𰸣�B
���������ƽ��ʱ��Ca(A)��C(B)= C(C)��C(D),��ƽ�ⳣ��K��1�����¶Ȳ��������£����������ݻ���ԭ��10����A�İٷֺ���ʼ��δ�иı䣬��˵����Ӧǰ������Dz���ģ���˦���1����B��ת������x��������C��D�����ʵ�������3x��ƽ��ʱʣ��A��B�ֱ���2��3x��3��3x������ �����x��0.4����ѡB��
�����x��0.4����ѡB��
�����Ѷȣ�һ��
5��ѡ���� ��ij���ݵ��ܱ������У����淴ӦA(g)��B(g)  ?xC(g)����ͼ��ʾ�Ĺ�ϵ���ߣ�����˵����ȷ���ǣ�?��
?xC(g)����ͼ��ʾ�Ĺ�ϵ���ߣ�����˵����ȷ���ǣ�?��
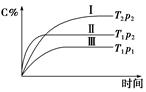
A���¶ȣ�T1��T2
B��ѹǿ��p1��p2
C������Ӧ�����ȷ�Ӧ
D��x��ֵ��2
�ο��𰸣�A
����������������ߢ�����ߢ��֪�����ߢ��ȴﵽƽ�⣬��T1��T2�������¶ȣ�C%��С��˵������ӦΪ���ȷ�Ӧ��A�ԡ�C�����������ߢ�����ߢ��֪�����ߢ��ȴ�ƽ�⣬˵��ѹǿp2��p1������ѹǿ��C%���ӣ�˵��ƽ��������Ӧ�����ƶ���x��1��B����D����
�����Ѷȣ�һ��