微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 镍--镉(Ni--Cd)可充电电池可以发生如下反应:
Cd(OH)2 + 2Ni(OH)2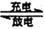 Cd + 2NiO(OH)+ 2H2O
Cd + 2NiO(OH)+ 2H2O
由此可知,该电池充电时的阳极是(?)。
A.Cd
B.NiO(OH)
C.Cd(OH)2
D.Ni(OH)2
参考答案:D
本题解析:阳极发生氧化反应,化合价升高,故选D。
点评:本题考查的是电解原理的应用,难度不大,旨在考查学生对基础知识的掌握情况。
本题难度:简单
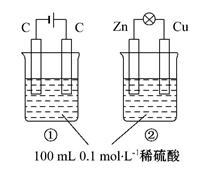
2、选择题 10. 关于如图所示①、②两个装置的评价正确的是

参考答案:D
本题解析:A项装置①外加了电源,为电解池,装置②形成Zn、Cu原电池;B项电解稀硫酸实质是电解水,所以装置①中硫酸浓度增大,装置②的总反应为:Zn+H2SO4=ZnSO4+H2↑,硫酸浓度减小;C项电解硫酸溶液的阳极为OH?失电子:4OH--4e-=2H2O+O2↑,原电池的正极为H+得电子:2H++2e?=H2↑;D项电解池电解质溶液中阳离子向阴极移动,原电池电解质溶液中阳离子向正极移动。
考点:电解池和原电池的工作原理
点评:本题综合考查了化学电源的相关知识,注重考查学生分析问题的能力,难度不大,注意把握化学电源的工作原理。
本题难度:一般
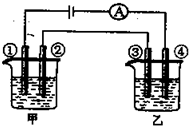
3、选择题 用铂电极电解下表中各组物质的稀溶液(如图)一段时间后,甲、乙两池中溶液的pH均碱小,且在①和④两极的电极产物的物质的量之比为1:2的是( )
| A | B | C | D
甲
KOH
H2SO4
Na2SO4
CuSO4
乙
CuSO4
AgNO3
HCl
HNO3
|
A.A
B.B
C.C
D.D
参考答案:A、甲池中,电解氢氧化钾的实质是电解水,碱性增强,pH增大,故A错误;
B、甲池中,①是阳极,发生电极反应:4OH-=4e-+O2+2H2O,电解硫酸的实质是电解水,酸性增强,pH减小,乙池中,④电极是阴极,发生电极反应4Ag++4e-=4Ag,在转移电子一样的情况下,①电极产生的氧气和④电极产生的金属银物质的量之比是1:4,故B错误;
C、甲池中,①是阳极,发生电极反应:4OH-=4e-+O2+2H2O,电解硫酸钠的实质是电解水,pH不变,故C错误;
D、甲池中,①是阳极,发生电极反应:4OH-=4e-+O2+2H2O,电解硫酸铜的过程生成硫酸,溶液酸性增强,pH减小,乙池中,④电极是阴极,发生电极反应4H++4e-=2H2,在转移电子一样的情况下,①电极产生的氧气和④电极产生的氢气物质的量之比是1:2,故D正确.
故选D.
本题解析:
本题难度:简单
4、填空题 氢气是一种清洁能源,氢气的制取与储存是氢气能源利用领域的研究热点。
已知:CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH =+206.2 kJ・mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH =+247.4 kJ・mol-1
2H2S(g)=2H2(g)+S2(g)ΔH =+169.8 kJ・mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与 H2O(g)反应生成CO2(g)和 H2(g)的热化学方程式为_________________________
(2)H2S 热分解制氢时,常向反应器中通入一定比例空气,使部分 H2S 燃烧,其目的是________;燃烧生成的 SO2与 H2S 进一步反应,生成物在常温下均为非气体,写出该反应的化学方程式:___________________________
(3)H2O 的热分解也可得到 H2,高温下水分解体系中主要气体的体积分数与温度的关系如图甲所示。图中 A、B 表示的物质依次是______________________________________。
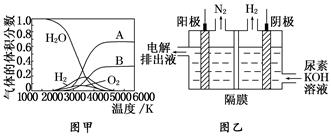
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图乙(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为_____________________
(5)Mg2Cu 是一种储氢合金。 350 ℃时,Mg2Cu 与 H2反应,生成 MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为 0.077)。Mg2Cu 与 H2反应的化学方程式为_____________________________________
参考答案:(1)CH4(g)+2H2O(g)=CO2(g)+4H2(g)ΔH=+165.0 kJ・mol-1
(2)为H2S热分解反应提供热量
2H2S+SO2=2H2O+3S(或4H2S+2SO2=4H2O+3S2)
(3)H、O(或氢原子、氧原子)
(4)CO(NH2)2+8OH--6e-=CO +N2↑+6H2O
+N2↑+6H2O
(5)2Mg2Cu+3H2△,MgCu2+3MgH2
本题解析:本题考查化学反应与能量,化学能与电能的转化及元素化合物相关知识,意在考查考生的综合运用能力。
(1)将所给反应依次编号为①②③,根据盖斯定律,由反应①×2-反应②即得题述反应的热化学方程式:CH4(g)+2H2O(g)=CO2(g)+4H2(g)ΔH=+165.0 kJ・mol-1。
(3)由图中A、B的体积分数比例近似为2∶1,则可确定A为H原子,B为O原子。
(4)H2是由溶液中的H+在阴极放电得到的,则阳极产生的是N2,阳极发生氧化反应,在碱性环境下的电极反应式为:CO(NH2)2+8OH--6e-=CO +N2↑+6H2O。
+N2↑+6H2O。
(5)由Mg2Cu变为MgCu2,可知Mg含量下降,则生成物中氢化物仅含的一种金属元素必为Mg,再根据其中氢的质量分数为0.077,则Mg与H物质的量之比为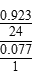 =
= ,即化学式为MgH2,则反应的化学方程式为:2Mg2Cu+3H2△,MgCu2+3MgH2。
,即化学式为MgH2,则反应的化学方程式为:2Mg2Cu+3H2△,MgCu2+3MgH2。
本题难度:困难
5、选择题 在U形管中,用惰性电极电解硫酸钠和石蕊的混合液,可观察到的现象是()
A.两极附近颜色无明显变化
B.两极均有气体产生,且阳极所产生的气体是阴极的两倍
C.阳极附近的颜色变红
D.阴极附近的颜色变红
参考答案:C
本题解析:略
本题难度:简单