��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��MgƬ��AlƬΪ�缫�����õ������ӣ�ͬʱ����NaOH��Һ�У�����Ϊ_________��
�ο��𰸣�Al
���������
�����Ѷȣ�һ��
2��ѡ���� ﮷�������������������ܶȸߣ��ɱ��ͣ����ڴ����ƹ㡣����ܷ�ӦʽΪ��
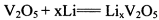 ,�õ�طŵ�ʱ���й�˵����ȷ���ǣ�)
,�õ�طŵ�ʱ���й�˵����ȷ���ǣ�)
A����������������Ӧ���缫����ΪV2O5
B������������������ƶ�
C�������ĵ缫��ӦʽΪ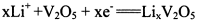
D���õ�ص���������Ҳ����KOH��Һ����
�ο��𰸣�C
�����������������������Ӧ���缫����ΪLi ��A������ڵ�·������������Ǩ�ƣ�B�������ڵ��������ˮ��Ӧ���ʵ�ز���ʹ��ˮ��Һ������ʣ�D��������������ԭ��Ӧ��C��ȷ��
�����Ѷȣ�һ��
3��ѡ���� ȼ�ϵ����һ�����͵�أ�����Ҫ������ȼ����ȼ�չ����аѻ�ѧ��ֱ��ת��Ϊ���ܣ�����ȼ�ϵ�صĻ�����Ӧ�ǣ�
X����2O2(g)��2H2O(l)��4e����4OH��?
Y����2H2(g)��4OH���C4e����4H2O(l)?
�����ж���ȷ����?
[? ]
A��X������?Y������������Ӧ?
B��Y������?X������������Ӧ
C��?X�Ǹ���?Y��������ԭ��Ӧ?
D��Y�Ǹ���?X������������Ӧ
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4������� (9��)���ྻ�Ľ���ƬFe��Zn ��A��B �ֱ���Cu�õ���������ں��ʵĵ������Һ�ʵ�鲢��¼��ѹָ����ƶ�����͵�ѹ���Ķ��������ʾ��
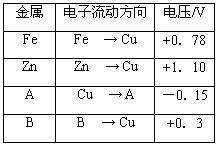
����ʵ���¼�����������գ�
��1���������缫�Ľ���������Խ��ѹ���Ķ���Խ ���������С������
��2��Zn��A��B���ֽ��������ǿ������˳���� ��
��3��Cu��A��ɵ�ԭ��أ� Ϊ������
�˵缫��ӦʽΪ ��
��4��A��B�γɺϽ�¶���ڳ�ʪ�����У� �ȱ���ʴ��
��5�����ȷ�Ӧ�е����ȼ��ijɷ���
��ҵ�ϳ��õ�����ұ���Ļ�ѧ����ʽΪ ��
�ο��𰸣���1����1�֣� ��2��Zn> B > A��1�֣� ��3��Cu��1�֣� Cu��2e��= Cu2+ ��2�֣� ��4��B��1�֣� ��5�����ۺͽ���������Ļ���1�֣� 2Al2O3="=" 4Al+3O2��2�֣�(���������÷�)
�����������
�����Ѷȣ���
5������� ��1����пƬ����Ƭ����ϡ���������ԭ��أ�����������һ�������ơ�пƬ�Ϸ����ĵ缫��ӦʽΪ�� ����Ƭ�Ϸ����ĵ缫��ӦʽΪ�� ��
��2�����õ����������������Ϊ100g������һ��ʱ���ȡ��пƬ����Ƭϴ�ɾ��������������Ϊ67.5g�� ������������������״����Ϊ ��
�ο��𰸣�(1)Zn �� 2e¯ = Zn2+ ,2H++2e¯= H2 ,��2��11.2L
�����������1����пƬ����Ƭ����ϡ�������������пƬΪ����ͭƬΪ������ԭ��أ�пƬ�Ϸ����ĵ缫��ӦʽΪ��)Zn �� 2e¯ = Zn2+ ,��Ƭ�Ϸ����ĵ缫��ӦʽΪ��2H++2e¯= H2��
��2�����ڷ�Ӧ��п�ܽ⣬���Է�Ӧ��п������m=100-67.5=32.5g��Ϊ32.5/65=0.5mol��ת�Ƶĵ�����Ϊ1mol������������0.5mol���������������������״����Ϊ11.2L��
���㣺ԭ���
���������⿼����ԭ��صĵ缫����д�Լ�һЩ�ļ��㣬�����ѶȲ���
�����Ѷȣ�һ��