微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上利用可逆反应N2(g)+3H2(g)  2NH3(g)合成氨,下列叙述正确的是
2NH3(g)合成氨,下列叙述正确的是
A.合成氨的适宜条件是高温、高压、催化剂,其中催化剂不改变该反应的逆反应速率
B.恒容通入氩气,使反应体系的压强增大,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,NH3 (g)的浓度分别是c1、c2,则时间间隔t1~t2内,NH3 (g)生成的平均速率为v=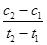
参考答案:D
本题解析:催化剂在反应中同等程度的改变正、逆反应速率,A错;B项:通入氩气压强增大,但是物质的浓度不变,所以速率不变;C项:降温会减小反应速率,将延长达到平衡的时间,错误;D项由反应速率的表达式可知正确。
本题难度:一般
2、填空题 液化石油气中常存在少量有毒气体羰基硫(COS),必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。
(1)写出羰基硫的电子式 ,羰基硫分子属于 (选填“极性”、“非极性”)分子。
(2)下列能说明碳与硫两元素非金属性相对强弱的是 。
a.相同条件下水溶液的pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
(3)羰基硫在水存在时会缓慢水解生成H2S,对钢铁设备产生电化学腐蚀。写出正极的电极反应式 ,负极的反应产物为 (填化学式)。
为除去羰基硫,工业上常采用催化加氢转化法,把羰基硫转化为H2S再除去:COS + H2 CO + H2S
CO + H2S
(4)已知升高温度,会降低羰基硫的转化率。则升高温度,平衡常数K ,反应速率 (均选填“增大”、“减小”、“不变”)。
(5)若反应在恒容绝热密闭容器中进行,能说明该反应已达到平衡状态的是 。
a.容器内气体密度保持不变 b.容器内温度保持不变
c.c(H2)=c(H2S) d.υ(H2)正=υ(H2S)正
(6)已知该反应的平衡常数很大,说明 。
参考答案:(1)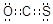 , 极性 (各1分,共2分)
, 极性 (各1分,共2分)
(2)a c (2分)
(3)H2S + 2e → H2↑+S2-(或2H+ + 2e → H2↑)(2分) FeS(1分)
(4)减小,增大(各1分,共2分)
(5)b (2分)
(6)正反应进行程度很大(1分。其他合理答案也给分)
本题解析:(1)羰基硫相当于是二氧化碳中的1个氧原子被硫原子取代,所以其电子式为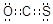 。S和O的非金属性不同,所以该化合物是极性分子。
。S和O的非金属性不同,所以该化合物是极性分子。
(2)a.非金属性越强,最高价氧化物对应水化物的酸性越强,相应的钠盐水解程度越小,所以相同条件下水溶液的pH:Na2CO3>Na2SO4可以碳与硫两元素非金属性相对强弱,a正确;b.非金属性越强,最高价氧化物对应水化物的酸性越强,亚硫酸不是最高价含氧酸,所以酸性:H2SO3>H2CO3不能说明碳与硫两元素非金属性相对强弱,b不正确;c.CS2中碳元素为+4价,硫元素为-2价,说明非金属性是硫强于碳,c正确,答案选ac。
(3)原电池中负极失去电子发生氧化反应,正极得到电子发生还原反应,硫化氢分子中氢元素得到电子,发生还原反应,因此电极反应式为H2S + 2e → H2↑+S2-。负极铁失去电子,生成亚铁离子与硫离子结合生成硫化亚铁,所以负极产物是FeS。
(4)升高温度,会降低羰基硫的转化率,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应。则升高温度,平衡常数K减小,而反应速率增大。
(5)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,则a.密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此容器内气体密度始终保持不变,不能说明反应达到平衡状态,a不正确;b.由于反应在恒容绝热密闭容器中进行,所以容器内温度保持不变可以说明反应达到平衡状态,b正确;c.平衡时浓度不再发生变化,但物质的浓度之间不一定相等,故c(H2)=c(H2S) 不能说明反应达到平衡状态,c不正确;d.υ(H2)正=υ(H2S)正,但二者的反应速率方向相同,所以不能说明反应达到平衡状态,d不正确,答案选b。
(6)平衡常数越大,反应物的转化率越大,因此若该反应的平衡常数很大,说明正反应进行程度很大。
考点:考查非金属性强弱比较、原电池原理、外界条件对平衡状态以及有关平衡常数的应用
本题难度:困难
3、选择题 下列反应中生成H2的速率最慢的是
[? ]
金属?
酸溶液
温度
A.
Mg?
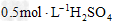
20℃
B.
Fe?

20℃
C.
Mg?

20℃
D.
Mg?

30℃
参考答案:B
本题解析:
本题难度:一般
4、选择题 在某一化学反应中,反应物B的浓度在5 s内从2.5 mol/L变成0.5 mol/L,在这5 s内B的化学反应速率为( )
A.0.4 mol/L
B.0.4 mol/L・s
C.0.4mol-1・L-1・s-1
D.0.4 mol/(L・s)
参考答案:D
本题解析:反应速率通常用单位时间内浓度的变化量来表示,则该反应的反应速率是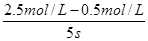 =0.4 mol/(L・s),答案选D。
=0.4 mol/(L・s),答案选D。
考点:考查反应速率的有关计算
点评:该题是基础性试题的考查,侧重对学生基础知识的巩固和训练,难度不大。该题的关键是明确反应速率的含义和计算依据,然后结合题意灵活运用即可,有利于培养学生规范的答题能力和逻辑推理能力。
本题难度:一般
5、计算题 在一个容积不变的反应器中,要求调节体系的温度使下列反应达到平衡时,保持容器内气体的总物质的量为12 mol。
已知反应A(g)+2B(g) 2C(g),现向容器中加入6.5 mol A、x mol B、2.0 mol C。
2C(g),现向容器中加入6.5 mol A、x mol B、2.0 mol C。
(1)若x=5.5时,需要降低体系的温度使反应在平衡时达到题设条件,则正反应为_______(填“吸热”或“放热”)反应。
(2)欲使起始反应维持向逆反应方向进行,则x的取值范围为_________。
(3)在一定温度下的上述平衡体系中,另按1∶2 的物质的量之比通入D和E两种气体(此时容器内气体的总物质的量不要求保持12 mol),按下式反应:D(g)+E(g) 2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入m mol D,n mol F和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为________mol(设A、B、C与D、E、F之间均不反应)。
2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入m mol D,n mol F和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为________mol(设A、B、C与D、E、F之间均不反应)。
参考答案:(1)放热(2)2.5<x<3.5
(3)2m+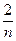
本题解析:(1)? A(g)? +? 2B(g) 2C(g)
2C(g)
起始/mol? 6.5? x?2
平衡n总="12" mol
当x=5.5时,6.5+5.5+2=13>12,降温使平衡向右移动,使n总="12" mol,故正反应为放热反应。
(2)若维持反应向逆反应方向进行,则有:
6.5+x+2<12,所以x<3.5。
设C转化了a? mol则:
A(g)? +? 2B(g) 2C(g)
2C(g)
起始6.5? x? 2
平衡6.5+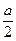 ? x+a? 2-a
? x+a? 2-a
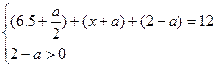
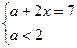 ?所以x>2.5
?所以x>2.5
故x的取值范围是2.5<x<3.5。
(3)另有反应:D(g)? +? E(g) 2F(g)
2F(g)
起始:? m? n(E)? n
新平衡:(m+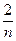 )∶[n(E)+
)∶[n(E)+ 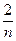 ]=1∶2。
]=1∶2。
由于是等体积反应,保持(m+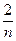 )∶[n(E)+
)∶[n(E)+ 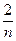 ]=1∶2即可,n(E)=2m+
]=1∶2即可,n(E)=2m+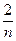 。
。
本题难度:简单