微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 元素周期律和元素周期表对深化物质性质的认识具有重要的作用,有利于将零乱的元素化合物知识整合起来形成知识网络.某同学整理了关于氯元素的相关知识,请你补充完整.
(1)氯元素的原子结构示意图为______,在周期表中的位置为______.
(2)氯、硫、磷三种元素对应的气态氢化物中,稳定性由强到弱的顺序为______,氯、溴两种元素的单质中,氧化性强的是______,设计简单的实验方案证明______.
(3)含有氯元素的常见物质转化关系如图: ,A、B中氯元素化合价的代数和为0,且均是共价化合物,A为强电解质,B具有漂白性,写出A→Cl2的化学反应方程式______;C与B的组成元素相同,C中氯元素的化合价为最高价,C与H2SO4相比,酸性强的是______(填化学式).
,A、B中氯元素化合价的代数和为0,且均是共价化合物,A为强电解质,B具有漂白性,写出A→Cl2的化学反应方程式______;C与B的组成元素相同,C中氯元素的化合价为最高价,C与H2SO4相比,酸性强的是______(填化学式).
参考答案:(1)氯的核电核数为17,原子核外有3个电子层,最外层电子数为7,原子结构示意图为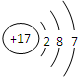 ,位于周期表第三周期、第ⅦA族,
,位于周期表第三周期、第ⅦA族,
故答案为: ;第三周期、第ⅦA族;
;第三周期、第ⅦA族;
(2)非金属性:Cl>S>P,元素的非金属性越强,对应的氢化物的稳定性越强,则稳定性由强到弱的顺序为HCl>H2S>PH3,元素的非金属性越强,单质的氧化性越强,氯、溴两种元素的单质中,氧化性强的是Cl2,可根据单质之间的置换反应证明,为取少量NaBr(HBr)溶液,向其中通入氯气,溶液变为橙色,则证明Cl2的氧化性强于Br2,
故答案为:HCl>H2S>PH3;Cl2;取少量NaBr(HBr)溶液,向其中通入氯气,溶液变为橙色,则证明Cl2的氧化性强于Br2;
(3)实验室用浓盐酸和二氧化锰在加热条件下制备氯气,反应的方程式为4HCl(浓)+MnO2△.MnCl2+Cl2↑+2H2O,B具有漂白性,应为HClO,C中氯元素的化合价为最高价,应为HClO4,为酸性最强的无机含氧酸,
故答案为:4HCl(浓)+MnO2△.MnCl2+Cl2↑+2H2O;HClO4.
本题解析:
本题难度:一般
2、选择题 通常状况下,NC13是一种油状液体,其分子空间构型与氨分子相似,下列对NC13的有关叙述正确的是( )
A.CCl4中C-C1键键长比NC13中N-C1键键长短
B.分子中的所有原子均达到8电子稳定结构
C.NCl3分子是非极性分子
D.NBr3比NCl3易挥发
参考答案:A、C原子的原子半径大于N原子的原子半径,所以CCl4中C-C1键键长比NC13中N-C1键键长,故A错误.
B、NC13中N原子最外层电子数5+化合价的绝对值3=8,所以N原子达到8电子稳定结构;NC13中C1原子最外层电子数7+化合价的绝对值1=8,所以C1原子达到8电子稳定结构,故B正确.
C、NC13的分子空间构型与氨分子相似,都是三角锥型结构,氨分子是极性分子,所以NCl3分子也是极性分子,故C错误.
D、分子晶体中物质的熔沸点与相对分子质量有关,相对分子质量越大其熔沸点越高,所以NBr3比NCl3的熔沸点高,NCl3比NBr3易挥发,故D错误.
故选B.
本题解析:
本题难度:一般
3、选择题 下列物质中既不含离子键,又不含共价键的有
[? ]
A.食盐水
B.氖气
C.氢气
D.NaOH
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列叙述中,正确的是
[? ]
A.含金属元素的离子一定都是阳离子
B.在氧化还原反应中,非金属单质一定是氧化剂
C.某元素从化合态变为游离态,该元素一定被氧化
D.金属阳离子被还原不一定得到金属单质
参考答案:D
本题解析:
本题难度:简单
5、选择题 键能是破坏1mol化学键吸收的热量或者生成1mol化学键放出的热量,解释下列物质性质的变化规律与物质结构间的因果关系时,与键能无关的变化规律是①HF、HCl、HBr、HI的热稳定性依次减弱②NH3易液化③F2、C12、Br2、I2的熔、沸点逐渐升高?④H2S的熔沸点小于H2O的熔沸点?⑤NaF、NaCl、NaBr、NaI的熔点依次减低( )
A.②③④
B.③④⑤
C.②③④⑤
D.全部
参考答案:A
本题解析:
本题难度:一般