微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 (12 分)揖选做题铱本题包括A、B 两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A 小题评分。
A. [物质结构与性质]
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为?。
②NO3- 的空间构型是?(用文字描述)。
(2)在铜锰氧化物的催化下,CO 被氧化为CO2,HCHO 被氧化为CO2和H2O。
①根据等电子体原理,CO 分子的结构式为?。
②H2O 分子中O 原子轨道的杂化类型为?。
③1 mol CO2中含有的σ键数目为?。
(3) 向CuSO4溶液中加入过量NaOH 溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为?。
参考答案:
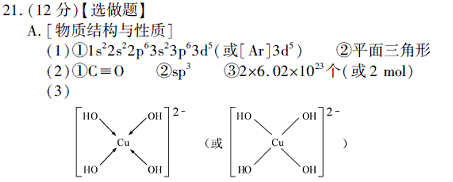
本题解析:(1)Mn原子序数为25,价电子排布为3d54s2,先失去4s上二个电子,即得Mn2+。NO3- 离子中氮原子无孤对电子,配位原子为3,则N采用sp2杂化,所以NO3- 的空间构型为平面三角形。(2)CO与N2互为等电子体,根据氮分子的结构式可以写出CO的结构式为C≡O。H2O中O原子存在两对孤对电子,配位原子为2,价电子对为4,所以O原子采用sp3杂化。二氧化碳分子内含有碳氧双键,双键中有一个为?键,一个为?键,则1molCO2中含有2mol?键。(3)Cu2+中存在空轨道,而OH-中O原子上面有孤对电子,故O与Cu之间以配位键结合。
【考点定位】电子排布式,空间构型,杂化方式,化学键的数法以及配位键的表示
本题难度:一般
2、选择题 关于离子键、共价键的各种叙述中,下列说法中正确的是
[? ]
A.在离子化合物里,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如Cl2)中
C.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键
D.由不同元素组成的含多个原子的分子里,一定只存在极性键
参考答案:C
本题解析:
本题难度:简单
3、填空题 铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第IB 族。Cu2+的核外电子排布式为________。
(2)下图是铜的某种氧化物的晶胞结构示意图,可确定该品胞中阴离子的个数为_____________。
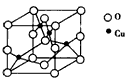
(3)胆矾CuSO4・5H2O可写成[Cu(H2O)4]SO4・H2O,其结构示意图如喜爱图所示:

下列说法正确的是_______(填字母)。
A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+ 配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是____________________________。
(5)Cu2O的熔点比Cu2S的________(填“高”或“低”),请解释原因___________________________。
参考答案:(1)[Ar]3d9或1s22s22p63s23p63d9
(2)4个
(3)BD
(4)F的电负性比N大,N-F成键电子对向F偏移,导致NF3中N原子核对其孤对电子的吸引能力增强,难以形成配位键,故NF3不易与Cu2+形成配离子
(5)高;Cu2O与Cu2S相比,阳离子相同,阴离子所带的电荷数也相同,但O2-半径比S2-半径小,所以Cu2O的晶格能更大,熔点更高
本题解析:
本题难度:一般
4、选择题 已知X、Y、Z、W四种短周期元素(均非稀有气体元素)在周期表中的相对位置如右图所示,下列说法正确的是( )
A.Z元素的原子半径可能比Y元素的小
B.Z元素的最高化合价可能比Y元素的高
C.W形成的单质的熔点一定高于Y
D.Z的最高价氧化物的水化物的酸性一定比W的强
