微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某密闭容器中有如下可逆反应:2SO2(g)+O2(g)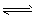 2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。
2SO3(g),(正反应是放热反应),达到平衡后,其它条件不变时,只改变下列的某一个条件,将变化的情况(增大、减小、不变)填入空格中。
(1)升高温度,v(正)___________,v(逆)___________,SO2 的转化率_____________。
(2)加正催化剂,v(正)___________,v(逆)___________,O2 的物质的量___________。
(3)缩小容器的体积,SO3的物质的量___________,SO2的转化率______________。
2、选择题 有X、Y、Z三种物质.常温下分别用Y或Z与X混合时,反应速率几乎相同的是( )
| 选项 | X | Y | Z
①
2mL?5%H2O2?溶液
1mL?1mol?L-1CuSO4溶液
1mL?1mol?L-1FeCl3溶液
②
1mL?1mol?L-1?NaHCO3溶液
1mL?1mol?L-1?HCl溶液
1mL?0.5mol?L-1?H2SO4溶液
③
钠块
10mL?乙醇
10mL?水
④
经过酸洗除锈的铁钉
5mL?海水
5mL?蒸馏水
|
A.①
B.②
C.③
D.④
3、填空题 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用
kJ・mol-1表示。请认真观察下图,然后回答问题。
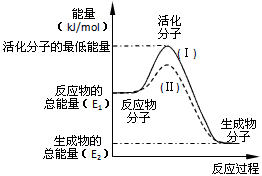
(1)图中所示反应是________(填“吸热”或“放热”)反应,该反应_______(填“需要”或“不需要”)加热,该反应的△H =________ (用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+O2(g) = H2O(g) △H = - 241.8 kJ・mol-1,该反应的活化能为
167.2 kJ・mol-1,则其逆反应的活化能为____________________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子百分数增多,反应速率加快,你认为最可能的原因是_________________________。
4、选择题 实验室用锌粒与VmL浓度为10%的稀硫酸反应制取氢气,若向反应混合物中加入下列物质,关于反应速率v说法正确的是
A.少量Na2SO4固体,v(H2)减小
B.VmLBaCl2溶液,v(H2)不变
C.加入细小的碳粒,v(H2)增大
D.加入NH4HSO4固体,v(H2)不变
5、选择题 用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g) CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法中正确的是( )
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法中正确的是( )
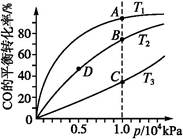
A.温度:T1>T2>T3
B.正反应速率:v(A)>v(C) v(B)>v(D)
C.平衡常数:K(A)>K(C) K(B)=K(D)
D.平均摩尔质量:M(A)<M(C) M(B)>M(D)