��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��д��ȷ����
[? ]
A.̼������Һ��������ϡ������CO32- +2H+ = CO2��+ H2O
B.������Һ�м����ռ���ҺH++OH- = H2O
C.����þ��Һ�м����Ȼ�����ҺBa2++SO42- = BaSO4��
D.����������Һ�м���ϡ������ҺBa2++OH- + H++SO42- = BaSO4�� + H2O
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��д����ȷ����?��?��
A���������ۼ���ϡ�����У�3Fe��8H����2NO3��=3Fe2����2NO����4H2O
B��Ca��HCO3��2��Һ�����Ca��OH��2��Һ��Ӧ��Ca2����HCO3����OH��=CaCO3����H2O
C��NH4HCO3��Һ����Ba��OH��2��Һ����:2HCO3һ��2OH����Ba2��=BaCO3����CO32����2H2O
D��Na2S��Һ��ͨ������H2S��S2һ��H2S=2HS��
�ο��𰸣�AC
�����������
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ����д��ȷ���ǣ�������
A��SiO2��NaOH��Һ��Ӧ��SiO2+2Na++2OH-=Na2SiO3+H2O
B��Ũ�ռ���Һ�м�����Ƭ��2Al+2OH-+2H2O=2AlO2-+3H2��
C������ϡ���ᷴӦ��Fe+2H+=Fe2++H2��
D��Cl2ͨ��ˮ�У�Cl2+H2O=2H++Cl-+ClO-
�ο��𰸣�A��SiO2��NaOH��Һ��Ӧ��SiO2+2OH-=SiO32-+H2O����A����
B�������ռӦ��ʵ���ǣ�2Al+2OH-+2H2O=2AlO2-+3H2������B��ȷ��
C��ϡ���������������Ӧ�����ӷ���ʽΪ3Fe+8H++2NO3-�T3Fe2++2NO��+4H2O����C����
D��HClOΪ������ʣ�Ӧд�ɻ�ѧʽ����ȷ��д��Ϊ��Cl2+H2O=Cl-+HClO-+H+����D����
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ����˵����ȷ���ǣ�?��
A��þ�뼫ϡ���ᷴӦ��������淋����ӷ���ʽΪ:4Mg+6H++N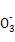 =4Mg2++N
=4Mg2++N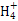 +3H2O
+3H2O
B��������,0.1 mol/LһԪ��HA��Һ��c(OH-)/c(H+)=1��10-8,�����Һ��pH=3
C����ͬ������,Ũ�Ⱦ�Ϊ0.01 mol/L��NH4Cl��Һ��NaCl��Һ��,ǰ�ߵ���������Ũ�ȴ��ں��ߵ���������Ũ��
D�����ʵ���Ũ����ȵĴ��������������Һ�������Ϻ����Һ��:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)+c(CH3COOH)
�ο��𰸣�B
���������A���ɡ�ԭ�Ӳ��غ�,ӦΪ4Mg+10H++N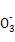 =4Mg2++N
=4Mg2++N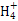 +3H2O,����;c(OH-)/c(H+)=1��10-8��c(OH-)��c(H+)=1��10-14����,�ɵ�c(H+)=1��10-3 mol��L-1,��pH=3,B��;������Һ������,NH4Cl��Һ�д���c(N
+3H2O,����;c(OH-)/c(H+)=1��10-8��c(OH-)��c(H+)=1��10-14����,�ɵ�c(H+)=1��10-3 mol��L-1,��pH=3,B��;������Һ������,NH4Cl��Һ�д���c(N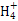 )+c(H+)=c(Cl-)+c(OH-),NaCl��Һ�д���c(Na+)+c(H+)=c(Cl-)+c(OH-),����NH4Cl��Һ�����Զ�NaCl��Һ������,��ǰ�ߵ�c(OH-)С�ں���,��c(Cl-)��Ϊ0.01 mol/L,��c(N
)+c(H+)=c(Cl-)+c(OH-),NaCl��Һ�д���c(Na+)+c(H+)=c(Cl-)+c(OH-),����NH4Cl��Һ�����Զ�NaCl��Һ������,��ǰ�ߵ�c(OH-)С�ں���,��c(Cl-)��Ϊ0.01 mol/L,��c(N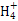 )+c(H+)��c(Na+)+c(H+),C��;������Һ������,CH3COONa��Һ�д���c(Na+)+c(H+)=c(CH3COO-)+c(OH-),D����
)+c(H+)��c(Na+)+c(H+),C��;������Һ������,CH3COONa��Һ�д���c(Na+)+c(H+)=c(CH3COO-)+c(OH-),D����
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��ʾ������ǣ�������
A������������ʵ���Ũ�ȵ�NaHCO3��Ba��OH��2����Һ��ϣ�
HCO3-+Ba2++OH-�TBaCO3��+H2O
B��Fe2O3���ڹ����������Һ�У�
Fe2O3+6H++2I-�T2Fe2++I2+3H2O
C��ͭƬ����ϡ�����У�
3Cu+2NO3-+8H+�T3Cu2++2NO��+4H2O
D�����Ȼ���Ũ��Һ�����ˮ�У���ȡ�����������壺
Fe3++3H2O=Fe��OH��3��+3H+
�ο��𰸣�A�������ʵ�����NaHCO3��Ba��OH��2����Һ��ϣ�̼���������������������1��1��Ӧ�����ɵ�̼��������ܺͱ����ӷ�Ӧ����HCO3-+Ba2++OH-�TBaCO3��+H2O����A��ȷ��
B���������Һ�������Ժͻ�ԭ�ԣ��ܽ��������ܽ⣬���ܽ����ɵ���������ԭ����B��ȷ��
C��ͭ��ϡ�����ܷ�Ӧ��������һ������������ѭ����غ㼰�����غ㶨�ɣ���C��ȷ��
D����ȡ������������ķ�ӦΪ��Fe3++3H2O?��?.?Fe��OH��3�����壩+3H+����D����
��ѡD��
���������
�����Ѷȣ�һ��