|
高中化学知识点总结《反应速率与平衡的有关计算》高频试题巩固(2017年最新版)(十)
2017-07-27 08:20:00
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 (14分)工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g) CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号)__________
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
| (2)下表所列数据是反应在不同温度下的化学平衡常数(K)
温度
| 250℃
| 300℃
| 350℃
| K
| 2.041
| 0.270
| 0.012
|
?
①该反应化学平衡常数表达式K=?
②由表中数据判断该反应的△H__________0(填“>”、“=”或“<”);
③某温度下,将2molCO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得C(CO)=0.2mol・L-1,此时的温度为__________
(3)25℃101KPa下,1g液态甲醇完全燃烧生成CO2和液态水时放出热量22.68kJ,表示甲醇燃烧热的热化学方程式为?
(4)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,该电池工作时负极电极反应式为?。若反应时消耗16g甲醇所产生的电能电解足量的CuSO4溶液,则将产生标准状况下的O2________升
参考答案:⑴C、 D;⑵①K=c(CH3OH)/c(CO)・c2(H2) ; ②△H<0;③250℃
⑶ CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)?ΔH=-725.76 kJ / mol
⑷ 负极CH3OH -6e-+8OH-=CO32-+6H2O ; 产生标准状况下的O216.8升
本题解析:A. CH3OH是生成物,而CO是反应物,在任何时刻都存在生成CH3OH的速率与消耗CO的速率相等,因此不能作为判断平衡的标志。错误。B. 由于反应是在体积固定的密闭容器中进行,反应前后遵循质量守恒定律,所以在无论反应是否达到平衡,混合气体的密度都不变。因此不能作为判断平衡的标志。错误。C. 由于该反应是个反应前后气体体积不等的可逆反应,若未达到平衡,气体的物质的量就要发生变化,则气体的密度也要发生变化,即混合气体的相对平均分子质量也要发生变化。因此混合气体的相对平均分子质量不变。可以作为判断反应达到平衡的标志。正确。D. 若反应达到平衡,反应混合物中CH3OH、CO、H2的任何一个组分的消耗浓度与产生浓度相等,即浓度都不再发生变化。因此可以作为判断反应达到平衡的标志。正确。⑵ ①化学平衡常数是可能反应达到平衡状态时各生成物浓度幂指数的乘积与各反应物浓度幂指数的乘积的比。所以 。②由表中数据可知:升高温度,化学平衡常数减小。说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度化学平衡向吸热反应方向移动。逆反应方向为吸热反应方向,所以该反应的正反应为放热反应,△H<0。③CO(g)+2H2(g) 。②由表中数据可知:升高温度,化学平衡常数减小。说明升高温度,化学平衡逆向移动。根据平衡移动原理:升高温度化学平衡向吸热反应方向移动。逆反应方向为吸热反应方向,所以该反应的正反应为放热反应,△H<0。③CO(g)+2H2(g) CH3OH(g)在反应开始时c(CO)=1mol/L;c(H2)=3mol/L;c(CH3OH)=0mol/L;当反应达到平衡时,C(CO)=0.2mol/L,所以根据方程式中各种物质的关系可知c(H2)=1.4mol/L;c(CH3OH)= 0.8mol/L化学平衡常数 CH3OH(g)在反应开始时c(CO)=1mol/L;c(H2)=3mol/L;c(CH3OH)=0mol/L;当反应达到平衡时,C(CO)=0.2mol/L,所以根据方程式中各种物质的关系可知c(H2)=1.4mol/L;c(CH3OH)= 0.8mol/L化学平衡常数 所以反应温度为250℃。(3)燃烧热是1mol的物质完全燃烧产生稳定的氧化物时放出的热量。根据题目提供的数据可知:表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)? ΔH=-725.76 kJ / mol;(4)在燃料电池中,通入燃料的电极为负极,通入氧气的电极为正极。由于电解质为碱性,所以在负极的电极反应式为CH3OH -6e-+8OH-=CO32-+6H2O。n(CH3OH)=16g÷32g/mol=0.5mol.所以n(e-)=0.5mol×6=3mol.根据电子守恒可得n(O2)=3mol÷4=0.75mol,V(O2)= 0.75mol×22.4L/mol=16.8L。 所以反应温度为250℃。(3)燃烧热是1mol的物质完全燃烧产生稳定的氧化物时放出的热量。根据题目提供的数据可知:表示甲醇燃烧热的热化学方程式为CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)? ΔH=-725.76 kJ / mol;(4)在燃料电池中,通入燃料的电极为负极,通入氧气的电极为正极。由于电解质为碱性,所以在负极的电极反应式为CH3OH -6e-+8OH-=CO32-+6H2O。n(CH3OH)=16g÷32g/mol=0.5mol.所以n(e-)=0.5mol×6=3mol.根据电子守恒可得n(O2)=3mol÷4=0.75mol,V(O2)= 0.75mol×22.4L/mol=16.8L。
本题难度:一般
2、选择题 已知:H2(g) +I2(g)  2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的 2HI(g) ΔH =" -14.9" kJ/mol。在甲、乙两个体积相同密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)="0.008" mol/L。 下列判断正确的
起始浓度
| c(H2) / mol/L
| c(I2) / mol/L
| c(HI) / mol/L
| 甲
| 0.01
| 0.01
| 0
| 乙
| 0.02
| 0.02
| 0
|
?
A.平衡时,乙中H2的转化率是甲中的2倍?
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等?
D.该温度下,反应的平衡常数K=0.25
参考答案:D
本题解析:A、该反应前后气体的体积不变,乙中的浓度为甲中的2倍,乙中压强为甲中2倍,压强不影响平衡移动,二者为等效平衡,平衡时对应各组分的转化率相同,错误;B、二者为等效平衡,平衡时乙中c(I2)是甲中的2倍,平衡时乙中颜色更深,错误;C、二者为等效平衡,反应物转化率相同,乙中参加反应I2的是甲中的2倍,乙中的热量变化是甲中的2倍,错误;D、平衡时氢气的浓度为0.008mol/L,则:
H2(g)+I2(g)?2HI(g)△
开始(mol/L):0.01?0.01?0
变化(mol/L):0.002? 0.002? 0.004
平衡(mol/L):0.008? 0.008? 0.004
故该温度下该反应的平衡常数k=0.0042×(0.008×0.008)=0.25,正确。
本题难度:一般
3、填空题 (20分)在一容积为2 L的密闭容器内加入0.2 mol 的N2和0.6 mol 的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图: 2NH3(g) △H<0,反应中NH3的物质的量浓度的变化的情况如右图:

(1)根据右图,计算从反应开始到平衡时,平均反应速率v(NH3)为____?_。
(2)该反应的化学平衡常数表达式K=_____?。
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________。
a. 0.20 mol/L? b. 0.12 mol/L? c. 0.10 mol/L? d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡_________________________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________________(填“增大”、“减小”或“不变”)。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
参考答案: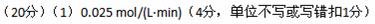

本题解析:略
本题难度:一般
4、选择题 某温度下,反应X(g)+3Y(g) 2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下: 2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下:
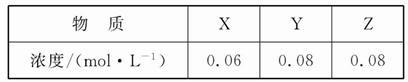
下列说法正确的是(? )
A.此时v(正)<v(逆)
B.平衡时Y的浓度为0.05 mol・L-1
C.平衡时X的转化率为40%
D.增大压强使平衡向正反应方向移动,平衡常数增大
参考答案:B
本题解析:根据Qc=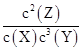 ?=0.082/(0.06×0.083)=208.3<1 600,反应没有达到平衡,向正反应方向移动,v(正)>v(逆),A错;若达到平衡时Y的浓度为0.05 mol・L-1,则Y在上面某时刻浓度的基础上又反应了0.03 mol・L-1,所以X、Y、Z的平衡浓度分别为0.05 mol・L-1、0.05 mol・L-1、0.1 mol・L-1,所以此时的Qc=0.12/(0.05×0.053)="1" 600,与此温度下的平衡常数数值相等,所以此时达到平衡状态, B对;根据表中数据可知起始时刻X、Y的浓度分别为0.1 mol・L-1、0.2 mol・L-1,达到平衡时X的浓度为0.05 mol・L-1,所以X的转化率为0.05 mol・L-1/0.1 mol・L-1×100%=50%,C错;增大压强,平衡正向移动,但是平衡常数不变,D错 ?=0.082/(0.06×0.083)=208.3<1 600,反应没有达到平衡,向正反应方向移动,v(正)>v(逆),A错;若达到平衡时Y的浓度为0.05 mol・L-1,则Y在上面某时刻浓度的基础上又反应了0.03 mol・L-1,所以X、Y、Z的平衡浓度分别为0.05 mol・L-1、0.05 mol・L-1、0.1 mol・L-1,所以此时的Qc=0.12/(0.05×0.053)="1" 600,与此温度下的平衡常数数值相等,所以此时达到平衡状态, B对;根据表中数据可知起始时刻X、Y的浓度分别为0.1 mol・L-1、0.2 mol・L-1,达到平衡时X的浓度为0.05 mol・L-1,所以X的转化率为0.05 mol・L-1/0.1 mol・L-1×100%=50%,C错;增大压强,平衡正向移动,但是平衡常数不变,D错
本题难度:一般
5、选择题 已知某物质颜色的强度与该物质的浓度成正比、与观察者的视程中的物质厚度成正比。在注射器中,存在NO2与N2O4的混合物,气体呈棕色,现将注射器的针筒慢慢往外拉,保持温度不变,此时混合物的颜色为

A.从针筒的顶端方向观察,气体颜色变深
B.从针筒的顶端方向观察,气体颜色变浅
C.从针筒的垂直方向观察,气体颜色没有变化
D.从针筒的垂直方向观察,气体颜色变深
参考答案:A
本题解析:NO2为红棕色气体,N2O4无色
对于可逆反应2NO2 N2O4,向外拉针筒时,相当于减压,平衡逆向移动,生成更多的NO2(但两物质的浓度是减小的)。 N2O4,向外拉针筒时,相当于减压,平衡逆向移动,生成更多的NO2(但两物质的浓度是减小的)。
故从针筒的顶端方向观察,NO2的浓度减小,但厚度增大,总体来说,气体颜色加深;但从针筒的垂直方向观察,NO2的浓度减小,厚度不变,气体的颜色变浅,答案为A
本题难度:一般
|