微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)甲醇是一种可再生能源,具有广泛的开发和应用前景。请回答:
(1)工业上合成甲醇CO(g) + 2H2(g)? ?CH3OH(g)? ΔH,在不同温度下的化学平衡常数(K)如表所示。
?CH3OH(g)? ΔH,在不同温度下的化学平衡常数(K)如表所示。
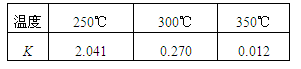
①根据表中数据可判断ΔH?(填“>” 或 “=” 或 “<”)0。?
②300℃时,向容积为1L的密闭容器中充入2 mol CO、3 mol H2和2 mol CH3OH,此时反应将?。
A.向正方向移动?B.向逆方向移动?C.处于平衡状态?
(2)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(l)? ΔH= -a? kJ・mol-1
②2CO (g)+ O2(g) = 2CO2(g)?ΔH= -b kJ・mol-1
写出该条件下甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
???。
(3)改变下列条件,能同时加快正反应的速率,增大CO的转化率的是?
A.使用催化剂?B.缩小容器体积
C.降低温度?D.分离CH3OH的物质的量
(4)以甲醇、氧气为原料,KOH溶液作为电解质溶液构成燃料电池总反应为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,则负极的电极反应式为????。
参考答案:(10分)(1)①<?②A
(2)CH3OH(l) + O2(g) = CO(g) + 2H2O(l)?ΔH= -(a―b)/2? kJ・mol-1
(3)B?(4)CH3OH ― 6 e- + 8OH― = CO32― + 6 H2O
本题解析:(1)随着温度的升高,平衡常数逐渐减小。这说明升高温度,破坏向逆反应方向移动,所以正方应是放热反应,即△H小于0。
(2)根据盖斯定律可知(①-②)÷2即得到反应CH3OH(l) + O2(g) = CO(g) + 2H2O(l),所以该反应的反应热△H= -(a―b)/2? kJ・mol-1。
(3)催化剂并能改变平衡状态,A不正确;缩小容器体积,增大压强,反应速率加快,平衡向正反应方向移动,增大CO的转化率,B正确;降低温度,反应速率降低,C不正确;分离CH3OH的物质的量,反应速率也是降低的,不正确,答案选B。
(4)根据反应式可知,甲醇失去电子,在负极通入,所以负极的电极反应式是CH3OH-6 e- + 8OH― = CO32― + 6 H2O。
点评:该题是中等难度的试题,也是高考中的常见题型。该题综合性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练。有助于培养学生的逻辑思维能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。该题的关键是明确原电池的工作原理,以及外界条件对平衡状态的影响,然后结合题意灵活运用即可。
本题难度:一般
2、选择题 将等物质的量的A、B混合于2?L的密闭容器中,发生下列反应:3A(g)+B(g) xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol・L-1・min-1,下列说法正确的是
xC(g)+2D(g),经4min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.125mol・L-1・min-1,下列说法正确的是
[? ]
A.以B表示的平均反应速率为v(B)=0.13?mol・L-1・min-1
B.该反应方程式中,x=2?
C.4min时,A的物质的量为0.75mol
D.4min时,A的转化率为50%
参考答案:BD
本题解析:
本题难度:一般
3、选择题 工业上常用还原沉淀法处理含铬废水(Cr2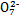 和Cr
和Cr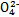 ),其流程为:Cr
),其流程为:Cr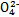
 Cr2
Cr2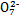
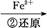 Cr3+
Cr3+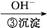 Cr(OH)3↓
Cr(OH)3↓
已知:
(1)步骤①中存在平衡:2Cr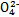 (黄色)+2H+
(黄色)+2H+ Cr2
Cr2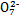 (橙色)+H2O
(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol・L-1时可视作该离子不存在
下列有关说法中正确的是( )
A.步骤①中加酸,将溶液的pH调节至2,溶液显黄色,Cr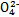 浓度增大
浓度增大
B.步骤①中当2v(Cr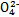 )=v(Cr2
)=v(Cr2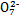 )时,说明反应2Cr
)时,说明反应2Cr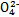 (黄色)+2H+
(黄色)+2H+ Cr2
Cr2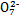 (橙色)+H2O达到平衡状态
(橙色)+H2O达到平衡状态
C.步骤②中,若要还原1 mol Cr2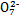 ,需要12 mol (NH4)2Fe(SO4)2・6H2O
,需要12 mol (NH4)2Fe(SO4)2・6H2O
D.步骤③中,当将溶液的pH调节至6时,则可认为废水中的铬已除尽
参考答案:D
本题解析:由(1)可知A选项错误;B选项不能判断正、逆反应速率,错误;C选项,1 mol Cr2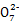 得到6 mol电子,还原1 mol Cr2
得到6 mol电子,还原1 mol Cr2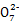 需要6 mol Fe2+,错误;D选项,c(OH-)=10-8 mol・L-1,由Ksp=10-32可得c(Cr3+)=10-8 mol・L-1,正确
需要6 mol Fe2+,错误;D选项,c(OH-)=10-8 mol・L-1,由Ksp=10-32可得c(Cr3+)=10-8 mol・L-1,正确
本题难度:一般
4、选择题 PCl5(气)  PCl3(气) +Cl2(气) △H>0 当反应达到平衡时,下列措施:①降温②恒容通入惰性气体③增加Cl2的浓度④加压⑤加催化剂⑥恒压通入惰性气体,能提高PCl5质量分数的是
PCl3(气) +Cl2(气) △H>0 当反应达到平衡时,下列措施:①降温②恒容通入惰性气体③增加Cl2的浓度④加压⑤加催化剂⑥恒压通入惰性气体,能提高PCl5质量分数的是
A.①②④
B.①③④
C.②③⑥
D.③⑤⑥
参考答案:B
本题解析:PCl5(气)  PCl3(气) +Cl2(气) △H>0提高PCl5质量分数,平衡正向移动;
PCl3(气) +Cl2(气) △H>0提高PCl5质量分数,平衡正向移动;
①降温,平衡向着放热反应方向移动,向逆向移动;②恒容通入惰性气体,各物质浓度不变,化学反应速率不变,化学平衡不移动;③增加Cl2的浓度,平衡逆向移动;④加压,平衡向着体积减小的方向移动,向逆向移动;⑤加催化剂,同等改变正逆化学反应速率,平衡不动;⑥恒压通入惰性气体,体积变大,相当于减压,平衡向着体积增大的方向移动,向着正向移动。
本题难度:简单
5、选择题 下列事实,不能用平衡移动原理解释的是
A.红棕色的NO2,加压后颜色先变深后变浅
B.将FeS固体投入到含有Cu2+的废水中以除去Cu2+
C.选择合适的催化剂可使水在较低温度下分解
D.滴有酚酞的Na2CO3溶液,加热后颜色变深
参考答案:C
本题解析:A可以,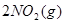 ?
?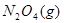 加压,二氧化氮浓度增大,即颜色加深,同时,由于增大压强,平衡将向正反应方向移动,颜色将变浅;B可以,FeS在溶液中存在如下可逆过程:
加压,二氧化氮浓度增大,即颜色加深,同时,由于增大压强,平衡将向正反应方向移动,颜色将变浅;B可以,FeS在溶液中存在如下可逆过程: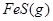 ?
?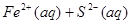 投入Cu2+的废水中,Cu2+能与S2―反应生成更难溶于水的沉淀,从而破坏FeS的溶解平衡;C不能,催化剂不影响平衡的移动,只能改变反应速率;D可以,Na2CO3溶液存在如下水解平衡:
投入Cu2+的废水中,Cu2+能与S2―反应生成更难溶于水的沉淀,从而破坏FeS的溶解平衡;C不能,催化剂不影响平衡的移动,只能改变反应速率;D可以,Na2CO3溶液存在如下水解平衡: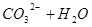 ?
?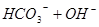 ,加热,平衡将向右移动,溶液碱性加强,即滴有酚酞的Na2CO3溶液,加热后颜色变深;
,加热,平衡将向右移动,溶液碱性加强,即滴有酚酞的Na2CO3溶液,加热后颜色变深;
本题难度:一般