微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法中可以证明反应H2(g)+I2(g)  2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是
①单位时间内生成n mol H2的同时生成n mol HI ②一个H―H键断裂的同时有两个H―I键断裂 ③百分含量w(HI)=w(I2) ④反应速率v(H2)=v(I2)=v(HI) ⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1 ⑥温度和体积一定时,生成物浓度不再变化 ⑦温度和体积一定时,容器内的压强不再变化 ⑧条件一定时,混合气体的平均相对分子质量不再变化 ⑨温度和体积一定时,混合气体颜色不再变化 ⑩温度和压强一定时,混合气体的密度不再变化
A.①②③④
B.②⑥⑨
C.②⑥⑨⑩
D.③⑤⑥⑦⑧
2、填空题 (9分)在一定温度下, 把2molN2和6molH2通入体积不变的容器中。容器中发生以下反应: N2(g) + 3H2(g)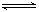 2NH3(g) ,△H= ―QKJ/mol。若反应达平衡后, 测得混合气体为7mol。据此回答下列问题:
2NH3(g) ,△H= ―QKJ/mol。若反应达平衡后, 测得混合气体为7mol。据此回答下列问题:
保持上述反应温度不变, 设a.b.c分别代表起始加入的N2.H2和NH3的物质的量。如果反应达平衡后混合气体中各物质的百分含量仍与上述平衡时完全相同, 那么:
(1)若a = 1.c =" 2," 则b =?。在此情况下, 反应起始时将向?方向进行(填“正”或“逆”)。
(2)若需规定起始时反应向逆方向进行,则c的范围是?。
3、填空题&nbs p; 在真空密闭容器中加入amol PH4I固体,在一定温度下发生反应:
PH4I(s)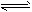 PH3(g)+HI(g)
PH3(g)+HI(g)
4PH3(g)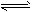 P4(S)+6H2(g)
P4(S)+6H2(g)
2HI(g)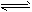 H2(g)+I2(g)
H2(g)+I2(g)
以上三个反应建立平衡后,测得HI为bmol,I2(g)为cmol,H2为dmol。求:
(1)平衡后,容器内P4(g)和PH3(g)的物质的量(用a,b,c,d表示) n(P4)=___________,
n(PH3)=______________。
(2)a,b,c三者的关系服从a>________(填b,c的代数式)。
(3)平衡后,增大压强容器内n(I2)________,n(PH4I)_________。(填增大、减小、不变)
4、计算题 在2 L密闭容器中,充入1 mol N2和3mol H2,恒温恒容条件下发生合成氨反应,2 min时达到平衡。测得平衡时N2的转化率为40%,求:
(1)用H2表示2min内该反应的平均反应速率
(2)NH3的平衡浓度
(3)H2在平衡混合气体中的体积分数
(4)平衡时容器的压强P平与起始时压强P始之比
5、填空题 (12分)现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高。
(1)已知1 mol N2(g)与适量H2(g)完全反应,当生成NH3(g)0.1mol时,放出9.22kJ热量,写出反应的热化学方程式:?。
(2)若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1?K2(填“>”? “="”" 或 “<” )。
(3)在一定温度下,向容积不变(始终为10L)的密闭容器中加入2 mol N2、8 mol H2 及固体催化剂。10分钟后反应达到平衡状态,容器内气体压强变为起始的80%,此时氨气的体积分数为?,用氮气表示的反应速率:?。若想提高氨气的产率,根据化学平衡移动原理,请提出合理的建议:?(任意写一条)。
(4)在上述相同条件下,若起始时加入4 mol NH3、2 mol H2及固体催化剂,反应达到平衡时NH3的体积分数比(3)中?(填“大”、“小”或“相等”)。
(5)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如右图)。在电解法合成氨的电解池中?(填“能”或“不能”) 用水作电解质溶液的溶剂,原因是?。
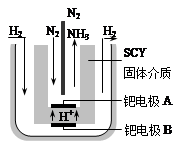
钯电极A是电解池的?极(填“阳”或“阴”),该极上的电极反应式是?。