微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定条件下,可逆反应X(g)+2Y(g) 2Z(g)达到平衡时,有50%的Y转化为Z,且X的转化率为25%,则起始时充入容器中的X和Y物质的量之比为
2Z(g)达到平衡时,有50%的Y转化为Z,且X的转化率为25%,则起始时充入容器中的X和Y物质的量之比为
A.2:1
B.1:1
C.2:3
D.3:2
参考答案:B
本题解析:假设起始的X和Y分别为x、ymol,反应X为amol,Y为2amol;有a/x=25%;2a/y=50%;故x:y=1:1。
本题难度:简单
2、填空题 在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力如图1-14-1所示,请回答:
(1)“0”点导电能力为0的理由______。
(2)a,b,c三点溶液的pH值由小到大的顺序为______。
(3)a,b,c三点中电离度最大的是:______。
(4)若使c点溶液中[CH3COO-]增大,溶液的pH值也增大,可采取的措施为:
①______;②______;③______。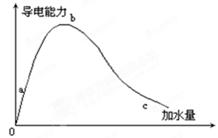
参考答案:(1)由于醋酸为共价化合物,在固、液态时不存在离子,也就谈不上存在自由移动的离子,所以不导电。
(2)b<a<c;(3)c;(4)加NaOH(固);Mg;Na2CO3(固)。
本题解析:
【错解分析】错答 (1)由于冰醋酸为固态,所以不导电。
(2)c<b<a;(3)b;(4)加热。
【正解】冰醋酸不导电,从表面上看是由于其状态原因造成。其实质是本身结构为共价化合物,不存在离子,也不存在自由移动的离子,因此不导电。
从导电能力上看,在b点醋酸的导电能力最强,说明溶液中自由移动离子浓度最大,其离子应为醋酸电离的氢离子和醋酸根离子,相应在a点、c点的氢离子浓度逐渐减小。由于思维定势误将该顺序视为pH值由小到大的顺序,pH值是氢离子浓度的负对数值,恰好与氢离子浓度大小顺序相反,因此结论为b<a<c。
为了使醋酸根离子浓度增大,而溶液的pH值也增大,只能是减小氢离子浓度,使电离平衡向右移动。采取的措施可以添加较活泼的金属、金属氧化物、碱和比醋酸弱的盐。本小题的误区是:加热促进醋酸的电离,醋酸根离子浓度增大,氢离子浓度也增大,与上小题同样的错误,pH值也增大。
本题难度:简单
3、选择题 将2mol SO2和1mol O2充入一容积固定的密闭容器中,在一定条件下反应:2SO2(g)+O2(g)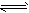 2SO3(g),下列哪些情况能说明该可逆反应已达化学平衡状态的是
2SO3(g),下列哪些情况能说明该可逆反应已达化学平衡状态的是
[? ]
A.每生成2mol SO2的同时,消耗2mol SO3
B.混合气体的质量不再变化
C.每生成2mol SO3的同时,消耗2mol SO3
D.每生成2mol SO3的同时,消耗1mol O2
参考答案:C
本题解析:
本题难度:一般
4、填空题 用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)
?Si3N4(s)+12HCl(g)△H=-Q(Q>0)
完成下列填空:
(1)在一定温度下进行上述反应,若反应容器的容积为2L,3min后达到平衡,测得固体的质量增加了2.80g,则H2的平均反应速率______?mol/(L?min);该反应的平衡常数表达式K=______
(2)上述反应达到平衡后,下列说法正确的是______.
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si3N4物质的量平衡向左移动
d.其他条件不变,增大HCl物质的量平衡向左移动
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_______
a.3v逆(N2)=v正(H2)?b.v正(HCl)=4v正(SiCl4)?c.混合气体密度保持不变
d.c(N2):c(H2):c(HCl)=1:3:6.
参考答案:(1)固体的质量增加了2.80g,n(Si3N4)=2.80g140g/mol=0.02mol,则参加反应的氢气为6×0.02mol=0.12mol,则用氢气表示的反应速率为0.12mol2L3min=0.02mol/(L.min),
平衡常数K=c12(HCl)c3(SiCl4)c2(N2)c6(H2),故答案为:0.02mol/(L.min);c12(HCl)c3(SiCl4)c2(N2)c6(H2);
(2)该反应为放热反应,气体体积增大的反应,则
a.其他条件不变,压强增大,平衡逆向移动,K减小,故a正确;
b.其他条件不变,温度升高,平衡逆向移动,K减小,故b正确;
c.其他条件不变,增大Si3N4物质的量,平衡不移动,故c错误;
d.其他条件不变,增大HCl物质的量平衡向左移动,故d正确;
故答案为:abd;
(3)a.由反应速率之比等于化学计量数之比,则3v正(N2)=v正(H2),则3v逆(N2)=v正(H2),所以v逆(N2)=v正(N2),则达到平衡,故a正确;?
b.v正(HCl)=4v正(SiCl4),不能确定正逆反应速率的关系,故b错误;?
c.因体积不变,气体的质量在变化,则混合气体密度保持不变时反应达到平衡,故c正确;
d.c(N2):c(H2):c(HCl)=1:3:6,取决于反应物的起始量及转化程度,不能确定反应是否平衡,故d错误;
故答案为:ac.
本题解析:
本题难度:一般
5、选择题 对于以下反应:A(s)+3B(g)?2C(g)+D(g),在一定温度、压强下,在一体积可变的容器中,当下列物理量不再发生变化时就可确定一定达到平衡状态的是( )
A.容器的体积不再变化
B.B的生成速率和D的反应速率为3:1
C.混合气体的密度不随时间变化
D.B、C、D的分子数之比为3:2:1
参考答案:A.A为固体,反应前后气体的化学计量数之和相等,无论是否达到平衡状态,气体体积不变,所以不能根据容器体积判断是否达到平衡状态,故A错误;
B.无论反应是否达到平衡状态,B的生成速率和D的反应速率始终为3:1,所以不能说明正逆反应速率相等,故B错误;
C.当反应达到平衡状态时,各物质的浓度不再变化,则其密度不再变化,所以能证明该反应达到平衡状态,故C正确;
D.平衡时的浓度取决于起始物质的配料比以及转化的程度,不能用以判断是否达到平衡状态,故D错误.
故选C.
本题解析:
本题难度:简单