��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ԭ�ӵļ۵����Ų��У���Ӧ�ڵ�һ�����������ǣ�������
A��4s24p1
B��3s23p2
C��2s22p3
D��2s23p4
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� ���������У������ڵ���ʵ���
A.H2SO4
B.CH4
C.KOH
D.Na2SO4
�ο��𰸣�B
������������������������ˮ��Һ�л�����״̬���ܵ���Ļ�����ǵ��������ˮ��Һ�к�����״̬�¶����ܵ���Ļ���������л��ﶼ�Ƿǵ���ʣ����۵���ʻ��Ƿǵ���ʶ������ǻ������
���A��������ˮ��Һ���ܵ�����������Ӷ�ʹ��ˮ��Һ���磬��������ĵ���ʣ���A����
B��������ˮ��Һ���Է��Ӵ��ڣ������Ƿǵ���ʣ���B����
C��������������ˮ��Һ�л�����״̬�¾��ܵ���Ļ�������ڵ���ʣ���C����
D������������ˮ��Һ�л�����״̬�¾��ܵ���Ļ�������ڵ���ʣ���D����
��ѡB��
���������⿼���˵���ʡ��ǵ���ʵ��жϣ��ѶȲ���ע�����ʱ�����һ�����磬����IJ�һ���ǵ���ʣ������۵���ʻ��Ƿǵ���ʶ������ǻ����Ϊ�״��㣮
�����Ѷȣ�����
3��ѡ���� ij��Һ�п��ܺ���Ba2+��I-��NH4+��Cu2+��SO32-�������Һ�м���������ˮ����Һ�Գ���ɫ�������й��ڸ���Һ��ɵ��ж���ȷ����
�ٿ϶�����I-?�ڿ϶�����Cu2+?�ۿ϶�����SO32-?�ܿ��ܺ���I-?�ݿ��ܺ���Ba2+��
A.�٢�
B.�٢ڢ�
C.�ۢ�
D.�ڢۢ�
�ο��𰸣�B
�����������������Һ�м���������ˮ����Һ�Գ���ɫ��˵����Һ�в���I-���ӣ����Ҳ���Cu2+���ӣ��纬Cu2+���ӣ�����Һ����ɫ��������Һ�����ԣ���һ���ж����������Ƿ���ڣ�
�����Һ�м���������ˮ����Һ�Գ���ɫ��˵����Һ�в���I-���ӣ����Ҳ���Cu2+���ӣ��纬Cu2+���ӣ�����Һ����ɫ��������Һ�����ԣ�������ֻʣ��SO32-���ӣ���һ������SO32-���ӣ�SO32-������Ba2+���ܹ��棬һ������Ba2+������ȷ���Т٢ڢۣ���ѡB��
���������⿼�����Ӽ�����Ŀ������ʱע�����Ŀ���ҳ���Ӧ�ĵ������������ʵ����ʽ����ƶϣ������ѶȲ���
�����Ѷȣ�����
4��ѡ���� ������������Ԫ�صĵ���������(��λ��kJ/mol)���ж�����˵������ȷ����
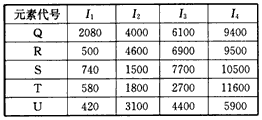
[? ]
A��Ԫ�صĵ縺�����Ŀ�����QԪ��
B��R��S��������U��ͬһ����
C��UԪ�ؿ��������ڱ���s��
D��ԭ�ӵļ۵��ӹ���Ϊns2np1�Ŀ�����TԪ��
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5��ѡ���� �������¼������ӷ���ʽ��CaCO3+2H+�TCa2++H2O+CO2����H++CO32-�THCO����CO2+H2O+ClO-�THClO+HCO3-����CO32-+HSO3-�THCO3-+SO42-���ɴ˵ó������½����в���ȷ����
A.CO32-��H+��Ca2+���ܴ�������
B.H2CO3�����Ա�HClOǿ����H2SO3��
C.H2SO3��һ��ǿ��
D.H2CO3��HClO����������
�ο��𰸣�C
���������������A�������Ӧ����ˮ�������Լ���������ʵ����Ӳ��ܹ��棻
B������ǿ���������ԭ�����ش��жϣ�
C�������������ᣬ������ǿ�
D��̼��ʹ������������ȫ���룮
���A��CO32-��H+��Ca2+������Ӧ�ֱ�����ˮ��������̼�Լ�̼��ƣ����ܴ������棬��A��ȷ��
B�����ݷ�ӦCO2+H2O+ClO-�THClO+HCO3-��ǿ���������ԭ������֪��H2CO3�����Ա�HClOǿ����H2SO3������B��ȷ��
C��H2SO3��һ�����ᣬ��C����
D��̼��ʹ������������ȫ���룬���������ᣬ��D��ȷ��
��ѡC��
�����������漰���ӹ��桢��ѧ��Ӧԭ���Լ����ǿ���ȷ���֪ʶ��ע�ⳣ��֪ʶ�������ǹؼ����ѶȲ���
�����Ѷȣ�һ��