微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对元素“电负性”数值的理解不正确的是
[? ]
A.“电负性”数值通常用来描述不同元素的气态原子得电子能力的大小
B.“电负性”数值的大小通常可以区分是金属、非金属还是类金属
C.成键两元素“电负性”数值的差值可以粗略预测形成化学键的类型
D.“电负性”数值通常用来作为判断元素金属性、非金属性强弱的尺度
2、选择题 A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素的下列叙述:
①原子半径A<B;②离子半径A>B;③原子序数A>B;④原子最外层电子数A<B;⑤A 的正价与B的负价绝对值一定相等;⑥A的电负性小于B的电负性;⑦A的第一电离能大于B的第一电离能。
其中正确的组合是
[? ]
A.①②⑦
B.③④⑥
C.③⑤
D.③④⑤⑥⑦
3、填空题 三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用。NF3是一种三角锥型分子,键角102?°,沸点-129?℃;可在铜的催化作用下由F2和过量NH3反应得到。
(1)写出制备?NF3的化学反应方程式:____________。
(2)NF3的沸点比NH3的沸点(-33?℃)低得多的主要原因是?_____________。
(3)与铜属于同一周期,且未成对价电子数最多的元素基态原子核外电子排布式为_____________。
(4)理论上HF、NaAlO2和NaCl按6∶1∶2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,则该物质的化学式为___________其中心离子是______________?,配位数为_______________?。
(5)根据下列五种元素的第一至第四电离能数据(单位:kJ・mol-1?),回答下面各题:
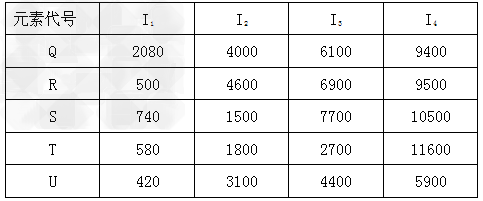
①在周期表中,最可能处于同一族的是?和? 。
②T 元素最可能是?区元素。若T 为第二周期元素,E 是第三周期元素中原子半径最小的元素,则T 、E 形成化合物的空间构型为?,其中心原子的杂化方式为? 。
4、选择题 某元素X的逐级电离能如图表示,下列说法正确的是( )
A.X元素可能为+4价
B.X可能为非金属
C.X为第五周期元素
D.X与氯反应时最可能生成的阳离子为X3+
