��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����˵������ȷ����?
A���ڹ̶�������ܱ������з������淴ӦA��s��+B��g�� C(g)+D��g���������������ܶȲ��ٸı�ʱ��˵���Ѵﵽ��ѧƽ��״̬
C(g)+D��g���������������ܶȲ��ٸı�ʱ��˵���Ѵﵽ��ѧƽ��״̬
B�����ڷ�ӦC��s��+CO2(g) 2CO(g)��H>0���ı�ijһ����������ѧƽ�ⳣ��������Ӧ����Ҳһ������
2CO(g)��H>0���ı�ijһ����������ѧƽ�ⳣ��������Ӧ����Ҳһ������
C����0.1mol��L-1��NH3��H2O�м����Ȼ�粒��壬����Һ�� ����
����
D����������Mg��OH��2����Һ�м���MgCl2Ũ��Һ����Һ�� ����
����
2��ѡ���� ij�¶��£���Ӧ2CH3OH(g)  CH3OCH3(g)+H2O(g)��ƽ�ⳣ��Ϊ400�����¶��£����ݻ�һ�����ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
CH3OCH3(g)+H2O(g)��ƽ�ⳣ��Ϊ400�����¶��£����ݻ�һ�����ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
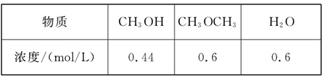
����˵������ȷ����(? )
A��ƽ��ʱCH3OH��ת���ʴ���80%
B����ʱ�淴Ӧ����С������Ӧ����
C��ƽ��ʱCH3OH��Ũ��Ϊ0.04 mol/L
D��CH3OH����ʼŨ��Ϊ1.04 mol/L
3������� ��������麟���������ҽҩ�Լ������ʹٽ���������Ԫ���ȣ���һ�ֿɹ�İ�������ijѧϰС���о���ʵ�������Ʊ���������淋Ļ�ѧԭ����?
��1���������Ϊ2:1��NH3��CO2����������һ���ݻ����������ܱ������У��ں㶨�¶���ʹ�䷢����Ӧ���ﵽƽ�⣺2NH3(g)��CO2(g)  NH2COONH4(s)
NH2COONH4(s)
��ʵ���õIJ�ͬ�¶��µ�ƽ�����������±���
�¶�(��)
| 15.0
| 20.0
| 25.0
| 30.0
| 35.0
|
ƽ����ѹǿ(kPa)
| 5.7
| 8.3
| 12.0
| 17.1
| 24.0
|
ƽ��������Ũ�� (10��3mol/L)
| 2.4
| 3.4
| 4.8
| 6.8
| 9.4
|
?
��������Ӧ�ĵ��ʱ䣺?H?0���ر�?S?0���������������������
���ݱ������ݣ������25.0��ʱ2NH3(g)��CO2(g)  NH2COONH4(s)�Ļ�ѧƽ�ⳣ��K��?��
NH2COONH4(s)�Ļ�ѧƽ�ⳣ��K��?��
�������Ѵ�ƽ��״̬�����������з���������İ�������茶��壬��Ӧ���ת���ʽ�?�����������С�����䡱����
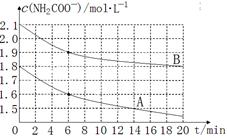
��2����������識���ˮ�⣺NH2COONH4��2H2O  ?NH4HCO3��NH3��H2O����ѧϰС��Ϊ����������ˮ�ⷴӦ���ֱ�ȡ�����Ƶõ���Ʒ����������ˮ�в����Ƴɲ�ͬŨ�ȵİ����������Һ�����Ƴ�c(NH2COO��)��ʱ�䣨t���仯��������ͼ��ʾ����A��B�ֱ�Ϊ��ͬ�¶�ʱ�ⶨ�����ߣ���?���A����B������������Ӧ��ʵ���¶ȸߣ��жϵ�������?��
?NH4HCO3��NH3��H2O����ѧϰС��Ϊ����������ˮ�ⷴӦ���ֱ�ȡ�����Ƶõ���Ʒ����������ˮ�в����Ƴɲ�ͬŨ�ȵİ����������Һ�����Ƴ�c(NH2COO��)��ʱ�䣨t���仯��������ͼ��ʾ����A��B�ֱ�Ϊ��ͬ�¶�ʱ�ⶨ�����ߣ���?���A����B������������Ӧ��ʵ���¶ȸߣ��жϵ�������?��
4��ѡ���� ���в�����ʹH2O�ĵ���ƽ�����������ƶ�����������Һ�����Ե���
A����ˮ�м���������HCl
B����ˮ�м���������NaOH
C����ˮ�м���NaCl��������100�棬pH="6"
D����ˮ�м�������NH4Cl
5��ѡ���� ���ܱ�������һ����������巢����Ӧ��x A (g) + y B(g) ?z C(g)��ƽ��ʱ���A��Ũ��Ϊ 0.5 mol/L�������¶Ȳ��䣬���������ݻ�ѹ����ԭ����1/2���ٴ�ƽ��ʱ���A��Ũ��Ϊ 0.8mol/L�������ж���ȷ���ǣ�?��
?z C(g)��ƽ��ʱ���A��Ũ��Ϊ 0.5 mol/L�������¶Ȳ��䣬���������ݻ�ѹ����ԭ����1/2���ٴ�ƽ��ʱ���A��Ũ��Ϊ 0.8mol/L�������ж���ȷ���ǣ�?��
A��x+y ��z
B��ƽ��������Ӧ�����ƶ�
C��B�����ʵ�������
D��C������������ֲ���