微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是?
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是?
A.2v(NH3)=v(CO2)
B.密闭容器中c(NH3)∶c(CO2)=2∶1
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
参考答案:C
本题解析:该反应为有固体参与的非等体反应,且容器体积不变,所以压强、密度均可作标志,该题应特别注意D项,因为该反应为固体的分解反应,所以NH3、CO2的体积分数始终为定值(NH3为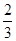 ,CO2为
,CO2为 )。
)。
本题难度:一般
2、填空题 (8分)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃
| 700
| 800
| 830
| 1000
| 1200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
?回答下列问题:
(1)该反应的化学平衡常数表达式为K=?;
(2)该反应为?反应(选填吸热、放热);
(3)某温度下,平衡浓度符合下式:3c(CO2)・c(H2)=5c(CO)・c(H2O),试判断此时的温度为?℃;
(4)830℃时,向该容器中加入1L CO2与1L H2?,平衡时CO2的体积分数是?。
参考答案:(1)K=_ _。
_。
(2) _放热_(填“吸热”或“放热”)反应。
(3)减小__(填“增大”、“减小”或“不变”,下同),_增大____。
(4)不移动(填“向左”、“向右”、“不移动”),增大A的浓度 _,__B
本题解析:略
本题难度:一般
3、填空题 一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:
2SO2(g)+O2(g) 2SO3(g)(正反应放热)
2SO3(g)(正反应放热)
反应过程中SO2、O2、SO3物质的量变化如图2-61所示:

图2-61
完成下列问题:
(1)降低温度,SO2的转化率____________,化学反应速度____________。(填“增大”“减小”或“不变”)
(2)反应处于平衡状态的时间是____________。
(3)反应进行至20 min时,曲线发生变化的原因是________________________ (用文字表达)。10 min到15 min的曲线变化的原因可能是____________(填写编号)。
a.加了催化剂
b.缩小容器体积
c.降低温度
d.增加SO3的物质的量
参考答案:(1)增大减小(2)15~20 min,25~30 min(3)增加了O2的量? ab
本题解析:(1)降温,平衡向正反应方向移动,SO2的转化率增大,化学反应速率降低。
(2)反应进行15 min时,SO2、O2、SO3的物质的量均不发生变化,说明反应达到了平衡状态。
(3)反应进行至20 min,O2的物质的量发生突变,说明此时增加了O2的量。
本题难度:一般
4、填空题 在真空密闭容器中加入amol PH4I固体,在一定温度下发生反应:
PH4I(s)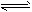 PH3(g)+HI(g)
PH3(g)+HI(g)
4PH3(g)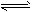 P4(S)+6H2(g)
P4(S)+6H2(g)
2HI(g)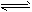 H2(g)+I2(g)
H2(g)+I2(g)
以上三个反应建立平衡后,测得HI为bmol,I2(g)为cmol,H2为dmol。求:
(1)平衡后,容器内P4(g)和PH3(g)的物质的量(用a,b,c,d表示) n(P4)=___________,
n(PH3)= ______________。
(2)a,b,c三者的关系服从a>________(填b,c的代数式)。
(3)平衡后,增大压强容器内n(I2)________,n(PH4I)_________。(填增大、减小、不变)
参考答案:(1)n(P4)=[1/6](d-c)mol;n(PH3)=b+[1/3](8-2c)mol
(2)b+2c
(3)减少;增加
本题解析:
本题难度:一般
5、选择题 在一定条件下,在容积为2L的密闭容器中,将2 mol 气体M和3 mol N气体混合,发生如下反应:2M(g) + 3N(g)  ?x Q(g) +3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4 mol/L,下列有关叙述正确的是
?x Q(g) +3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4 mol/L,下列有关叙述正确的是
A.x值为2
B.混合气体的密度增大
C.平衡时N的浓度为0.2 mol/L
D.N的转化率为80%
参考答案:D
本题解析:采用“三段式”计算
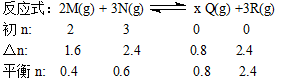
从以上数据可看出:x=1,平衡时N的浓度为0.3 mol/L,N的转化率为80%
由于气体的体积及质量均不变,故密度也是定值
答案为D
本题难度:一般