微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于原电池的叙述中,正确的是( )
A.构成原电池的两极必须是两种不同的金属
B.原电池是将化学能转化为电能的装置
C.原电池工作中总是负极溶解,正极上有物质析出
D.在原电池正极上发生反应的物质是还原剂,总是溶液中的阳离子在此被还原
参考答案:A.构成原电池的两个电极可能都是金属,也可能是金属和导电的非金属,故A错误;
B.原电池是将化学能转变为电能的装置,故B正确;
C.原电池工作时,负极上失电子,但负极材料不一定溶解,正极上得电子但不一定有物质析出,如氢氧燃料电池,故C错误;
D.在原电池正极上发生反应的物质是氧化剂,但不一定是溶液中的阳离子在此被还原,如氢氧燃料电池,故D错误;
故选B.
本题解析:
本题难度:简单
2、填空题 研究碳及其化合物的综合利用对促进低碳社会的构建具有重要的意义。请运用相关知识研究碳及其化合物的性质。
(1)近年来,我国用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
C+ K2Cr2O7+ ― CO2↑+ K2SO4 + Cr2(SO4)3+ H2O
①完成并配平上述化学方程式。
②在上述方程式上用单线桥标出该反应电子转移的方向与数目。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是 。
②由MgO可制成“镁-次氯酸盐”电池,其装置示意图如图1,该电池反应的离子方程式为 。
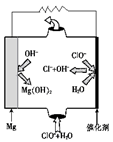

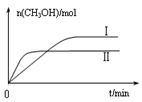
图1 图2 图3
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K= 。
②取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的△H 0(填“>”“<”或“=”)。
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、II对应的平衡常数大小关系为KⅠ KII(填“>” “<”或“=”)。
参考答案:(1)①3 2 8 H2SO4 3 2 2 8 (2分)
②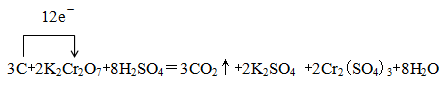 (1分)
(1分)
(2)①2MgSO4 + CO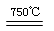 2MgO + SO2 + CO2 + SO3(3分)
2MgO + SO2 + CO2 + SO3(3分)
②Mg + ClO- + H2O=Cl- + Mg(OH)2(3分)
(3)①K=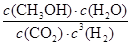 (2分) ②< (2分) ③> (2分)
(2分) ②< (2分) ③> (2分)
本题解析:(1)①根据反应式可知,反应中碳元素的化合价从0价升高到+4价,失去4个电子,碳是还原剂。Cr元素的化合价从+6价降低到+3价,得到3个电子,K2Cr2O7是氧化剂。根据电子得失守恒可知,还原剂碳与氧化剂K2Cr2O7的物质的量之比是3:2。根据原子守恒可知,反应前还有硫酸参加,因此配平后的方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4 +2Cr2(SO4)3+8H2O。
②根据①可知,用单线桥标出该反应电子转移的方向与数目为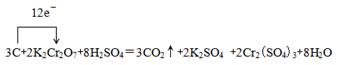 。
。
(2)①用CO还原MgSO4,在750℃时,测得气体中含等物质的量SO2和SO3,其中S元素的化合价从+6价降低到+4价,得到2个电子,所以根据电子得失守恒可知,CO的氧化产物是CO2,且与SO2的物质的量相等,因此此时反应的化学方程式是2MgSO4 + CO 2MgO + SO2 + CO2 + SO3。
2MgO + SO2 + CO2 + SO3。
②根据图1可知,镁是负极失去电子转化为氢氧化镁。次氯酸盐在正极得到电子,被还原为氯离子,所以该电池的总反应离子方程式为Mg + ClO- + H2O=Cl- + Mg(OH)2。
(3)①化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据方程式可知该反应的平衡常数表达式为K=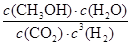 。
。
②根据图2可知,在甲醇的含量达到最大值后,如果升高温度,甲醇的含量反而降低,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应,即△H<0。
③根据图3可知,曲线Ⅱ首先达到平衡状态,这说明曲线Ⅱ的反应速率快。但曲线Ⅱ对应的甲醇物质的量小于曲线I对应的甲醇的物质的量。由于该反应是体积减小的放热的可逆反应,所以反应条件应该是升高温度,促使平衡向逆反应方向移动,因此平衡常数减小,即KⅠ>KII。
考点:考查氧化还原反应配平、表示;原电池判断;平衡常数以及外界条件对平衡状态的影响
本题难度:困难
3、填空题 请回答下列化学有关问题:
(1)现代工业将煤汽化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的用途。
①已知:2C(s)+O2(g)=2CO(g);ΔH1 ,? 2H2(g)+O2(g)=2H2O(g);ΔH2 。
则反应C(s)+H2O(g)  CO(g)+H2(g);ΔH=?。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH=?。(用含ΔH1、ΔH2的代数式表示)
②CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)  CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol?CO和2mol?H2的混合气体,控温,进行实验测得相关数据如下图1和图2。
CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol?CO和2mol?H2的混合气体,控温,进行实验测得相关数据如下图1和图2。
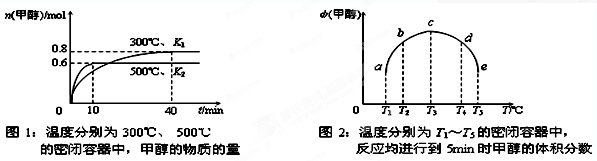
a. 该反应的ΔH3??0(选填“<”、“>”或“=”,下同), K1?K2。?
b. 将容器d中的平衡状态转变到容器c中的平衡状态,可采取的措施有?。
(2)煤汽化后的煤渣可提炼重金属。右图为某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度变化情况。据图分析:
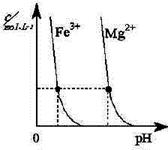
该温度下,溶度积常数的关系为:Ksp[ Fe(OH)3]____Ksp[Mg(OH)2]
(填:>、=、<);如果在新生成的Mg(OH)2浊液中滴入足量的Fe3+,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是?
参考答案:(1)(7分)? ① (ΔH1-ΔH2)/2? ② a.< ?>? b. 降温、增(或加)压
(2)<?由于Ksp[ Fe(OH)3]<Ksp[Mg(OH)2] (1分),浊液中存在溶解平衡:Mg(OH)2 Mg2++2OH-(1分),新加入的Fe3+与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动(1分),最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3(1分)。
Mg2++2OH-(1分),新加入的Fe3+与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动(1分),最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3(1分)。
本题解析:(1)①根据盖斯定律可知,(①-②)÷2即得到C(s)+H2O(g)  CO(g)+H2(g),所以ΔH= (ΔH1-ΔH2)/2。
CO(g)+H2(g),所以ΔH= (ΔH1-ΔH2)/2。
②根据图像可知,温度高,平衡时甲醇的低,说明升高温度,平衡溴逆反应方向移动,因此正反应是放热反应,低温下的平衡常数大,即K1>K2。
③d转化为c,甲醇的物质的量增加,说明平衡向正反应方向移动,因此根据反应式可知,反应是放热的、体积减小的可逆反应,所以改变的条件可以是降温或增(或加)压。
(2)根据图像可知,在金属离子浓度相同的条件下,氢氧化铁形成沉淀需要的pH小,所以氢氧化铁的溶度积常数小于氢氧化镁的。由于Ksp[ Fe(OH)3]<Ksp[Mg(OH)2],浊液中存在溶解平衡:Mg(OH)2 Mg2++2OH-,新加入的Fe3+与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动,最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3。
Mg2++2OH-,新加入的Fe3+与OH-生成更难溶解的Fe(OH)3,使平衡继续向右移动,最后Mg(OH)2全部溶解转化为红棕色的Fe(OH)3。
本题难度:一般
4、选择题 把a、b、c、d四块金属浸泡在稀H2SO4中,用导线两两相连组成原电池.若a、b相连时,a为负极;c、d相连时,d极上产生大量气泡;a、c相连时,c极发生还原反应;b、d相连时,电子由d经导线流向b.则这四种金属的活动性由强到弱为
A.a>b>c>d
B.a>c>d>b
C.c>a>b>d
D.b>d>c>a
参考答案:B
本题解析:作负极的金属较作正极的金属活泼.a、b相连时,a为负极,则活泼性a>b.c、d相连时d上产生大量气泡,d为正极,则活泼性c>d.a、c相连时,c极发生还原反应,c作正极,则活泼性a>c.b、d相连时,电子由d经导线流向b,d为负极,则活泼性d>b.综合以上分析,活泼性a>c>d>b.
本题难度:简单
5、填空题 Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4―SOCl2。电池的总反应可表示为:4Li+2SOCl2 ==="4LiCl" +S +SO2
请回答下列问题:
(1)电池的负极材料为__________,发生的电极反应为__________________;
(2)电池正极发生的电极反应为_________________________________________;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成.如果把少量水滴到SOCl2中,实验现象是_______________________________________,
反应的化学方程式为______________________________________________;
(4)组装该电池必须在无水、无氧的条件下进行,原因是
_______________________________________________________________________。
参考答案:(10分)? (1)锂 (1分)? Li-e-=Li+(2分)
(2)2SOCl2+4e-=4Cl-+S+SO2(2分)
(3)出现白雾,有刺激性气体生成 (1分) SOCl2+H2O===SO2↑+2HCl↑(2分)
(4)锂是活泼金属,易与H2O、O2反应; SOCl2也可与水反应(2分)
本题解析:(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反。所以根据方程式可知,Li失去电子,是还原剂,因此负极材料是Li,负极电极反应式是Li-e-=Li+。
(2)正极得到电子,发生还原反应,则正极电极反应式是2SOCl2+4e-=4Cl-+S+SO2。
(3)NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成,因此如果把少量水滴到SOCl2中,会生成亚硫酸和氯化氢,所以实验现象是出现白雾,有刺激性气体生成,反应的化学方程式是SOCl2+H2O=SO2↑+2HCl↑。
(4)由于锂是活泼金属,易与H2O、O2反应,且SOCl2也可与水反应,所以该电池必须在无水、无氧的条件下进行。
点评:该题是中等难度的试题,试题以新型原电池为载体,重点考查学生灵活运用原电池原理解决实际问题的能力,有利于激发学生的学习兴趣和学习积极性,有利于培养学生的逻辑推理能力和规范答题能力。
本题难度:一般