| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ������Ļ�ѧ��Դ����Ƶ���㹮�̣�2017��ģ��棩(��)
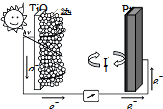 �ο��𰸣�A����ͼ���ӵ��ƶ������֪���뵼����TiO2��Ⱦ��Ϊԭ��صĸ��������缫Ϊԭ��ص������������ΪI3-��I-�Ļ���I3-�������ϵõ��ӱ���ԭ��������ӦΪI3-+2e-=3I-����A��ȷ�� ��������� �����Ѷȣ��� 4��ѡ���� ����ӵ���Ѿ���ΪӦ����㷺�Ŀɳ���أ�ij������� ��صĽṹʾ��ͼ��������������ĸ�Ĥֻ����Li+ͨ������س��ʱ���ܷ�Ӧ��ѧ����ʽΪ��LiC002=Li1-xC002+xLi�����ڸõ�ص����۴�����ǣ������� |

�ο��𰸣�A���ŵ�ʱ����ԭ��صĹ���ԭ������ԭ����У�������Li+������������A��ȷ��
B���ŵ�ʱ����ԭ��صĹ���ԭ����ԭ��صĸ�������ʧ���ӵ�������Ӧ����xLi-xe-=xLi+����B��ȷ��
C�����ʱ�����ڵ��صĹ���ԭ�������ص����������õ��ӵĻ�ԭ��Ӧ�����Ԫ�ر���ԭ����C����
D�����ʱ�����ڵ��صĹ���ԭ���������ǽ�����ת��Ϊ��ѧ�ܵ�װ�ã���D��ȷ��
��ѡC��
���������
�����Ѷȣ���
5��ѡ���� �ݱ��������������о���п���ȡ��Ŀǰ�㷺ʹ�õ����أ���������������ȾС���ص㣮���ط�ӦΪ��2Zn+O2=2ZnO��ԭ��Ϊп�������͵������Һ��������������ȷ���ǣ�������
A��пΪ�����������ڸ�����Ӧ
B�������ĵ缫��ӦΪ��Zn-2e-+2OH-�TZnO+H2O
C��OH-�ڵ������Һ���������ƶ�
D����ع���ʱ��Һ��pH?����
�ο��𰸣�A��п�Ļ��ϼ����ߣ�ʧȥ���ӣ�����������Ӧ��ԭ��صĸ����������õ����ӵ�����������A����
B���������Һһ����������Һ����Ϊ���в�����������п�������Ǽ��Ե�أ������ĵ缫��ӦΪ��Zn-2e-+2OH-�TZnO+H2O����B��ȷ��
C��OH-�ڵ������Һ�����ƶ�����C����
D����ع���ʱ��������ӦΪ��O2+2H2O+4e-=4OH-����Һ������������Ũ�Ȼ������䣬PH���䣬��D����
��ѡB��
���������
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ������������ԭ��.. | |
| �����Ŀ |