微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在标准状况下,将NO、NO2、O2三种气体按一定比例充满一固定容积的容器,并将该容器倒置在水槽中,充分反应后,容器中无气体剩余,所得溶液的浓度为Mmol/L。则M的取值范围是
A.0<M<1/22.4
B.1/39.2<M<1/22.4
C.1/28<M<1/22.4
D.1/39.2<M<1/28
参考答案:D
本题解析:设烧瓶容积为V升,采用极值法
当原混合气体全部为NO和O2时:4NO+3O2+2H2O=4HNO3,硝酸的物质的量为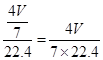 =mol,溶液的浓度为
=mol,溶液的浓度为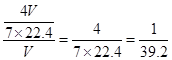 =mol/L
=mol/L
当原混合气体全部为NO2和O2时:4NO2+O2+2H2O=4HNO3,硝酸的物质的量为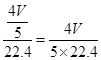 =mol,溶液的浓度为
=mol,溶液的浓度为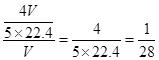 mol/L
mol/L
故答案为D
本题难度:一般
2、选择题 不需要放入棕色瓶存放的溶液是(? )
A.浓硫酸
B.浓硝酸
C.浓氨水
D.硝酸银
参考答案:A
本题解析:见光易分解的物质一般需要保存在棕色瓶中,在4个选项中浓硫酸稳定,不易分解,所以答案是A。
本题难度:简单
3、选择题 NH4HCO3是一种离子化合物,下列关于该物质的叙述错误的是
A.所含四种元素的原子半径由小到大的顺序为:H<O<N<C
B.同周期的三种元素的得电子能力由大到小的顺序为: O>N>C
C.除去NaCl固体中混有少量的NH4HCO3固体可以采用加热的方法
D.其与足量氢氧化钠溶液共热的离子方程式为:NH4++OHˉ NH3↑+H2O
NH3↑+H2O
参考答案:D
本题解析:A.H是第一周期的元素,原子核外有一个电子层,C、N、O都是第二周期的元素,原子核外有两个电子层。对于电子层数不同的元素来说,原子的电子层数越多原子半径越大;对于电子层数相同的元素来说,元素的原子序数越大,原子半径就越小。所以这四种元素的原子半径由小到大的顺序是H<O<N<C。正确。B.同周期的三种元素从左到右,元素的非金属性逐渐增强,元素的原子得到电子的能力逐渐增强。故得电子能力由大到小的顺序为: O>N>C 。正确。C.加热时NH4HCO3发生分解反应:NH4HCO3 NH3↑+H2O+CO2↑。不会有残留的固体杂质。因此可以采用加热的方法除去NaCl固体中混有少量的NH4HCO3杂质。正确。D.NaOH与NH4HCO3电离产生的阴离子、阳离子均发生反应。故其与足量氢氧化钠溶液共热的离子方程式为:HCO3-+NH4++2OHˉ
NH3↑+H2O+CO2↑。不会有残留的固体杂质。因此可以采用加热的方法除去NaCl固体中混有少量的NH4HCO3杂质。正确。D.NaOH与NH4HCO3电离产生的阴离子、阳离子均发生反应。故其与足量氢氧化钠溶液共热的离子方程式为:HCO3-+NH4++2OHˉ NH3↑+H2O + CO32-.错误。4HCO3的化学性质的知识。
NH3↑+H2O + CO32-.错误。4HCO3的化学性质的知识。
本题难度:简单
4、选择题 将下列各组气体分别通入水中,其中一种气体消失,另一种气体体积增大的是(?)
A.CO2和HCl
B.O2和F2
C.SO2和Cl2
D.NO和NO2
参考答案:BD
本题解析:2F2+2H2O====4HF+O2,3NO2+H2O====2HNO3+NO。
本题难度:简单
5、填空题 (13分)如右图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由_______________逐渐变为_______色,试管内的液面会逐渐_____________,剩余气体约占试管容积的__________,用化学方程式表示这种变化__________________________;上述反应停止后向试管中缓慢通入氧气,气体颜色又由______色逐渐变为____________色,之后又变为______色,继续通入氧气,直到试管中充满液体为止,用一个化学方程式表示试管中发生的化学反应_____________________________________。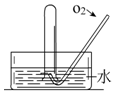
参考答案:红棕色?无?上升? 1/3? 3NO2 + H2O = 2HNO3 + NO?无?红棕色?无? 4NO + 3O2 + 2H2O = 4HNO3
本题解析:略
本题难度:一般