微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E
的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2
反应生成C2A和气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:A_______,B_______, E_______。
(2)画出E的原子结构示意图_____?__。
写出电子式D2A2___?____,EB4__?_?____。
(3)比较EA2与EB4的熔点高低(填化学式)_______>_______。
(4)A的氢化物的沸点与同族下一周期元素的氢化物相比,A的氢化物的沸点?(填“高”或“低”),原因是?。
参考答案:(1)氧、氟、硅(2)略(3)SiO2;SiF4(4)高,因为A的氢化物分子间可形成氢键,而另一种则无。(每空1分共10分)
本题解析:略
本题难度:简单
2、选择题 下列各组液体混合物中有两种成分,可以用分液漏斗分离的是
A.甲苯和油脂
B.乙酸和乙酸乙酯
C.豆油和水
D.豆油和四氯化碳
参考答案:C
本题解析:用分液漏斗分离的条件是两种液体互不相溶且密度不同而能分层.C项中豆油是有机物,水为无机强极性溶剂,其余各组均互溶.
本题难度:困难
3、选择题 下列元素一定是主族元素的是(?)
A.原子核外N电子层上只有一个电子的元素
B.原子核外M层电子数为偶数的元素
C.原子核外M层电子数为奇数的元素
D.原子核外N层电子数为2的元素
参考答案:C
本题解析:原子核外N电子层上只有一个电子的元素可能是主族元素如K,也可能不是主族元素如Cu和Cr,所以A错;原子核外M层电子为偶数,则M层电子数可能为2、4、6、8,可能为0族元素,不一定是主族元素,所以B错;而原子核外M层电子数为奇数,说明该元素原子的M层即为最外层,其电子数可能为1、3、5、7,最外层电子数等于主族序数,所以C正确;原子核外N层电子数为2的元素可能是主族元素如Ca,也可能不是主族元素如Zn,所以D错。
本题难度:一般
4、选择题 电泳实验中发现硫化砷的胶粒移向阳极,由此可推断硫化砷胶粒
A.带负电荷
B.带正电荷
C.不带电荷
D.可能带正电荷,也可能带负电荷
参考答案:A
本题解析:电泳实验中移向阳极的胶粒带负电荷,移向阴极的胶粒带正电荷。
本题难度:简单
5、填空题 有关短周期元素A、B、C、D、E、F的信息如下:
元素
| 有关信息
|
A
| 最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐
|
B
| 最外层电子数是次外层电子数的2倍
|
C
| M层上有3个电子
|
D
| 短周期原子半径最大的主族元素
|
E
| 其单质是淡黄色固体
|
F
| 最高正价与最低负价代数和为6
|
?
请回答下列问题:
(1)写出实验室制取乙的化学方程式?。
(2)下列说法正确的是?(填序号)。
①实验室可用如图所示装置制取B的最高价氧化物
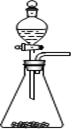
②用C单质做成的槽车,都可用来运输甲的浓溶液
③ C和铜与稀硫酸组成的原电池,C电极被还原
④ D单质在氧气中燃烧后的产物可用在防毒面具中作供氧剂
⑤鼓励乘坐公交车出行,倡导低碳生活,是控制和治理BO2解决“温室效应”的有效途径之一
 ⑥ DF的电子式为H∶Cl∶
⑥ DF的电子式为H∶Cl∶
(3)将E的常见氧化物(该氧化物能使品红溶液褪色)通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,可知其中含Cl:35.7%,Cu:64.3%,则该氧化物在上述反应中的作用是?。
A.漂白剂?B.氧化剂?C.还原剂
(4)请用化学方法加以验证(3)中的氧化物,简要写出实验方法、试剂及预期可观察到的现象?。
参考答案:(1)Ca(OH)2+2NH4Cl CaCl 2+2NH3↑+ 2H2O
CaCl 2+2NH3↑+ 2H2O
(2)①②④⑤? (少选1个得1分,少选2个或多选不得分)(3)C
(4)将适量气体样品通入品红溶液,溶液红色褪去,加热溶液,又恢复红色,说明气体为SO2(其他合理答案也可)
本题解析:A最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐,则A是氮元素,甲是硝酸,乙是氨气,生成的盐是硝酸铵。B最外层电子数是次外层电子数的2倍,则B一定是第二周期元素,是碳元素。C M层上有3个电子,所以C是Al元素。D短周期原子半径最大的主族元素,则D是Na元素。E其单质是淡黄色固体,所以E是S元素。F最高正价与最低负价代数和为6,这说明F是第ⅦA族元素,则F是氯元素。
(1)实验室制取氨气的化学方程式为Ca(OH)2+2NH4Cl CaCl 2+2NH3↑+ 2H2O。
CaCl 2+2NH3↑+ 2H2O。
(2)实验室用碳酸钙与盐酸反应制取CO2,属于固体与液体反应不需要加热的,因此装置图正确,①正确;常温下铝在浓硝酸中发生钝化,所以可以用铝单质做成的槽车,都可用来运输甲的浓溶液,②正确;铝的金属性强于铜,所以铝和铜与稀硫酸组成的原电池,铝电极是负极被氧化,③不正确;过氧化钠能和水以及CO2反应生成氧气,所以钠单质在氧气中燃烧后的产物可用在防毒面具中作供氧剂,④正确;鼓励乘坐公交车出行,倡导低碳生活,是控制和治理CO2解决“温室效应”的有效途径之一,⑤正确;钠和氯是活泼的金属与非金属,二者形成的化合物氯化钠是离子化合物,电子式为 ,⑥不正确,答案选①②④⑤。
,⑥不正确,答案选①②④⑤。
(3)将E的常见氧化物(该氧化物能使品红溶液褪色),这说明该氧化物是SO2。SO2通入由CuSO4和NaCl混合的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀进行元素质量分数分析,可知其中含Cl:35.7%,Cu:64.3%,则该沉淀中Cl与Cu的原子个数之比=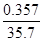 :
: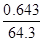 =1:1,所以其化学式为CuCl,即铜元素的化合价从+2价降低到+1价,这说明反应中硫酸铜起到氧化剂的作用,则SO2起到还原剂的作用,答案选C。
=1:1,所以其化学式为CuCl,即铜元素的化合价从+2价降低到+1价,这说明反应中硫酸铜起到氧化剂的作用,则SO2起到还原剂的作用,答案选C。
(4)SO2具有漂白性,能使品红溶液褪色,所以检验SO2的实验操作是将适量气体样品通入品红溶液,溶液红色褪去,加热溶液,又恢复红色,说明气体为SO2。2制备;过氧化钠用途;原电池判断以及SO2的性质与检验等
本题难度:一般