微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列电子式书写错误的是?
[? ]
A.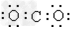
B.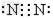
C.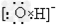
D.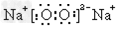
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列说法中不正确的是( )
A.在共价化合物中不可能含有离子键
B.含有共价键的化合物不一定是共价化合物
C.主族元素形成的阴离子不一定都满足8电子结构
D.非金属之间形成的化学键一定是共价键
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列各组物质中,都是由极性键构成的非极性分子是( )
A.CO2和CH4
B.NH3和H2O
C.BF3和H2
D.CS2和H2O2
参考答案:A、CO2中含有极性键,但结构对称,正负电荷的中心重合,属于非极性分子;CH4中含有极性键,但结构对称,正负电荷的中心重合,属于非极性分子,故A正确;
B、NH3中含有极性键,空间结构为三角锥形,正负电荷的中心不重合,属于极性分子;H2O中含有极性键,空间结构为V型,,正负电荷的中心不重合,属于极性分子,故B错误;
C、BF3中含有极性键,但结构对称,正负电荷的中心重合,属于非极性分子;H2中含有极性键,但结构对称,正负电荷的中心重合,属于非极性分子,故C正确;
D、CS2中含有极性键,但结构对称,正负电荷的中心重合,属于非极性分子;H2O2中含有极性键和非极性键,但结构不对称,正负电荷的中心不重合,属于极性分子;故D错误;
故选AC.
本题解析:
本题难度:简单
4、填空题 (1)Fe3+可以与SCN-、CN-、F-、有机分子等形成很多的配合物。
①写出基态Fe3+的核外电子排布式?。
②已知(CN)2是直线型分子,并有对称性,则(CN)2中π键和σ键的个数比为?。
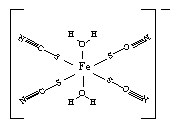
③下图是SCN-与Fe3+形成的一种配合物,画出该配合物中的配位键(以箭头表示)。
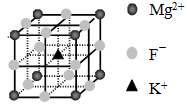
④F-不仅可与Fe3+形成[FeF6]3+,还可以与Mg2+、K+形成一种立方晶系的离子晶体(如下图)。该晶体的化学式为?。
 ?
?
(2)氨气是一种重要的化工原料。
①液氨和水类似,也能发生电离:NH3+NH3 NH4++NH2-,其离子积常数为l.0×l0-30。现将2.3g金属钠投入1.0 L液氨中,钠完全反应生成NaNH2,假设溶液的体积不变,所得溶液中NH4+的浓度
NH4++NH2-,其离子积常数为l.0×l0-30。现将2.3g金属钠投入1.0 L液氨中,钠完全反应生成NaNH2,假设溶液的体积不变,所得溶液中NH4+的浓度
为?。
②已知:N2(g)+O2(g)=2NO(g)?△H=+180kJ・mol-l
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)?△H=-908 kJ・mol-l
写出氨气被一氧化氮氧化生成氮气和气态水的热化学方程式:?。
(3)在下图装置中,若通电一段时间后乙装置左侧电极质量增加。
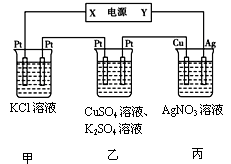
①下列说法错误的是?;
A.乙中左侧电极反应式:Cu2++2e-=Cu
B.电解一段时间后,装置丙的pH减小
C.向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态
D.电解一段时间后,向乙中加入0.1molCu(OH)2可使电解质溶液复原,则电路中通过的电子为0.2mol②若将甲中溶液换成MgCl2,则电解总反应的离子方程式为;