微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 水的电离平衡曲线如图所示。下列说法中,正确的是
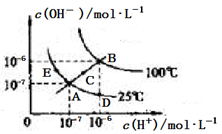
A.图中A、D、E三点处KW间的关系:E处>A处>D处
B.温度不变时,往水中通入适量HCl气体,可以使溶液中的离子浓度从A点变化到D点
C.温度不变时,在水中加入适量CH3COONa固体,可以使水的电离从A点变化到C点
D.在B点处,0.5mol・L-1的H2SO4溶液与1mol・L-1的KOH溶液等体积混合,充分反应后,所得溶液的pH=7
参考答案:B
本题解析:A错,KW只受温度影响,与其它因素无关,A、D、E三点处KW间的关系为E处=A处=D处;
B正确,往水中通入适量HCL气体,溶液中氢离子浓度增大,氢氧根离子浓度减小;
C错,温度不变,KW不变,在水中加入适量CH3COONa固体,可以使水的电离从A点变化到E点,溶液呈碱性;
D错,在B点处,0.5mol・L-1的H2SO4溶液与1mol・L-1的KOH溶液等体积混合,充分反应后,溶液呈中性,所得溶液的pH=6
本题难度:一般
2、选择题 已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ・mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ・mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ・mol-1
下列说法正确的是? ( )
A.H2(g)的燃烧热为571.6 kJ・mol-1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C. H2SO4(aq)+
H2SO4(aq)+ Ba(OH)2(aq)=
Ba(OH)2(aq)= BaSO4(s)+H2O(l) ΔH=-57.3 kJ・mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ・mol-1
D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+135.9 kJ・mol-1
参考答案:B
本题解析:燃烧热是1 mol物质完全燃烧,A错误。相同质量时H2的物质的量是CH3OH的16倍,H2放出的热量多,B项正确。H2SO4与Ba(OH)2反应除发生中和反应外还发生沉淀反应ΔH≠-57.3 kJ/mol,C项错误。D项ΔH=-131.4 kJ/mol,D项错误。
本题难度:一般
3、选择题 为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是

A.H2O的分解反应是放热反应
B.氢能源已被普遍使用
C.2 mol H2O具有的总能量低于2 mol H2和1 mol O2的能量
D.氢气不易贮存和运输,无开发利用价值
参考答案:C
本题解析:氢气燃烧生成水是放热反应,则水的分解反应是吸热反应,A不正确,C正确;由于氢气的获得目前还没有更好的技术,所以氢能源还没有被普遍使用,B不正确;氢气属于新能源,具有很好的开发价值,D不正确,答案选C。
点评:该题是常识性知识的考查,试题贴近当今的热点,有利于激发学生的学习兴趣和学习积极性,也有利于培养学生的能源节约意识。
本题难度:一般
4、选择题 C、CO、CH4、C2H5OH是常用的燃料,它们每1mol分别完全燃烧生成CO2(g)及H2O(l)时,放出的热量依次为393.5kJ、283.0kJ、890.3kJ、1?366.8kJ。相同质量的这4种燃料,完全燃烧时放出热量最多的是
[? ]
A、C?
B、CO?
C、CH4?
D、C2H5OH
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列操作中,能使电离平衡H2O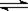 H++OH-向右移动且溶液呈碱性的是(?)
H++OH-向右移动且溶液呈碱性的是(?)
A.向水中通入氨气
B.向水中加入Al2(SO4)3溶液
C.向水中加入Na2CO3溶液
D.将水加热到100℃,使pH=6
参考答案:C
本题解析:A错误,通入氨气后,溶液呈碱性,抑制水的电离。
B错误,铝离子水解结合水电离出的氢氧根离子,使水的电离平衡向右移动,溶液呈酸性。
C正确,碳酸根离子水解结合水电离的氢离子,促进水的电离,溶液呈碱性。
D错误,加热促进电离,平衡右移,但溶液仍然呈中性。所以正确答案是C。
本题难度:一般