��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ڷ�ӦA2+3B2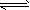 2AB3���±�ʾ�ķ�Ӧ�����У�����������
2AB3���±�ʾ�ķ�Ӧ�����У�����������
[? ]
A��vA2=0��4mol��L-1��min-1
B��vB2=0��8mol��L-1��min-1
C��vAB3=0��6mol��L-1��min-1
D��vA2=0��01mol��L-1��s-1
2������� ��һ���¶��£���4mol?SO2��2molO2����4L���ܱ������У���һ�������·�Ӧ��10����ʱ�ﵽƽ�⣺2SO2+O2?2SO3���ƽ��ʱ����������ʵ���Ϊ5mol����
��1��10����ʱO2�ķ�Ӧ����Ϊ______mol/��L?min��
��2��ƽ��ʱSO2��ת����______
��3���÷�Ӧ��ƽ�ⳣ��Ϊ______��
3��ѡ���� ij�����ܱ������У����淴ӦA(s)  ?B+C(g) ��H=" +Q" kJ��mol��1��Q�������ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
?B+C(g) ��H=" +Q" kJ��mol��1��Q�������ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
A.����B��״ֻ̬��Ϊ��̬��Һ̬
B.ƽ��ʱ����λʱ����n(A)���ĩsn(C)����=1�s1
C. ����ʼʱ�������м���1molB��1molC���ﵽƽ��ʱ�ų�����Q kJ
D. ����������䣬��ƽ����ϵ�м���B��ƽ��������淴Ӧ�����ƶ�
4��ѡ���� 25��ʱ���ں���Pb2����Sn2����ijˮ��Һ�У��������������(Sn)��������Ӧ��Sn(s)��Pb2��(aq) Sn2��(aq)��Pb(s)����ϵ��c(Pb2��)��c(Sn2��)�仯��ϵ��ͼ��ʾ�����ж���ȷ����
Sn2��(aq)��Pb(s)����ϵ��c(Pb2��)��c(Sn2��)�仯��ϵ��ͼ��ʾ�����ж���ȷ����
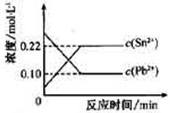
A����ƽ����ϵ�м������Ǧ��c(Pb2��)����
B����ƽ����ϵ�м�������Sn(NO3)2�����c(Pb2��)��С
C�������¶ȣ�ƽ����ϵ��c(Pb2��)����˵���÷�Ӧ����Ϊ��H>0
D��25��ʱ���÷�Ӧ��ƽ�ⳣ��K��2.2
5������� ��1��20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ��˵�������Ӧ��__________������ȡ����ȡ�����Ӧ��NO2��CO��������____________������ڡ�����С�ڡ����ڡ���CO2��NO����������

��2����ij���Ϊ2L���ܱ������г���1.5mol NO2��2mol CO����һ�������·�����Ӧ��
NO2+CO=CO2+NO��2minʱ�����������NO�����ʵ���Ϊ0.5 mol����
�ٴ˶�ʱ���ڣ���CO2��ʾ��ƽ����Ӧ����Ϊ_____________________
��2minʱ������������������ʵ���Ϊ_____________________
�ۼ���˷�Ӧ��5minʱ�ﵽƽ�⣬���ʱ����������������ʵ���_________________������ڡ�����С�ڡ����ڡ���2minʱ����������������ʵ�����