微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列措施或事实不能用勒夏特列原理解释的是
A.新制的氯水在光照下颜色变浅
B.增大压强,有利于SO2与O2反应生成SO3
C.加催化剂,使N2和H2在一定条件下转化为NH3
D.工业上生产硫酸的过程中,使用过量的空气以提高SO2的转化率
2、选择题 一定条件下,体积为2L的密闭容器中,1molX和3molY进行反应:
X(g)+3Y(g) 2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是(?)
2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是(?)
A.以X浓度变化表示的反应速率为1/8mol/(L・S)
B.12s后将容器体积扩大为10L,Z的平衡浓度变为原来的1/5
C.若增大X的浓度,则物质Y的转化率减小
D.若该反应的△H<0 ,升高温度,平衡常数K减小
3、计算题 (18分)(1)1 mol O2与足量氢气反应产生水蒸气放热483.6 kJ,若1 g水蒸气转化成液态水放热2.444 kJ,请写出表示氢气燃烧热的热化学方程式:__________________________________。
(2)由汽油裂解得到乙烯、丙烯是重要的化工原料,请写出下列转化的方程式,并注明反应类型。
丙烯? → 聚丙烯
___________________________________________________?
(3)将N2、H2置于容积为2L的密闭容器中,发生反应,反应进行到4S末,测得N2 2mol 、H21.5mol、NH32mol。则用氮气浓度的减少来表示该反应速率为__________ 。
(4)在500ml密闭容器中,将2mol A和1molB混合加热到500℃,达到平衡
2 A(g) +B (g) 3C(g)?K = 16求A转化为C的转化率为__________。
3C(g)?K = 16求A转化为C的转化率为__________。
(5) 在密闭容器中发生下列反应:aA(g)  cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a? _______ c+d(填“>”、“=”或“<”)。
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a? _______ c+d(填“>”、“=”或“<”)。
(6) 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,反应的化学方程式为______________________________________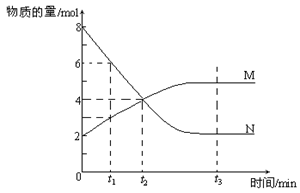
4、填空题 已知化学反应①:Fe(s)+CO2(g)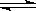 ?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)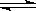 FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
温度
| K1
| K2
|
973 K
| 1.47
| 2.38
|
1173 K
| 2.15
| 1.67
|
?
请填空:
(1)通过表格中的数值可以推断:反应①是________(填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)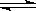 CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=?.
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=?.
(3)在相同温度下,根据反应①与②可推导出K1、K2与K3之间的关系式________,据此关系式及上表数据,也能推断出反应③是________(填“吸热”或“放热”)反应.
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有________(填写字母序号,下同).
A.增大压强? B.体积不变时充入稀有气体? C.升高温度
D.使用合适的催化剂? E.在体系中投入少量P2O5固体
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:①图甲中t2时刻发生改变的条件可能是________________.
②图乙中t2时刻发生改变的条件可能是?.
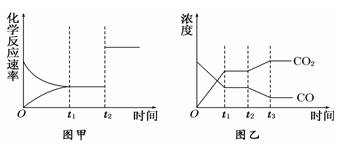
A.升高温度? B.降低温度? C.加入催化剂? D.增大压强?
E.减小压强? F.充入CO2? G.分离出部分CO
5、选择题 下列关于化学反应限度的说法正确的是
A.当某可逆反应达到平衡状态时,这就是这个反应所能达到的限度
B.当某可逆反应进行到平衡状态时,这个反应的正向反应速率和逆向反应速率相等
C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
D.化学反应的限度不可以通过改变条件而改变