��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
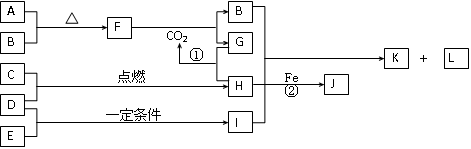
1������� A��J�ֱ��ʾ��ѧ��ѧ�г�����һ�����ʣ�����֮������ϵ��ͼ��ʾ�����ַ�Ӧ�������û���г���������֪GΪ����Ԫ�صĹ�̬���������A��һ�ֽ������ʣ�F��һ�ֺ��ɫ���壬A��B��C��D��E��F���������о���ͬһ��Ԫ�أ�����д���пհף�
��1��A��B��C��D��E��F���������к��е�ͬһ��Ԫ�������ڱ��е�λ����______��
��2��B�Ļ�ѧʽ��______��K�ĵ���ʽ��______��
��3��д���ܵ����ӷ���ʽ��______��
��4����������K��ˮ��Һ�м������ᣬʹ��ǡ����ȫ��Ӧ��������Һ��pH______7�����������������=�����������ӷ���ʽ��ʾ��ԭ��______��
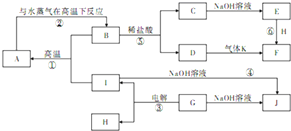
�ο��𰸣�GΪ����Ԫ�صĹ�̬�����������G��Al2O3��Al2O3��NaOH��Һ��Ӧ����NaAlO2��ˮ�����Al2O3��������������AlҲ�ܺ�NaOH��Һ��Ӧ����ΪIҲ�ܺ�NaOH��Һ��Ӧ����J����I��Al��J��NaAlO2��H��O2��
A��һ�ֽ������ʣ�F��һ�ֺ��ɫ���壬��F��Fe��OH��3��E��������Ӧ����Fe��OH��3����E��F����ͬһ��Ԫ�أ���E��Fe��OH��2��A��B��C��D��E��F���������о���ͬһ��Ԫ�أ���AΪ�������ʣ�����Ԫ���غ�֪��A��Fe������ˮ�����ڸ����·����û���Ӧ����Fe3O4��������B�ܺ����������ȷ�Ӧ����B��Fe3O4��Fe3O4�����ᷴӦ����FeCl3��FeCl2��C��NaOH��Ӧ����Fe��OH��2��D��NaOH��Ӧ����Fe��OH��3����C��FeCl2��D��FeCl3���Ȼ�����Һ�Ͱ�����Ӧ����Fe��OH��3����K��NH3��
��1��A��B��C��D��E��F���������к��е�ͬһ��Ԫ����Fe����λ�ڵ������ڡ��ڢ��壬
�ʴ�Ϊ���������ڡ��ڢ��壻
��2��ͨ�����Ϸ���֪��B��Fe3O4��K�ǰ����������ʽΪ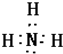 ��
��
�ʴ�Ϊ��Fe3O4��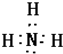 ��
��
��3����������������Һ��Ӧ����ƫ�����ƺ����������ӷ�Ӧ����ʽΪ��2Al+2OH-+2H2O�T2AlO-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O�T2AlO-+3H2����
��4�����������ᷴӦ�����Ȼ�泥��Ȼ����ǿ�������Σ�笠�������ˮ���ʹ����Һ�����ԣ���pH��7��
ˮ�����ӷ�Ӧ����ʽΪ��NH4++H2O?NH3?H2O+H+��
�ʴ�Ϊ������NH4++H2O?NH3?H2O+H+��
���������
�����Ѷȣ�һ��
2������� ��14�֣���֪A��BΪ���嵥�ʣ�����AΪ����ɫ���壬BΪ��ɫ���壻
CΪ�������ˮ��Һ��pHС��7��DΪ�������ʣ�����֮��������ת����ϵ��
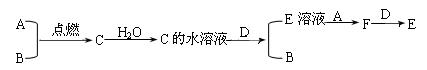
��1����д��A��B��C��D�Ļ�ѧʽ��
A_________��B_________��C___________��D_________��
��2��д��C��ˮ��Һ��D��Ӧ�����ӷ���ʽ��______________________;
E��Һ��A��Ӧ�����ӷ���ʽ��_______________________________��
F+D��Ӧ�����ӷ���ʽ��____________________________________��
�ο��𰸣���1���� 8 �֣�? Cl2? H2? HCl? Fe?
��2���� 6 �֣�? 2H++Fe = H2��+Fe2+?2Fe2++Cl2=2Fe3++2Cl-?2Fe3++Fe = 3Fe2+
�����������
�����Ѷȣ�һ��
3������� ��12�֣����п�ͼ��ʾ��ת����ϵ�У�A��B��C��D��E���dz���Ԫ�صĵ��ʣ��ڳ��³�ѹ��A�ǹ��壬��������壬��C�ʻ���ɫ��������H��I������������ʱ�������̡�������G����ɫ��ӦΪ��ɫ��ͨ�������L����ɫҺ�塣��Ӧ�ٺ͢ھ�����Һ�н��С�
�밴Ҫ���ʴ��������⣺
��1��д���������ʵĻ�ѧʽ��F?��K?��
��2������Ӧ������Һ�н��У������ӷ���ʽΪ?��
��3��ʵ������ȡI�Ļ�ѧ����ʽΪ?��
��4����J��Һ�е���NaOH��Һʱ������Ϊ?���û�ѧ����ʽ���ñ仯����?��
�ο��𰸣���1��Na2O2��2�֣�? NO��2�֣�
��2��CO32����2H����CO2����H2O��2�֣�
��3��2NH4Cl + Ca(OH)2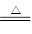 ?CaCl2 + 2NH3��+ 2H2O��2�֣�
?CaCl2 + 2NH3��+ 2H2O��2�֣�
��4�����ɰ�ɫ������Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ��2�֣�
4Fe(OH)2+ O2 + 2H2O=4Fe(OH)3��2�֣�
�����������
�����Ѷȣ���
4������� (8��) ��֪AΪ��ɫ��Һ��B��C��I��KΪ���ʣ������Ϊ���������B��L��I��K ������Ϊ���壬��ֻ��IΪ��ɫ���塣GΪ��ɫ���壬F����ɫ��Ӧ����ɫ�겣��Ƭ����ɫ��������ת����ϵ��ͼ��
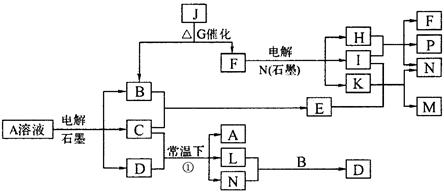
�ش��������⣺
��1��F�ĵ���ʽ��____________��
��2��д����Ӧ�ٵĻ�ѧ��Ӧ����ʽ��?��
��3���ö��Ե缫�������A��Һ��һ��ʱ�����Ҫʹ��Һ�ָ������ǰ��״̬���������Һ�м�������___________��__________��
��4����֪B��H��C2H5OH�ܹ����ȼ�ϵ�أ�д����ȼ�ϵ�صĸ����缫��Ӧ����ʽ��?��
�ο��𰸣�(8��)
��1��K��[�á���������]����2�֣�
��2��3Cu��8HNO3(ϡ) 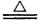 ?Cu(NO3)2��2NO��4H2O ?��2�֣�
?Cu(NO3)2��2NO��4H2O ?��2�֣�
��3��CuO��CuCO3?��2�֣�?
��4��C2H5OH��12e����16OH��==2CO32����11H2O����2�֣�
�����������
�����Ѷȣ�һ��
5������� �����£�����A��B��C�ֱ�Ϊ��������������ɫ���塢��ɫ���壬�ں��ʷ�Ӧ�����£����ǿ��������ͼ���з�Ӧ����֪E��Һ����ɫ�ģ�

��ش��������⣺
��1��A��______B��______���ѧʽ��
��2����Ӧ�ٵĻ�ѧ����ʽΪ______
��3����Ӧ�۵Ļ�ѧ����ʽΪ______
��4����Ӧ�ܵĻ�ѧ����ʽΪ______��
�ο��𰸣�BΪ����ɫ���壬ӦΪCl2��C����ɫ���嵥�����ܺ�������Ӧ����C��H2��E��HCl�������ܺ�A��Ӧ����F����������A����֮ǰ�Ľ�����F�ܱ�������������D����������A�ܺ�������Ӧ����D����A�DZ�۽�����λ����֮ǰ����A��Fe��D��FeCl3��F��FeCl2��
��1��ͨ�����Ϸ���֪��A��Fe��B��Cl2��
�ʴ�Ϊ��Fe��Cl2��
��2����Ӧ��ΪFe��Cl2�ķ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ2Fe+3Cl2��ȼ.2FeCl3���ʴ�Ϊ��2Fe+3Cl2��ȼ.2FeCl3��
��2Fe+3Cl22FeCl3
��3����Ӧ��Ϊ����ϡ����ķ�Ӧ����Ӧ����ʽΪ��2HCl+Fe=FeCl2+H2�����ʴ�Ϊ��2HCl+Fe=FeCl2+H2����
��4����Ӧ��Ϊ�Ȼ������������ķ�Ӧ����Ӧ����ʽΪ2FeCl2+Cl2=2FeCl3���ʴ�Ϊ��2FeCl2+Cl2=2FeCl3��
���������
�����Ѷȣ�һ��