��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� һ���Ի�ͭ������Ϊԭ����ȡͭ������������¹��գ�ԭ�ϵ��ۺ������ʽϸߡ�����Ҫ�������£�
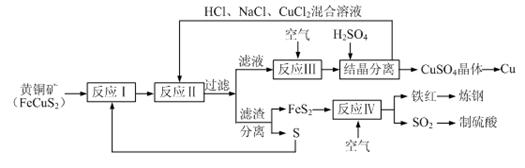
ע����Ӧ������ӷ���ʽΪCu2++CuS+4Cl����2CuCl2����S
��ش��������⣺
�ŷ�Ӧ��IJ���Ϊ���ѧʽ��? ��?��
�Ʒ�Ӧ������ӷ���ʽΪ? ��?��
��һ���¶��£��ڷ�Ӧ�����õ���Һ�м���ϡ���ᣬ������������ͭ���壬��ԭ����
? ��?��
������ʱ���ɽ�����Ͷ�����ڵ������У��ù�������Ҫ��Ӧ�Ļ�ѧ����ʽ��? ��?��
��ij���᳧Ϊ�ⶨ��Ӧ������������SO2�����������ȡ280mL��������ɱ�״����������Ʒ������Fe2(SO4)3��Һ��ȫ��Ӧ����Ũ��Ϊ0.02000 mol/L��K2Cr2O7����Һ�ζ����յ㣬����K2Cr2O7��Һ25.00 mL ��
��֪��Cr2O72��+ Fe2��+ H����Cr 3++
3++  Fe3��+ H2O��δ��ƽ��
Fe3��+ H2O��δ��ƽ��
��SO2ͨ��Fe2(SO4)3��Һ��������Ӧ�����ӷ���ʽΪ? ��?��
�ڷ�Ӧ������������SO2���������Ϊ? ��?��
�ο��𰸣���FeS2��CuS
��4CuCl2��+O2+4H+ ��4Cu2+��8Cl��+2H2O
��4Cu2+��8Cl��+2H2O
�Ǹ��¶��£�����ͭ���ܽ��С���Ȼ�ͭ
��3C+Fe2O3 2Fe+3CO
2Fe+3CO
�ɢ�SO2 + 2Fe3++ 2H2O��SO42-+ 2Fe2++ 4H+? ��12.00% ��ÿ��2�֣���12�֣�
�����������
�����Ѷȣ�һ��
2������� (10��)A��B��C��D��E����ѧ������5�ֻ����A��B�������Ԫ��X��Y���ĵ����������г����� ������������ʼ�Ĺ�ϵ����ͼ��ʾ��
������������ʼ�Ĺ�ϵ����ͼ��ʾ��
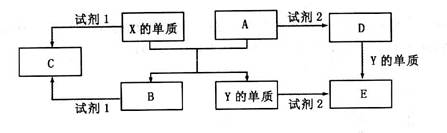
�ش��������⣺
(1)X�ĵ�����A��Ӧ�Ļ�ѧ����ʽ��___________________________________________��
(2)��C��Һ�Լ��ԣ����Լ�1��___________________________________��Һ(д��ѧʽ)��
��C��Һ�����ԣ��������Ե�ԭ����(�����ӷ���ʽ��ʾ)
____________________________________________________��
(3)���Լ�1���Լ�2����ϡ���ᡣ
�ټ�������D����Һ�н������ӵķ�����_______________________________________��
��д��D��E��Ӧ�����ӷ���ʽ______________________________________________ __��
__��
��ij��Ч��ˮ������Y(OH)SO4�ۺϵõ��ġ���ҵ����E��ϡ�������������Ϊԭ�����Ʊ�Y(OH)SO4����Ӧ����NO���ɣ��÷�Ӧ�Ļ�ѧ����ʽ��(������ƽ)��
___________________________________________________________________________��
�ο��𰸣���1��
 ��2��NaOH(��KOH)(1��)��
��2��NaOH(��KOH)(1��)��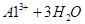 ?
?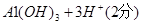
��3����ȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ�� ��ɫ����֤��ԭ��Һ�к���Fe3+��2�֣�
��ɫ����֤��ԭ��Һ�к���Fe3+��2�֣�
�� ��1�֣�
��1�֣�
��
�����������
�����Ѷȣ�һ��
3������� ��A��B��C��D��E��F��G��H��I���ֳ������ʣ����ǵ�ת����ϵ����Ӧ����δע������ͼ��ʾ��������AΪҺ̬��DΪ��̬��B��C��E��GΪ��̬��C����ʹ������ľ����ȼ��������B��C��DΪ���ʣ�FΪ����ɫ��ĩ״�����I����ɫ��ӦΪ��ɫ��
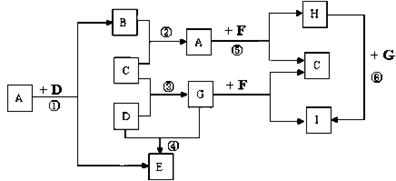
��ش𣺣�1��д��F�ĵ���ʽ?����2��G�Ľṹʽ��?��
��3����Ӧ����?��Ӧ������ȡ����ߡ����ȡ���
��4��д����Ӧ�ݵĻ�ѧ��Ӧ����ʽ?
��5��B��C�����ѱ�Ӧ��������ɴ���ȼ�ϵ���У���ͼ��ʾ������B���ɼ���Ҳ�����ȼ�ϵ�أ������缫���ɶ����̼���ɣ����õ�ع���ʱ��
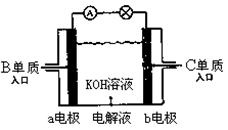
��b�缫������Һ��pH��?���������С�������䡱����
��a�缫�ϵĵ缫��ӦʽΪ��???��
��6���ڱ�״���£�����3��36L����Gͨ��50mL 4mol/L��H��Һ�У���һ�����ӷ���ʽ��ʾ����̣�?
�ο��𰸣���ÿ��2�֣���14�֣���1��?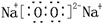 ?��2��O��C��O��3������
?��2��O��C��O��3������
��4��2Na2O2+2H2O��4NaOH+O2 ��?��5�������� CH4��10OH����8e����CO32-+7H2O?
��6��4OH��+3CO2��H2O+CO32-+2HCO3-
���������������AΪҺ̬����A������ˮ��FΪ����ɫ��ĩ״���������Fˮ�������ơ�ˮ�������Ʒ�Ӧ�����������ƺ�������CΪ��̬�����C��������Fˮ�������ơ�G����̬��Ҳ�ܺ������Ʒ�Ӧ������������G��CO2��I��̼���ơ�C��B��Ӧ����ˮ����B��������DΪ��̬���ܺ�������Ӧ����CO2������D��̼��̼��CO2��Ӧ����CO����E��CO��������̼��ˮ������Ӧ����������CO��
��1���������Ƶĵ���ʽ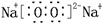 ��
��
��2��CO2�Ľṹʽ��O��C��O��
��3��̼��CO2��Ӧ�����ȷ�Ӧ������Ӧ�������ȷ�Ӧ��
��4����Ӧ�ݵĻ�ѧ��Ӧ����ʽ2Na2O2+2H2O��4NaOH+O2 ����
��5����b�缫ͨ������������b�缫�������������õ����ӣ�������ԭ��Ӧ���缫��Ӧʽ��O2��4e����H2O��4OH��������b�缫������Һ��pH������
�ڼ����ڸ���ͨ�룬ʧȥ���ӣ�����������Ӧ����a�缫�ϵĵ缫��ӦʽΪCH4��10OH����8e����CO32-+7H2O��
��6��3.36L����CO2�����ʵ�����3.36L��22.4L/mol��0.15mol���������Ƶ����ʵ�����0.05L��4mol/L��0.2mol��������������̼�����ƺ�̼���ơ�����CO2���������Ƶ����ʵ���֮����3:4�����Ը÷�Ӧ�����ӷ���ʽ��4OH��+3CO2��H2O+CO32-+2HCO3-��
�������������е��Ѷȵ����⣬�����ۺ���ǿ����ѧ����˼ά����Ҫ��ߣ�����������ѧ���������������ͷ�ɢ˼ά����������������Ҫע����ǻ�ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�����
4������� ��10�֣�ÿ��2�֣���֪Cr(OH)3�ڼ��Խ�ǿ����Һ�н�����[Cr(OH)4]�D�����Ļ������ж�������+6�۸���ǿ�����ԣ��䶾����+3�۸����Ե�100������ˣ�����Ժ����ķ�ˮ���д������ɲ����������ַ�����
��ԭ�������Խ�������FeSO4�Ƚ�+6�۸���ԭ��+3�۸���
�����������£�

�й�������ȫ������pH���±���
��1��д��Cr2O72����FeSO4��Һ�����������·�Ӧ�����ӷ���ʽ________________________________________________________��
��2���ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+�����������������
���ڲ������п����ڵ�����ҺpH���Լ�Ϊ��_____________������ţ���
A��Na2O2? B��Ca(OH)2? C��Ba(OH)2? D��NaOH
��ʱ������Һ��pH��Χ��____________������ţ���ѡ�
A��12��14? B��10��11? C��6��8? D��3��4
��3�����������4.0��10-3mol��L-1��AgNO3��4.0��10-3mol��L-1��K2CrO4��Һ���������Ag2CrO4������Ksp(Ag2CrO4)=9.0��10-12������д����ʾAg2CrO4�ܽ�ƽ��ķ���ʽ��2�֣�������Ҫд��������Ag2CrO4����ԭ��ļ�����̣�2�֣���
�ο��𰸣���ÿ��2�֣��ܼ�10�֣�
��1��Cr2O72�� + 6Fe2+ +14H+ ="=" 2Cr3+ + 6Fe3+ + 7H2O��
��2��B?C
��3��Ag2CrO4 (s)  ?2Ag+(aq) + CrO42��(aq)
?2Ag+(aq) + CrO42��(aq)

�������������1�������������л�ԭ�ԣ�Cr2O72-��ǿ�����ԣ������ܷ���������ԭ��Ӧ�����������ӱ����������������ӣ�Cr2O72-����ԭΪCr3+����Ӧ����ʽΪCr2O72-+6Fe2++14H+�T2 Cr3++6Fe3++7H2O��
�ʴ�Ϊ��Cr2O72-+6Fe2++14H+�T2 Cr3++6Fe3++7H2O��
��2��A��Na2O2��ǿ�����ԣ��ܰ�Cr3+������Cr6+���Ӷ��ò���Cr��OH��3���ʴ���
B��Ca��OH��2�� D��NaOHʹFe3+��Cr3+�������������������û�����������������ɣ�����ȷ��
C��Ba��OH��2������������ܲ������ᱵ�������������ʣ��ʴ���
�ں�����ˮ�м���FeSO4���ٵ���pH��ʹFe3+��Cr3+�������������������û������������������������Һ��PHӦ����5.6С��9������B��ȷ��
�ʴ�Ϊ��B��C��
���������⿼�������ӷ���ʽ����д���ѶȲ���ע�����е�ͼʾ�ͱ������ṩ����Ϣ����������������������Ϣ����Ĺؼ���
�����Ѷȣ���
5������� ͼ�Т١���ֱ�����йط�Ӧ�е�һ�����ʣ����Ǿ�����ѧ��ѧ�г������ʡ���֪�١��ۺ͢ޡ����зֱ���ͬһ��Ԫ�ء�
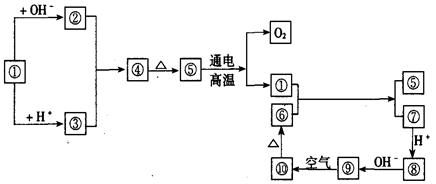
(1)�ֱ�д���١��ܡ���Ļ�ѧʽ�����ӷ��ţ�
��_________����_________����_________��
(2)д�����з�Ӧ����ʽ�������ӷ�Ӧ��д�����ӷ���ʽ��
�٣�OH����________________________________�ݣ���________________________________�٣��ޡ���________________________________
�ᣫ������________________________________
�ο��𰸣�(1)��Al?��Al(OH)3?��Fe2��
(2)2A1��2OH����2H2O=2AlO2����3H2 ��
ͨ��
����������ݣ���O2�����١�����ѧ��ѧ��ͨ��ֽ�����O2�Ļ����ﳣ����ΪAl2O3���ټ�����OH����Ӧ���ɢڣ�������H����Ӧ���ɢۣ��Ң١��ۺ�ͬһ��Ԫ�أ��ں͢��ܷ�Ӧ���ɢܣ����Խ�һ����֪��ΪA1����ΪAlO2������ΪA13������ΪA1(OH)3����ΪAl2O3���ɢࡪ���ᡪ�����֪��Ϊ������������ڿ����б���������ѧ��ѧ�г�������Fe(OH)2�����ΪFe(OH)3�����ȷֽ�����ΪFe2O3���֢�+���ڸ��������·�����Ӧ�����dz��������ȷ�Ӧ�����ԣ���һ��֤����ΪA1����ΪFe2O3�����ΪFe����ΪFe2����
�����Ѷȣ�һ��