| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《氧化性和还原性强弱的比较》高频考点强化练习(2017年最新版)(十)
参考答案:A 本题解析:在氧化还原反应中,铁元素化合价升高,作还原剂,A项正确;SO2中S元素由+4价降低到0价,得电子作氧化剂,被还原,B项错误;根据氧原子守恒,SO2转化为S,氧原子数减少,MFe2OX转化为MFe2Oy,氧原子数必然增加,x<y,C项错误;根据氧化剂的氧化性大于氧化产物的氧化性,氧化性SO2 > MFe2Oy,D项错误;选A。 本题难度:一般 3、实验题 (13分)某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示: |
参考答案:(1)液柱高度保持不变 ;安全瓶,防止倒吸;NaOH(各1分)(2)C(1分);
(3)Fe2+、SO42-(1分);(4)方案①(2分);SO2、Fe2+都能使酸性高锰酸钾褪色(2分)
(5)D中蓝色褪去(2分) I2+SO2+2H2O=4H++2I-+ SO42- (2分)
本题解析:(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若液柱高度保持不变,则整个装置气密性良好。装置E的作用是安全瓶,防止倒吸现象的发生;由于SO2是大气污染物,直接排放会造成大气污染,所以在装置F中为NaOH溶液,用以吸收多余的SO2。(2)装置B的作用之一是观察SO2的生成速率,为了减少SO2在其中的溶解,同时防止引入杂质气体,A SO2容易溶于蒸馏水,会消耗气体,错误;B.饱和Na2SO3溶液与SO2和水反应产生NaHSO3,导致气体被消耗,错误;C.饱和NaHSO3溶液不能与SO2发生反应,气体也不能溶解,正确;D.由于酸性H2SO3>H2CO3,所以SO2与发生饱和NaHCO3溶液反应会产生CO2,产生杂质气体,错误。所以在B中的液体最好选择饱和NaHSO3溶液,选项是C;(3)SO2气体与Fe3+发生反应:SO2+2Fe3++2H2O=4H++SO42-+2Fe2+;SO2被氧化为SO42-,Fe3+被还原为Fe2+;(4)方案①:KMnO4有强的氧化性,能够把Fe2+或SO2氧化,而其本身被还原为无色的Mn2+,所以往第一份试液中加入KMnO4溶液,紫红色褪去不能证明SO2与Fe3+发生了氧化还原反应,错误;方案②:往第一份试液加入KSCN溶液,不变红,证明无Fe3+,再加入新制的氯水,溶液变红,说明Cl2与Fe2+反应产生了Fe3+,能证明SO2与Fe3+发生了氧化还原反应,正确;方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀,就证明在溶液中含有SO42-,从而证明证明SO2与Fe3+发生了氧化还原反应,正确。(5)若I-的还原性弱于SO2,则会发生反应:l2+SO2+2H2O=H2SO4+2Hl,含有淀粉的碘水溶液的蓝色褪去,该反应的蜡烛方程式是I2+SO2+2H2O=4H++2I-+ SO42- ;
考点:考查装置气密性的检查、仪器的作用、试剂的选择、物质性质的比较及检验、方程式的书写的知识。
本题难度:困难
4、实验题 (10分)某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
(1)提出问题:Fe3+、Br2哪一个的氧化性更强?
(2)猜想
①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含
(填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含___所致。
3)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。供选用的试剂:
A.酚酞试液
B.CCl4
C.无水酒精
D.KSCN溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| | 选用试剂 | 实验现象 |
| 方案1 | | |
| 方案2 | | |
参考答案:(共10分)(2)①Br2 ②Fe3+(每空1分)
(3)注:两方案不分顺序 (试剂代号写成大写字母不给分)(每空1分)
选用试剂
实验现象
方案1
d
溶液呈血红色
方案2
b
CCl4层呈无色
(4)①2Fe2++Br2=2Fe3++2Br- ②2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl?
(第(4)小题每空2分)
本题解析:(2)Fe2+的颜色:浅绿色,Fe3+的颜色:棕黄色,溴水的颜色:橙黄色,根据题意在足量的氯化亚铁溶液中加入l-2滴溴水,若Fe3+氧化性强于Br2,则不发生氧化还原反应,溶液呈黄色是由加入溴水引起的;如果Br2氧化性强于Fe3+,则发生反应:2Fe2++Br2
本题难度:困难
5、选择题 SO42-和S2O82-结构中,硫原子均位于氧原子组成的四面体的中心,且所有原子的最外层电均满足8电子结构,下列说法正确的是
[? ]
A SO42-的电子式为 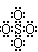
B S2O82-中没有非极性键
C S2O82-比SO42-稳定
D S2O82-有强氧化性
参考答案:D
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《大气污染与治理》.. | |