微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (20分)工业上常利用含硫废水生产Na2S2O3?5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
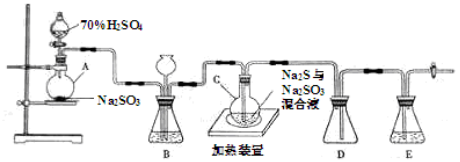
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)?(I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l)?(II)
S(s)+Na2SO3(aq) Na2S2O3(aq)?(III)
Na2S2O3(aq)?(III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若?,则整个装置气密性良好。装置D的作用是?
??。装置E中为?溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为?。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择?。
a.蒸馏水? b.饱和Na2SO3溶液
c.饱和NaHSO3溶液? d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是?。已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是?。反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器含有?。
a.烧杯? b.蒸发皿? c.试管? d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3?5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:
?。
已知Na2S2O3?5H2O遇酸易分解:S2O32?+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液
参考答案:(1)液注高度保持不变;防止倒吸;NaOH(合理即得分)
(2)2:1
(3)c;控制滴加硫酸的速度(合理即得分);溶液变澄清(或浑浊消失);a、d
(4)取少量产品溶于足量稀盐酸,静置,取上层清液(或过滤,取滤液),滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质。(合理即得分)
本题解析:(1)液注高度保持不变,说明气密性良好;D为安全瓶,防止倒吸;装置E起到吸收尾气中SO2、H2S的作用,可选用NaOH溶液。
(2)根据题目所给3个反应,可得出对应关系:2Na2S ~ 2H2S ~ 3S ~3 Na2SO3,2Na2S反应时同时生成2Na2SO3,还需要1Na2SO3,所以烧瓶C中Na2S和Na2SO3物质的量之比为2:1
(3)SO2易溶于水,能与Na2SO3溶液、NaHCO3溶液反应,但在NaHSO3溶液中溶解度较小,所以c项正确;SO2为70% H2SO4与Na2SO3反应制取,所以为使SO2缓慢进入烧瓶C,采用的操作是控制滴加硫酸的速度;反应III 固体S反应,所以烧瓶C中反应达到终点的现象是溶液变澄清(或浑浊消失);蒸发皿和试管可以直接加热,烧杯和锥形瓶加热时需要使用石棉网,故a、d正确。
(4)加入盐酸,Na2S2O3反应S沉淀,所以静置后取上层清液,滴加BaCl2溶液,若出现沉淀则说明含有Na2SO4杂质。
本题难度:一般
2、选择题 只用一种试剂可以区别NH4Cl、MgCl2、FeCl2、AlCl3、(NH4)2SO4五种溶液,这种试剂是( )
A.Ba(OH)2溶液
B.NaOH溶液
C.硫酸
D.KNO3溶液
参考答案:A.NH4Cl、MgCl2、FeCl2、AlCl3、(NH4)2SO4五种溶液分别与Ba(OH)2溶液反应,现象依次为:刺激性气体、白色沉淀、白色沉淀变为灰绿色最后变为红褐色、白色沉淀后溶解、白色沉淀和刺激性气体,现象不同,能区别,故A正确;
B.NH4Cl、(NH4)2SO4与NaOH反应均生成刺激性气体,不能区分,故B错误;
C.五种物质与硫酸均不反应,不能区分,故C错误;
D.五种物质与硝酸钾均不反应,不能区分,故C错误;
故选A.
本题解析:
本题难度:简单
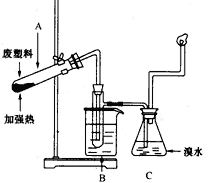
3、实验题 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图所示。 加热聚丙烯废塑料得到的产物如下表所示:
 ?
? 
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。 A中残留物聚乙炔写出反应②、③的化学方程式_____________;____________ 。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有__________ 种。
(3)锥形瓶C中观察到的现象是____________ ,经溴水充分吸收后,剩余气体经干燥后平均相对分子质量为________________ 。
(4)写出C中逸出的气体在工业上的两种用途___________ 、___________。
参考答案:
(1)CaC2+2H2O→Ca(OH)2+C2H2 ;CH≡CH→
(2)4
(3)棕黄色溶液变无色(或溴水褪色);4.8
(4)合成氨原料; 作燃料或有机化工原料
本题解析:
本题难度:一般
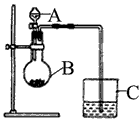
4、实验题 某同学想通过比较两种最高价氧化物水化物的酸性强弱来验证硫与碳的非金属性的强弱,他采用了下图所示的装置。
请回答:
(1)仪器A的名称是___________ ,应盛放下列药品中的_____________ 。
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
(2)仪器B的名称是___________ ,应盛放下列药品中的_____________ 。
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
(3)仪器C中应盛放的药品是______________ ,如果看到的现象是____________ ,证明B中发生反应生成了___________ ,即可说明____________比____________酸性强。 B中发生反应的离子方程式为___________ 。
参考答案:(1)分液漏斗 ;a
(2)圆底烧瓶 ;d
(3)澄清石灰水;石灰水变浑浊 ;CO2 ;硫酸 ;碳酸 ;CO32- +2H+ === CO2↑+H2O
本题解析:
本题难度:一般
5、选择题 某学生的实验报告所列出的下列数据中合理的是(?)
A.用1mol的醋酸溶液和1.01mol的氢氧化钠溶液做中和热实验测得中和热的数值为57.3KJ/mol
B.通过实验得知在常温常压下,12g固体C和32g气体O2所具有的总能量一定大于44g气体CO2所具有的总能量
C.室温下,用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.7mL
参考答案:B
本题解析:醋酸是弱酸,电离时吸热,所以醋酸和氢氧化钠溶液生成1mol水放热小于57.3kJ,A错误;炭与氧气反应生成二氧化碳放热,B正确;广泛pH试纸测得pH值为整数,C错误;滴定管的精确度为0.01mL,D错误。
点评:稀溶液中,强酸和强碱生成1mol水放热57.3kJ。若浓硫酸与氢氧化钠溶液生成1mol水放热大于57.3kJ/mol;若醋酸与氢氧化钠溶液或盐酸与氨水分别生成1mol水放热小于57.3kJ。
本题难度:简单