微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 如图表示在没有通风橱的条件下制备氯气时设计的装置,图中a.b是可控制的弹簧铁夹.(氯气在饱和氯化钠溶液中的溶解度较小.)
(1)仪器A的名称是______;水槽中应盛放的是______;烧杯中盛放的是______;烧瓶中反应的化学方程式______;
(2)在收集氯气时,应______.(填如何控制a.b)
(3)若要制得标准状况下的Cl20.672L,理论上需要MnO2的质量是______g被氧化盐酸的物质的量______mol
(4)若要增大新制氯水中HClO的浓度可加入______
A.食盐B.水C.CaCO3D.NaOH.

参考答案:(1)根据仪器特点可知A为分液漏斗;因为氯气有毒,可污染空气,要进行尾气吸收,并且氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以常用氢氧化钠溶液吸收尾气中,烧杯中盛放氢氧化钠溶液收,集完毕,关闭a,打开b,多余的气体通入氢氧化钠溶液进行吸收,防止污染空气;Cl2+2NaOH=NaCl+NaClO+H2O;氯气在饱和氯化钠溶液中的溶解度较小,实验室常用排饱和食盐水法收集氯气,实验室常用二氧化锰和浓盐酸在加热条件下生成氯气,反应的化学方程式为MnO2+4HCl△.MnCl2+Cl2↑+2H2O,
故答案为:分液漏斗;饱和食盐水;氢氧化钠溶液;MnO2+4HCl△.MnCl2+Cl2↑+2H2O;
(2)氯气在饱和氯化钠溶液中的溶解度较小,实验室常用排饱和食盐水法收集氯气,收集时,应关闭b,打开a,故答案为:关闭b,打开a;
(3)n(Cl2)=VVm=0.672L22.4L/mol=0.03mol;
生成0.03molCl2参加反应的HCl的物质的量为x,反应的二氧化锰物质的量为Y;
MnO2+4HCl△.MnCl2+Cl2↑+2H2O
1 4 1
y x 0.03mol
x=0.12mol
y=0.03mol
被氧化的HCl的物质的量=0.12mol×12=0.06mol.
理论上反应的二氧化锰质量=0.03mol×87g/mol=2.61g;
故答案为:2.61;0.06;
(4)氯水中氯气和水反应生成盐酸和次氯酸,Cl2+H2O=HClO+HCl,
A、食盐加入,增大氯离子浓度,平衡左移,次氯酸浓度减小,故A不符合;
B、水加入平衡状态物质浓度减小,次氯酸浓度减小,故B不符合;
C、加入碳酸钙和盐酸反应促进平衡正向进行,次氯酸浓度增大,故C符合;
D、加入氢氧化钠会和盐酸、次氯酸发生反应,次氯酸浓度减小,故D不符合;
故答案为:C.
本题解析:
本题难度:一般
2、计算题 实验室用8.7g的MnO2与50ml足量的浓盐酸制取氯气
(1)写出制取氯气的反应方程式
(2)求生成氯气的体积(标准状况)
(3)若向反应后的剩余溶液中,加入足量AgNO3溶液,生成沉淀57.4g,求原浓盐酸的物质的量浓度。
参考答案:(1)MnO2+4HCl MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)2.24L
(3)12mol・L-1
本题解析:
本题难度:一般
3、实验题 I. 合成氨工业对化学的国防工业具有重要意义。写出氨的两种重要用途_________________________。
II. 实验室制备氨气,下列方法中适宜选用的是 ___________________。
① 固态氯化铵加热分解
② 固体氢氧化钠中滴加浓氨水
③ 氯化铵溶液与氢氧化钠溶液共热
④ 固态氯化铵与氢氧化钙混合加热
III. 为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图中夹持装置均已略去)。
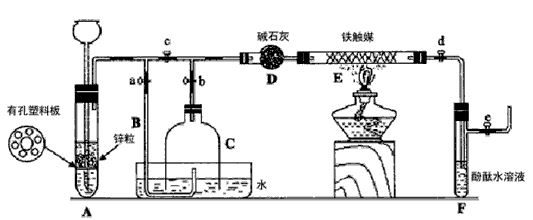
[实验操作]
① 检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气发生。在F出口处收集氢气并检验其纯度。
② 关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③ 用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红
。回答下列问题:
(1)检验氢气纯度的目的是______________。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是____________ ,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是_____________ ,C瓶内气体的成份是________________。
(3)在步骤③中,先加热铁触媒的原因是_________。反应管E中发生反应的化学方程式是________。
参考答案:I. 制化肥、制硝酸
II. ②④
III. (1)排除空气,保证安全
(2)锌粒与酸脱离 ;尽量增大氢气的浓度以提高氮气的转化率;N2 、H2
(3)铁触媒在较高温度时活性增大,加快氨合成的反应速率 ;
本题解析:
本题难度:困难
4、选择题 下列气体的制备可采用下图装置的是
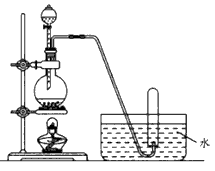
[?]
A.铜与浓硝酸反应制NO2
B.铜与稀硝酸反应制NO
C.加热浓氨水法制氨气
D.大理石与硫酸反应制CO2
参考答案:B
本题解析:
本题难度:简单
5、简答题 氨在人类的生产和生活中有着广泛的应用.某化学兴趣小组利用图一装置探究氨气的有关性质.
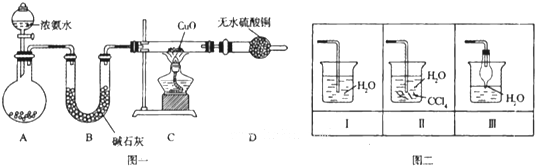
(1)装置A中烧瓶内试剂可选用______(填序号).B的作用是______.
a.碱石灰b.浓硫酸c.生石灰d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先______(填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为______.该反应证明氨气具有______性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是______(填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,所得溶液的物质的量浓度为______mol/L.
参考答案:(1)装置A是制备氨气的发生装置,浓氨水滴入固体碱石灰或氧化钙或固体氢氧化钠都可以生成氨气,浓硫酸和氨气发生反应,氨气易溶入烧碱溶液,不选择浓硫酸、氢氧化钠溶液制备氨气,所以装置A中试剂为:a.碱石灰,c.生石灰;B装置中的碱石灰是吸收水蒸气,干燥氨气的作用,
故答案:ac;干燥氨气;
(2)连接好装置并检验装置的气密性后,装入药品,打开旋塞逐滴向圆底烧瓶中加入氨水发生反应生成氨气,故答案为:Ⅰ;
(3)实验中观察到C中CuO粉末变红证明生成铜,D中无水硫酸铜变蓝生成水,并收集到一种单质气体,依据氧化还原反应分析,氧化铜氧化氨气为氮气,氧化铜被还原为铜,反应的化学方程式为:3CuO+2NH3△.3Cu+N2+3H2O;氮元素化合价升高为0价,做还原剂具有还原性,
故答案为:3CuO+2NH3△.3Cu+N2+3H2O;还原性;
(4)氨气极易溶于水尾气吸收需要防止倒吸,图二中能用来吸收尾气的装置是Ⅱ、Ⅲ,装置Ⅰ易发生倒吸,故答案为:Ⅱ、Ⅲ;
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成0.5L溶液,溶质氨气物质的量为0.1mol,所得溶液的物质的量浓度=0.1mol0.5L=0.2mol/L,
故答案为:0.2.
本题解析:
本题难度:一般