微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分)某课外活动小组为了测定某氯化锶(SrCl2)样品的纯度,设计了如下方案:
称取1.0g样品溶解于适量水中,向其中加入含AgNO32.38g的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应生成沉淀的离子),Cl―即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。请回答下列问题:
(1)滴定反应达到终点的现象是?;
(2)实施滴定的溶液以呈?(选填“酸性”、“中性”或“碱性”)为宜,加
?(填化学式)试剂可达到这一目的;
(3)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n (Clˉ)的测定结果?(选填“偏高”、“偏低”或“无影响”);
(4)到达终点后,则必须轻轻摇动锥形瓶,(此时不得剧烈摇动)以减少误差,否则这种误差会使n (Clˉ)测定值偏低,这说明两者的溶解度:AgCl ??AgSCN(填“>”或“<”);
(5)若以Fe3+的溶液作指示剂,用NH4SCN标准溶液滴定剩余的AgNO3时,用去上述浓度的NH4SCN溶液20.0mL,则原氯化锶样品的纯度为?。
参考答案:(1)溶液由无色变为血红色?(2)酸性?HNO3
(3)偏高?(4)>?(5)79.5%
本题解析:(1)由于铁离子能和NH4SCN反应使溶液显红色,所以终点时的现象是溶液由无色变为血红色。
(2)由于在碱性溶液中铁离子和银离子易形成氢氧化物沉淀,所以溶液应该显酸性。由于不能引入杂质,所以易用硝酸酸化。
(3)沉淀表面会吸附部分Ag+,所以会导致查质量增加,从而导致测定结果偏高。
(4)这种误差会使n (Clˉ)测定值偏低,这说明沉淀会转化为AgSCN沉淀,因此氯化银的溶解度大于AgSCN的。
(5)消耗0.2mol/L的NH4SCN的物质的量是0.004mol,硝酸银是2.38g÷170g/mol=0.014mol,所以和氯离子反应的硝酸银是0.014mol-0.004mol=0.01mol,因此氯化锶的质量是0.005mol×156g/mol=0.795g,所以原氯化锶样品的纯度为79.5%。
本题难度:一般
2、实验题 碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y·zH2O。某校化学兴趣小组欲测定其化学式,实验设计如下:
实验I:称取一定质量的A,加热分解至恒重。
实验Ⅱ:称取一定质量的A与足量的酸反应,测量生成CO2气体的质量。
可供选择的仪器和药品如图所示:(酸溶液限选6mol/LHCl或6mol/LH2SO4,其它试剂任选。)
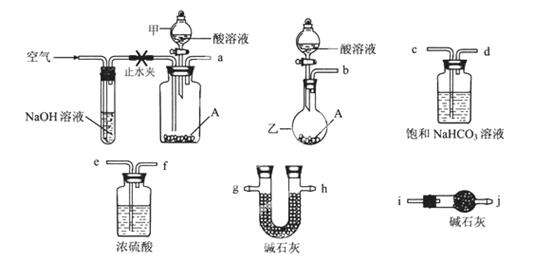
回答下列问题:
(1)仪器乙的名称为________。
(2)请选择必要的装置完成实验II,正确的连接顺序为________ (按气流方向,用接口字母表示);选用的酸溶液是________。
(3)有人提出不采用实验I,可在实验II结束后,在A完全反应后所得溶液中滴加足量的氨水,用无灰滤纸过滤,用蒸馏水洗涤反应容器2?3次,将洗涤液过滤,洗涤沉淀2?3次,将附着沉淀的滤纸放到坩埚中加热分解至恒重。判断沉淀已洗涤干净的方法是_________________,实际上未采用该方案的原因是不符合实验设计的________原则(填字母编号)。
A.科学性
B.安全性
C.可行性
D.简约性