| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《弱电解质电离平衡》答题技巧(2017年最新版)(二)
参考答案: 本题解析: 本题难度:一般 3、选择题 某温度下,向一定物质的量浓度的盐酸和醋酸中分别加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示.根据图判断下列说法正确的是( ) |
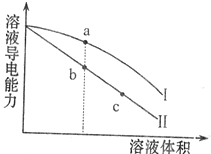
参考答案:D
本题解析:
本题难度:简单
4、选择题 已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是
A.该溶液的c(H+) = 10-4 mol/L
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.将此溶液加水稀释后,电离的HA分子数大于0.1%
参考答案:B
本题解析:A、该溶液中的氢离子浓度为0.1×0.1%= 10-4 mol/L ,故正确,不选A;B、升高温度,平衡正向移动,氢离子浓度增大,pH减小,故选B;C、根据电离平衡常数的计算公式,电离平衡常数=(0.1×0.1%)(0.1×0.1%)÷0.1=1×10-7,故正确,不选C;D、加水稀释后,电离平衡正向移动,电离的分子比原来多,故正确,不选D、
考点:弱电解质的电离。
本题难度:一般
5、选择题 能说明醋酸是弱电解质的是( )
①醋酸溶液中加入醋酸钠固体pH变大
②0.1mol?L-1的醋酸钠溶液的pH约为9
③可以用食醋清除热水瓶内的水垢
④pH=2的醋酸溶液稀释1000倍后pH小于5.
A.①③④
B.①②④
C.②④
D.①②③④
参考答案:①醋酸溶液中加入醋酸钠固体pH变大,说明醋酸钠是强碱弱酸盐,所以能说明醋酸是弱电解质,故正确;
②0.1mol?L-1的醋酸钠溶液的pH约为9,溶液呈碱性,所以说明醋酸钠是强碱弱酸盐,则能说明醋酸是弱电解质,故正确;
③食醋能清除水垢,说明醋酸的酸性比碳酸强,但不能说明醋酸是弱电解质,故错误;
④pH=2的醋酸溶液稀释1000倍后,如果醋酸是强电解质,则稀释后溶液的pH=5,实际上溶液的pH小于5,则说明醋酸是弱电解质,故正确;
故选B.
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学试题《硝酸》试题特训(2.. | |