| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《离子方程式的书写及正误判断》在线测试(2017年最新版)(六)
参考答案:D 本题解析:A错,溶液中碳酸氢根离子也要与氢氧根离子反应;B错,电荷未守恒,正确为2Fe2++Cl2 本题难度:一般 2、选择题 在给定的四种溶液中,加入以下各种离子后,各离子能在原溶液中大量共存的有 |
参考答案:
本题解析:
本题难度:一般
3、填空题 (9分)某强酸性溶液X中可能含有H+、A13+、NH4+、Fe2+、CO32-、SO42-、C1-、NO3- 中的若干种。某研究性小组为了探究其成分,进行了如下实验: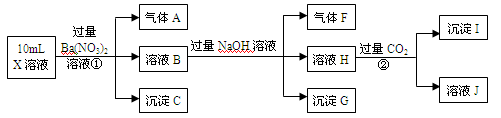
请回答下列问题:
(1)沉淀C的化学式为 ,气体A的化学式为 。
(2)写出向溶液H中通入过量CO2气体生成沉淀I的离子方程式: 。
(3)通常可以利用KClO在KOH溶液中氧化沉淀G来制备一种新型、高效、多功能水处理剂K2MO4。(M为G中的一种元素,K2MO4易溶于水)请写出制备过程中的离子方程式(M用具体的元素符号表示) 。
(4)无法确定的离子是 ,请设计实验验证该离子是否存在的方法 。
参考答案:(1)BaSO4 NO (各1分)(2)[Al(OH)4]-+CO2 ==Al(OH)3↓+HCO3-(2分)
(3)3ClO-+2Fe(OH)3+4OH-==2FeO42-+3Cl-+5H2O(2分)
(4)C1-(1分) 取少量的B溶液于试管中,(滴加稀硝酸酸化),滴加AgNO3溶液,若有白色沉淀生成,证明含有C1-;若无白色沉淀生成,证明不含C1-(2分)
本题解析:溶液显强酸性,则一定不存在碳酸根离子,存在氢离子。混合液中加入过量硝酸钡溶液,产生气体A、溶液B和沉淀C,这说明溶液中一定有还原性离子在酸性溶液中被硝酸根氧化,因此一定含有亚铁离子。在强酸性溶液中硝酸根能氧化亚铁离子,则硝酸根一定不存在,气体A是NO,C是硫酸钡,所以含有硫酸根离子。B中加入过量的氢氧化钠溶液又产生气体F、溶液H和沉淀G,则F一定是氨气,即含有铵根。G中一定存在氢氧化铁。H中加入过量的CO2沉淀溶液J和沉淀I,则I应该是氢氧化铝,即H中含有偏铝酸钠,因此原溶液中含有铝离子。
(1)根据以上分析可知沉淀C的化学式为BaSO4,气体A的化学式为NO。
(2)向溶液H中通入过量CO2气体生成沉淀I的离子方程式为[Al(OH)4]-+CO2==Al(OH)3↓+HCO3-。
(3)次氯酸钾氧化氢氧化铁生成高铁酸钾的离子方程式为3ClO-+2Fe(OH)3+4OH-=2FeO42-+3Cl-+5H2O。
(4)根据以上分析可知无法确定的离子是C1-。由于溶液中的硫酸根离子能干扰氯离子的检验,则验证该离子是否存在的方法为取少量的B溶液于试管中,(滴加稀硝酸酸化),滴加AgNO3溶液,若有白色沉淀生成,证明含有C1-;若无白色沉淀生成,证明不含C1-。
考点:考查离子共存与检验的应该分析判断
本题难度:困难
4、选择题 下列离子方程式中正确的是 ( )
A.在漂白粉的溶液中通入一定量的二氧化硫气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
B.向溴化亚铁溶液中通入过量氯气:Fe2++2Br-+2Cl2=Fe3++Br2+4Cl-
C.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
D.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-→BaSO4↓+2H2O
参考答案:C
本题解析:略
本题难度:一般
5、选择题 下列离子方程式中,不正确的是
A.向FeCl2溶液中通入 Cl2 2Fe2+ + Cl2= 2Fe3+ + 2Clˉ
B.FeCl3溶液跟过量氨水 Fe3+ + 3NH3?H2O = Fe(OH)3↓ + 3NH4+
C.碳酸氢钙溶液跟稀硝酸Ca(HCO3)2 + 2H+= Ca2+ + 2H2O + 2CO2↑
D.钠与水的反应2Na + 2H2O = 2Na+ + 2OH- + H2↑
参考答案:C
本题解析:A.向FeCl2溶液中通入Cl2生成氯化铁,离子方程式正确,A正确;B.FeCl3溶液跟过量氨水反应生成氢氧化铁沉淀和氯化铵,离子方程式正确,B正确;C.碳酸氢钙溶液跟稀硝酸反应生成硝酸钙、水和CO2,离子方程式为HCO3-+ H+=H2O + CO2↑,C错误;D.钠与水的反应生成氢氧化钠和氢气,离子方程式正确,D正确,答案选C。
考点:考查离子方程式的正误判断
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《炔烃的性质.. | |