��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �����ͼ��ѡ�ñ�Ҫ��װ�ý��е�ⱥ��ʳ��ˮ��ʵ�飬Ҫ��ⶨ�����������������������������

��1��A�������ĵ缫��Ӧʽ��______B�������ĵ缫��Ӧʽ��______
��2�������������ʵ��װ��ʱ�����ӿڵ���ȷ����˳��Ϊ��A��______��______��______��B��______��______��______��
��3��֤����������Cl2��ʵ��������______��
��4����֪�����ò�����H2�����Ϊ44.8mL���Ѿ�����ɱ�״������������Һ�����Ϊ50mL����ʱ��Һ��NaOH�����ʵ���Ũ��Ϊ______��
��5����һ�͵�ⱥ��ʳ��ˮ����ת���෴��װ���У�һ��ͨ����飬��һ��ͨ���������������ҺΪKOH��Һ�������ķ�ӦʽΪ______�����ķ�ӦʽΪ______��
�ο��𰸣���1����ⱥ��ʳ��ˮ�������ʱ��A���ǻ��ý����缫��ӦΪ�������������������ӵõ��ӣ�
��ӦʽΪ��2H++2e-=H2����B����������������������ʧ���ӵĹ��̣���Ӧʽ�ǣ�2Cl--2e-=Cl2����
�ʴ�Ϊ��2H++2e-=H2����2Cl--2e-=Cl2����
��2���ⶨ�������������������ˮ�������������Ƕ̽�����������A��G����װ�е��۵⻯����Һ��ϴ��ƿ��������ʱ������Ҫ�����̳�������B��D������Ҫ����β����������E��C���ʴ�Ϊ��G��F��H��D��E��C��
��3���������Խ��⻯���еĵ��û����������ɵĵⵥ�ʿ�ʹʹʪ��ĵ��۵⻯����ֽ����������֤����������Cl2��ʵ��������ʪ��ĵ��۵⻯����ֽ�������ʴ�Ϊ��ʪ��ĵ��۵⻯����ֽ������
��4�����ݵ�ⱥ��ʳ��ˮ�ĵ��ԭ������ʽ��2NaCl+2H2O?ͨ��?.?2NaOH+H2��+Cl2������������H2�����Ϊ44.8mL0.002molʱ�������������Ƶ����ʵ���Ϊ0.004mol��������Һ��NaOH�����ʵ���Ũ��=0.004mol0.05L=0.08mol/L��
�ʴ�Ϊ��0.08mol/L��
��5���ڼ���ȼ�ϵ���У�������ʧ���ӵ���ȼ�ϼ��飬�ڼ��Ի����µ缫��ӦΪ��CH4-8e-+10OH-=CO32-+7H2O�������ϵõ��ӵ����������ڼ��Ի����µ缫��ӦΪ��2O2+8e-+4?H2O=8OH-��
�ʴ�Ϊ��CH4-8e-+10OH-=CO32-+7H2O��2O2+8e-+4?H2O=8OH-��
���������
�����Ѷȣ�һ��
2��ѡ���� �����ϲ������Ϊԭ��صĻ�ѧ��Ӧ�ǣ�������
A��CH4+2O2
CO2+2H2O
B��AgNO3+NaCl=NaNO3+AgCl
C��2H2+O22H2O
D��2FeCl3+Fe�T3FeCl2
�ο��𰸣�A���÷�Ӧ�����Է���������ԭ��Ӧ����������Ƴ�ԭ��أ���A����
B���÷�Ӧ���ڸ��ֽⷴӦ������������ԭ��Ӧ�����Բ�����Ƴ�ԭ��أ���B��ȷ��
C���÷�Ӧ�����Է���������ԭ��Ӧ����������Ƴ�ԭ��أ���C����
D���÷�Ӧ�����Է���������ԭ��Ӧ����������Ƴ�ԭ��أ���D����
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� ��ҵ������������������ȼ�գ������ò�������ˮ�Ʊ����ᡣ������������ԭ���ԭ��ֱ���Ʊ������ͬʱ��ȡ���ܣ����������뷨���У�����˵���϶��������
A���������϶��ý���������һ��Ũ�ȵ��������������Һ
B��ͨ�������ĵ缫Ϊԭ��ص�����
C���÷����ɽ���ѧ����ȫת��Ϊ����
D��ͨ�����ĵ缫�����ķ�ӦΪ��H2 �� 2H��+2e��
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
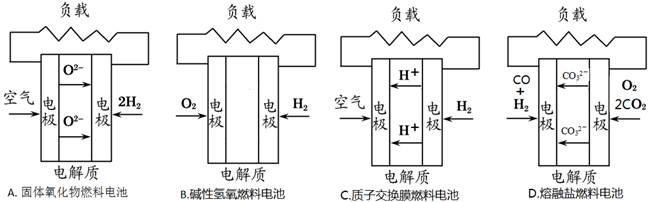
4��ѡ���� ������4��ȼ�ϵ�صĹ���ԭ��ʾ��ͼ������������Ӧ�IJ���Ϊˮ����
�ο��𰸣�C
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ���ݴ˿����жϡ�A���ڹ���������ȼ�ϵ���У�������Ӧʽ��O2+4e-��2O2-����A���������⣻B������ȼ�ϵ���У�������ӦʽO2+2H20+4e-��4OH-����B���������⣻C�����ӽ���Ĥȼ�ϵ�أ�������Ӧʽ4H++O2+4e-��2H20����C��ȷ��D��������ȼ�ϵ���У�������Ӧʽ��2CO2+O2+4e-��2CO32-����D���������⣬��ѡC��
�����Ѷȣ�һ��
5��ѡ���� ��þ��������ƽ�в���ʢ��һ��Ũ�ȵ�NaOH��Һ���ձ��У��õ��ߺ͵��������ӳ�ԭ��أ�װ����ͼ��ʾ���˵�ع���ʱ������������ȷ����(? )

A��Mg��Al���ã�Mgʧȥ���ӱ�������Mg2+
B������������������Ĥ�����ɲ��ش���
C���õ�ص������·�У����������ɵ��Ӷ����ƶ��γɵ�
D��Al�ǵ�ظ�������ʼ����ʱ��Һ�л������а�ɫ��������
�ο��𰸣�B
������������������龳��ԭ��ص�������⣬����Ĺؼ���Ȼ��Ҫ��ȷԭ��ع���ʱ����Ӧ���Է�������ԭ��Ӧ���ڼ��������£�����þ���ܷ�����Ӧ��������Al������NaOH��Ӧ����NaAlO2��H2����AlΪ��ԭ������ԭ��ظ�����A��������ҺΪNaOH��Һ��Alʧ���ӣ�Ϊ����������B��������������ĤΪAl2O3��Al2O3����NaOH��Һ��Ӧ���ʲ��ش������ԡ�C����ڵ�·�е��������������Ӷ����ƶ��γɵģ�����D���ع���ʱ��Ԫ�صķ�ӦΪAl��AlO2-������������������
�����Ѷȣ�һ��