��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� A��B��C��D��E������������ͬ�ĵ�����������֮���ܷ������·�Ӧ��A+B=C+D�������B��D��E?���B�������а�ɫ������B��������������ش�
��1���û�ѧ���ű�ʾ����4������A��______B��______C��______D��______
��2��д��B��D��E?���B����ʱ�����ӷ���ʽ��______��
�ο��𰸣�A��B��C��D��E������������ͬ�ĵ����������Դ�10�������������жϣ�10��������
һ�ˣ�Ne��N3-��O2-��F-��Na+��Mg2+��Al3+
���ˣ�HF��OH-
���ˣ�H2O��NH2-
�ĺˣ�NH3��H3O+
��ˣ�CH4��NH4+
����֮���ܷ������·�Ӧ��A+B=C+D���ƶ�AΪNH4+��BΪOH-��CΪNH3��DΪH2O�������B��D��E ���B�������а�ɫ������B������������˵�������ܽ���B��OH-���У��ƶ�EΪAl3+��
��1����ѧ���ű�ʾ����4����Ϊ��AΪNH4+��BΪOH-��CΪNH3��DΪH2O���ʴ�Ϊ��NH4+��OH-��NH3��H2O��
��2��B��D��E ���B����ʱ�����ӷ���ʽΪ��Al3++4OH-�TAlO-+2H2O���ʴ�Ϊ��Al3++4OH-�TAlO-+2H2O��
���������
�����Ѷȣ�һ��
2���ƶ��� A��B��C��D��E��F��G��H��I����ѧ��ѧ�г��������壬���Ǿ��ɶ�����Ԫ����ɣ������������ʣ�
��A��B��E��F��G��ʹʪ�����ɫʯ����ֽ��죬I��ʹʪ��ĺ�ɫʯ����ֽ������C��D��H����ʹʪ���ʯ����ֽ��ɫ��
��A��I����������ɫ������
��B��E����ʹƷ����Һ��ɫ��
�ܽ����ȵ�ͭ˿����װ��B��ƿ�У�ƿ�ڳ����ػ�ɫ���̣�
�ݽ���ȼ��þ������װ��F��ƿ�У�þ������ȼ�գ����ɰ�ɫ��ĩ��ƿ�ڱڸ��ź�ɫ������
��C��D�������ɺ���ɫ���壻
��G��D��ȼ�տ��Բ���E��H2O��
�ཫB��H��ƿ�л�Ϻ����������ü����ӣ�ƿ�ڱڳ�����״Һ�β�����A��
�ش��������⣺
(1)A�Ļ�ѧʽ��____�����������Ļ�ѧʽ��_________��
(2)���з�����Ӧ�Ļ�ѧ����ʽ��____��
(3)���з�����Ӧ�Ļ�ѧ����ʽ��____��
(4)C�Ļ�ѧʽ��____��D�Ļ�ѧʽ��__________��
(5)���з�����Ӧ�Ļ�ѧ����ʽ��____��
(6)H�Ļ�ѧʽ��____��
�ο��𰸣�(1)HCl��NH4Cl
(2)Cu+Cl2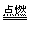 CuCl2
CuCl2
(3)2Mg+CO 2MgO+C
2MgO+C
(4)NO��O2
(5)2H2S+3O2 2SO2+2H2O
2SO2+2H2O
(6)CH4
���������
�����Ѷȣ�һ��
3������� ��5�֣���������ѧ��ѧ�г������ʵ�ת����ϵͼ�У���֪������AΪ����ɫ���塢BΪ�������ʣ�D��E��M�dz������嵥�ʣ�����MΪ����ɫ��N��θ����Ҫ�ɷ֣���ҵ����E��M����ȡN�����ƶϣ�
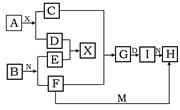
��1��д�����л�ѧʽ? A??I?
��2��Gת��ΪI������Ϊ?
��3��F+M��H���ӷ���ʽΪ?
��4��A+X��C+D�Ļ�ѧ����ʽΪ________________________
�ο��𰸣���1��Na2O2��Fe(OH)3����2����ɫ����Ѹ��ת��Ϊ����ɫ�����ת��Ϊ���ɫ��
��3��2Fe2����Cl2=2Fe3��?(4)2Na2O2��2H2O=4NaOH��O2��
���������MΪ����ɫ����M��������N��θ����Ҫ�ɷ֣���N���Ȼ��⡣AΪ����ɫ���壬���A�ǹ������ơ�BΪ�������ʣ���E��������F���������Լ�����Ӧ��˵��B�DZ�۽�������Ϊ��������F���Ȼ�������H���Ȼ�����D��������Ӧ������D��������X��ˮ��C���������ƣ�G��������������I������������
�����Ѷȣ�һ��
4������� ��8�֣�A��B��C��D��E��F��G���������У�����A��D��EΪ���ʣ���D��EΪ��̬��GΪҺ̬������֮���������ת����ϵ��
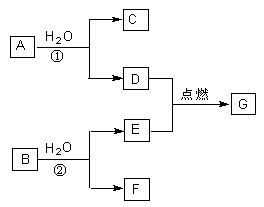
��1����A��B���������ʱ�����ɵ�D��Eǡ����ȫ��Ӧ����C�ĵ���ʽ��?����Ӧ�ڵ����ӷ���ʽ�� ?��
?��
��2����A��B��������Ϊ38��21ʱ�����ɵ�D��E�����ʵ���֮��Ϊ1��2����ǡ����ȫ��Ӧ����B�ĵ���ʽΪ?����Ӧ�ٵĻ�ѧ����ʽ��??��
�ο��𰸣�

�����������
�����Ѷȣ�һ��
5������� ��8�֣��ס��ҡ����������ʶ�����AԪ�أ�ֻ�м��ǵ��ʣ���ת����ϵ���£�

��1��������Ŀǰ���糫��������ŷŵ��������壬��Ҳ����AԪ�ء�����7�����ӵĺ���A���÷��ű�ʾΪ?������Һ�ʼ��Ե�ԭ�������ӷ���ʽ��ʾΪ?��
��2����A�Ƿǽ���Ԫ�أ������������������������2�����������ִ�ͨѶ�п���������?��д��һ���б��μӵġ���֤��̼�ķǽ�����ǿ��A�Ļ�ѧ����ʽ?��
��3����������������õĹ��ɽ������ʣ����ڵ�ȼ������������Ӧ�����ҡ�������ϡ���ᣬ���ҡ����Ļ�ѧ����ʽΪ?��
�ο��𰸣���8 �֣����������͡�����1�֣����ظ��۷֣�
��1��136C��1�֣�? CO32��+ H2O HCO3?+ OH����2 �֣���û���治�÷֣�
HCO3?+ OH����2 �֣���û���治�÷֣�
��2�����ά��1 �֣���? Na2SiO3 + H2O + CO2 ="=" H2SiO3��+ Na2CO3��2 �֣�
��3�� Fe3O4 + 8 HCl="=" 2FeCl 3 + FeCl 2+ 4 H2O��2 �֣�
����������ƶ�������Ҫ��ͻ�ƿڣ������ǵ��ʡ��DZ����һ�����ۣ�����һ�������
��1����������ͬʱ����������Ƕ�����̼�������C������CO2���������ҷ�Ӧͬʱ����AԪ�أ�˵��������CO32����������HCO3?����ʾ����Ҫ�����ָ�ԭ�ӵ�������������A��136C��13C��̼���γʼ��Ե�ԭ����̼������ӵ�ˮ����ɵģ�CO32��+ H2O HCO3?+ OH��
HCO3?+ OH��
��2������������������������2���ó���Si�������Ƕ������裬���������������ƣ������ǹ����ơ�֤��Ԫ�صķǽ�����ǿ���������ȱȽ϶�Ӧ����������ˮ���������ǿ�������̼��������ɹ��ᣬ˵��̼�������ǿ�ڹ��ᣬ��һ��֤��C�ķǽ�����ǿ��Si��
��3����õĹ��ɽ������ʾ���������ȼ���������ɵ���Fe3O4������Fe2O3��Ҫע�����֡�
�������������ڱȽ��ۺϵ����⣬�����࣬��Ҫѧ�������ѧ֪ʶ���з�������������������ѧ���۽��н��ͣ��Ѷ��еȡ�
�����Ѷȣ�һ��